药品补充申请申报资料及技术要求(征求意见稿)注册事项:21
变更直接接触药品的包装材料或者容器(除第10事项外,即除注射剂、眼用制剂、气雾剂、粉雾剂、喷雾剂外)一、申报资料项目及其说明:1
药品批准证明文件及其附件的复印件:包括与申请事项有关的本品各种批准文件,如药品注册批件、补充申请批件、商品名批准文件、药品标准颁布件、药品标准修订批件和统一换发药品批准文号的文件、《新药证书》等
附件包括上述批件的附件,如原药品标准、说明书、标签样稿及其他附件
证明性文件:2
1申请人是药品生产企业的,应当提供《药品生产许可证》及其变更记录页、营业执照、《药品生产质量管理规范》认证证书复印件
2变更后包装材料的药包材注册证
修订的药品说明书样稿,并附详细修订说明
修订的药品标签样稿,并附详细修订说明
药学研究资料:5
1以文字或列表方式说明变更前包装材料和容器、变更后包装材料和容器,主要变化及原因
2对变更前后处方工艺进行比较,说明处方工艺是否发生改变
3对变更前后产品质量进行对比研究,尤其是杂质状况
4对新包装3批样品进行加速试验及长期留样考察,并与原包装产品的稳定性情况进行比较
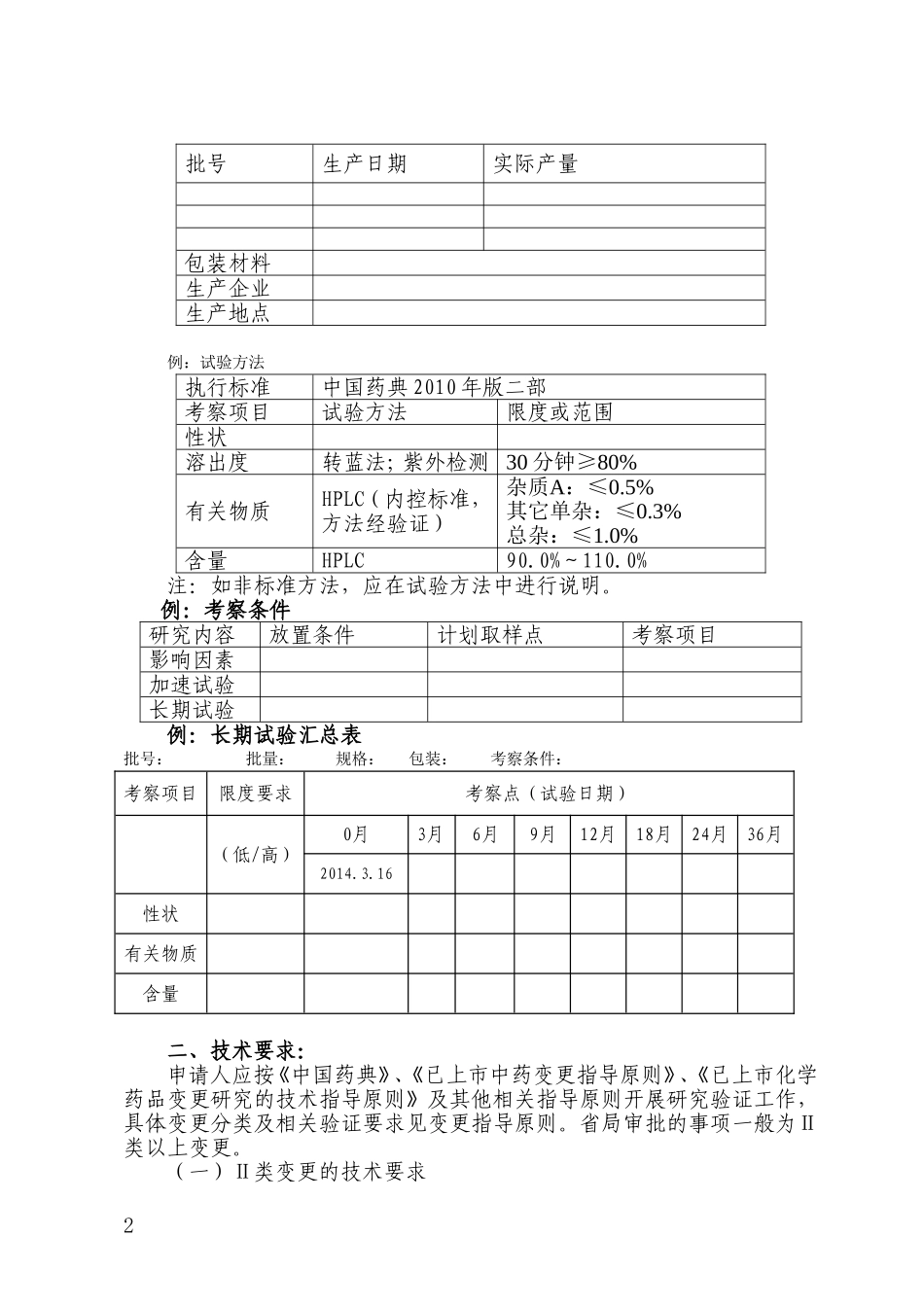
稳定性研究资料分为三部分:(1)稳定性试验方案,一般包括a
样品有关信息(生产企业、批号、批产量、生产时间、包装材料等),可列表说明;b
试验项目及试验方法;c
稳定性试验安排(考察时间及进行的检查项目)各项检查可接受的限度或范围
(2)按照每批样品分别提供加速稳定性和长期稳定性考察数据,一般按表格形式进行说明,有数据的需列出详细数据,不能仅写“符合规定”,如有关物质
(3)根据稳定性考察结果对产品稳定性进行分析评价,明确新包装的有效期
(4)相关研究图谱
5直接接触药品的包装材料和容器的选择依据及质量标准、包材生产企业提供的检验报告书
6该产品的药品质量标准