九年级化学公开课教学设计课题:溶解度及溶解度曲线目标:(一)知识与能力:1、了解溶解度的概念,初步学会绘制和查阅溶解度曲线
2、知道气体溶解度的表示方法及其影响
(二)过程与方法:通过溶解曲线绘制的探究掌握溶解度概念及影响因素
(三)情感态度与价值观:感受用溶解度知识对一些问题的解释
重点:溶解度概念,溶解度曲线绘制的探究气体溶解度及其影响因素
难点:溶解量,溶解性与溶解度三者的关系
教程:[复习]讨论下列各题是否正确1、某溶液一旦达到饱和、便无法再分溶解原有的溶质了
()2、在溶液中有固体长期存在,该溶液必定饱和
()3、在溶液中物质被溶剂溶解了的量称为溶解量
()[设问]什么叫溶解性
[讲述]一种物质在某溶剂里中溶解能力的大小称为该物质在这种溶剂中的溶解性,决定溶解性大小内因是溶质与溶剂的本性,外因是温度和压强,溶解性可分哪几个等级
(学生看表回答)溶解性易溶可溶微溶难溶或不溶溶解度>10克>1克<1克<0.01克一、[概念的形成]1、用“溶解量或溶解性”能定量地比较KNO3与KClO3在水中的溶解能力的大小吗
2、在一定温度下一定溶剂中,蔗糖的溶解量有一个限度,科学上如何量度这种溶解限度
3、阅读课文,讨论溶解度的概念
溶解度是用的质量克数来定量表达的,它有三个前提:①外界条件——一定温度下;②溶剂的比较标准——每100g水中;③溶液的状态——已达到饱和
二、溶解度的表示方法:1、列表法2、坐标法(绘制和查阅溶解度曲线)[练习]1、查阅图7—11,200C时NH4NO3的溶解度是,600C时50g水最多能溶解gNH4Cl,200C时KNO3的溶解能力比NanO3(大小或一样)800C时会发生什么变化
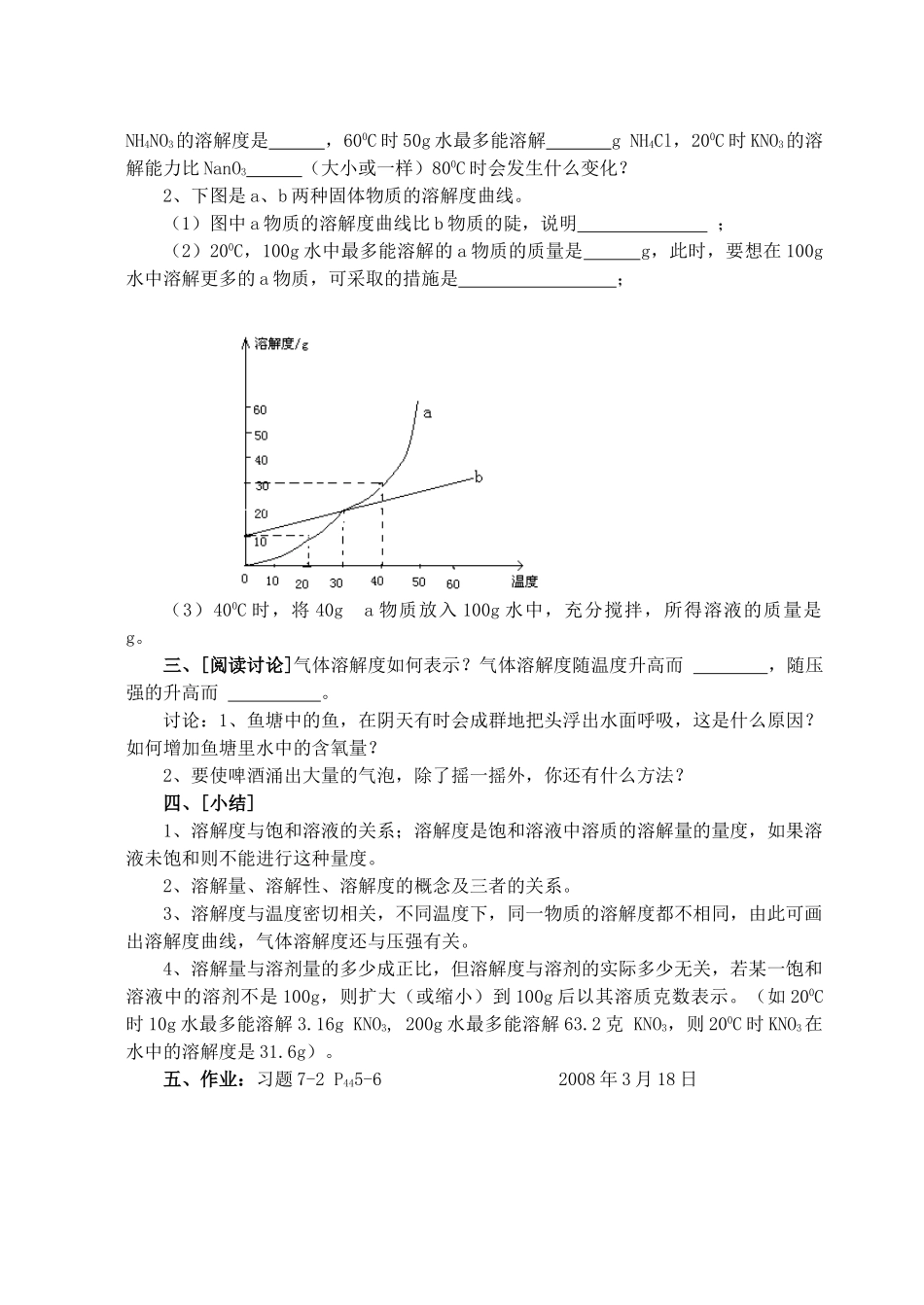
2、下图是a、b两种固体物质的溶解度曲线
(1)图中a物质的溶解度曲线比b物质的陡,说明;(2)200C,100g水中最多能溶解的a物质的质量是g,此时,要想