学习内容专题二复习课学习目标的检验方法
3.根据实验事实了解氧化还原反应的本质是电子的转移,举例说明生产、生活中常见的氧化还原反应
4.通过实验了解氯等非金属及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响
过程方法:学会归纳化学知识的方法
情感态度与价值观:认识海水是人类宝贵的自然资源,培养与大自然友好相处
学习重点氯单质及其化合物、钠单质及其化合物的性质和用途学习难点氧化还原反应的分析和离子方程式的正确书写
教学过程用案人自我创新一、知识网络:NaNaOHNaHCO3Na2CO3Cl2Ca(ClO)2MgMgSO4海水(Cl-,Br-,I-,Na+,Mg2+)Br2I2二.知识重点:1、氧化还原反应的判断的分析:化合价降低,得到电子,被还原氧化剂+还原剂=====还原产物+氧化产物化合价升高,失去电子,被氧化【总结】高失氧还原剂低得还氧化剂2、离子方程式:步骤:写——拆——删——查三氯气的性质1
铁与氯气反应方程式:
铁与盐酸反应方程式:
氯气与水反应方程式:
制漂白粉的化学反应方程式:
【例题】ClO2是一种杀菌效率高、二次污染小的水处理剂
实验室可以通过下列反应值得ClO2:2KClO3+H2C2O4+H2SO4△2ClO2↑+K2SO4+2CO2↑+H2O下列说法正确的是()A
KClO3在反应中得到电子B
H2C2O4在反应中被氧化C
ClO2是氧化产物D
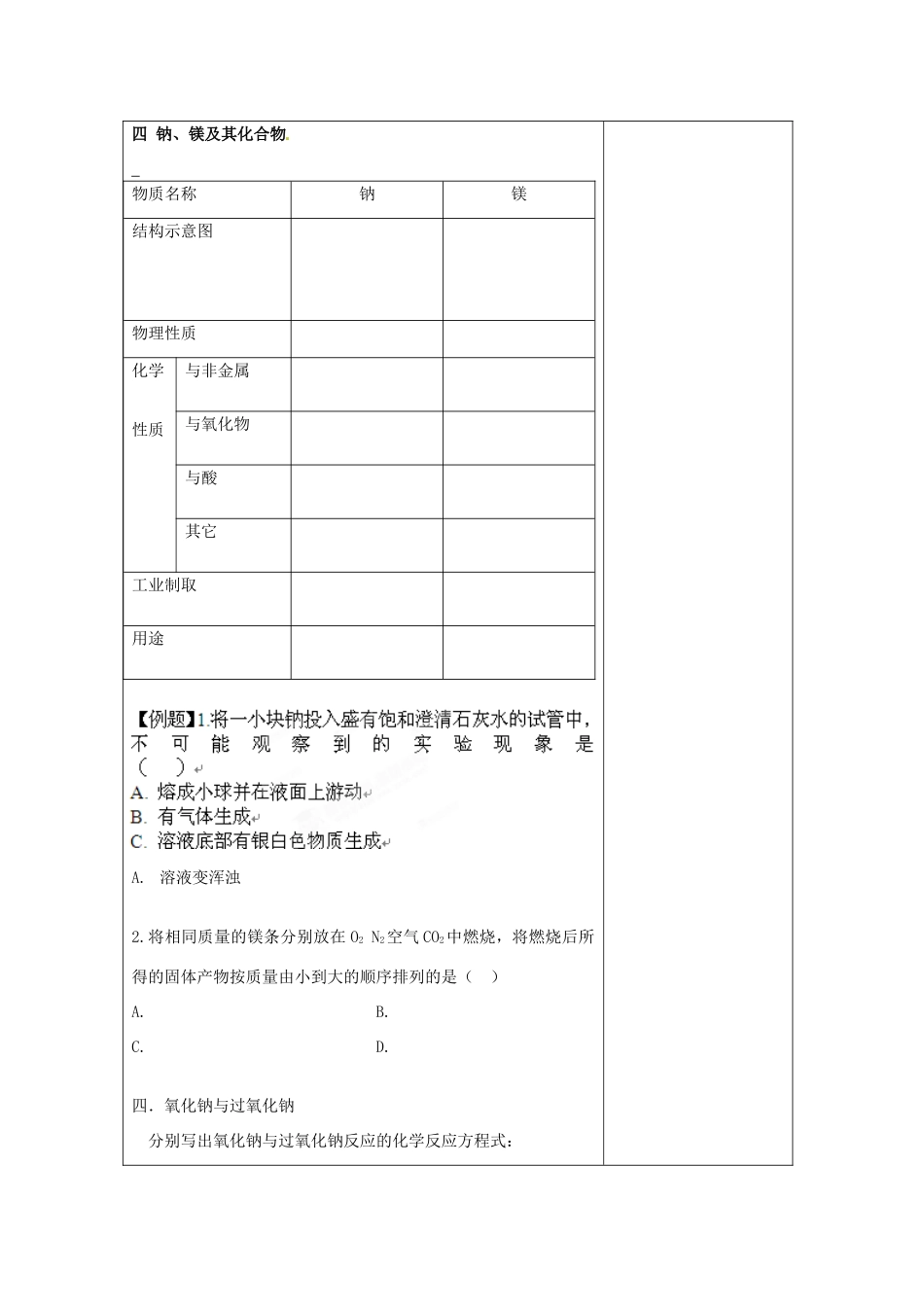
1molKClO3参加反应有2mol电子转移四钠、镁及其化合物物质名称钠镁结构示意图物理性质化学性质与非金属与氧化物与酸其它工业制取用途A
溶液变浑浊2
将相同质量的镁条分别放在O2N2空气CO2中燃烧,将燃烧后所得的固体产物按质量由小到大的顺序排列的是()A
四.氧化钠与过氧化钠分别写出氧化钠与过氧化钠反应的化学反应方程式:五.碳酸钠与碳酸氢钠与酸盐酸与碱NaOHCa(O