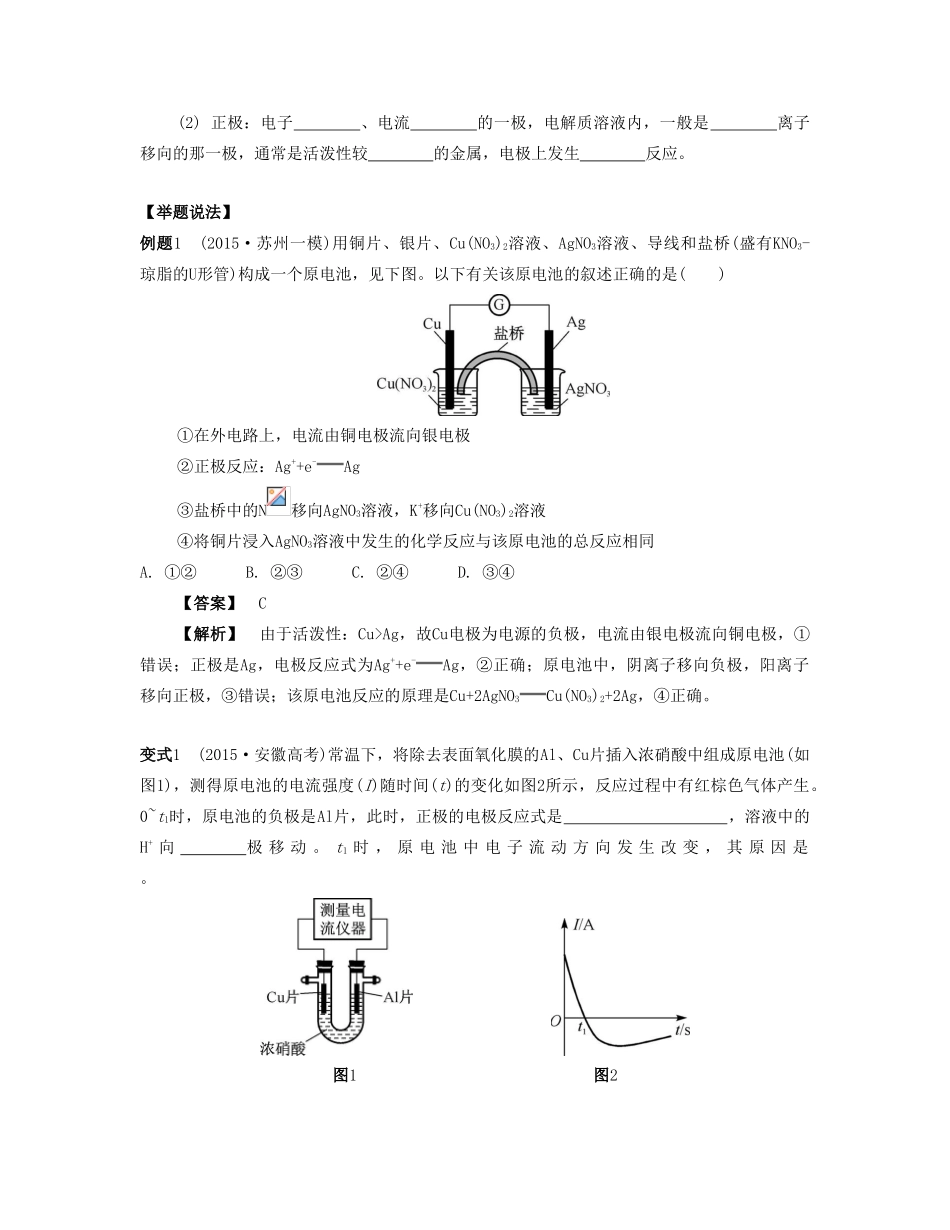
课时17原电池及其应用(本课时对应学生用书第74~78页)【课时导航】复习目标1.理解原电池工作原理,能写出常见的简单电极反应式和电池总反应方程式。2.了解常见的化学电源,认识化学能与电能相互转化的实际意义及其重要应用。3.认识金属腐蚀的危害,理解金属发生电化学腐蚀的原因,能运用恰当的措施防止铁、铝等金属腐蚀。4.了解提高燃料的燃烧效率、开发高能清洁燃料电池和研制新型化学电源的重要性。认识化学在解决能源危机中的重要作用。知识网络问题思考问题1判断原电池正、负极的方法有哪些?问题2原电池原理有哪些应用?【自主学习】考点1原电池的工作原理【基础梳理】1.概念:原电池是将转化为的装置。2.构成原电池的条件:(1)一般有两个的电极。(2)将电极插入中。(3)用导线连接电极构成。(4)能自发进行的。3.电极及电极反应(1)负极:电子、电流的一极,电解质溶液内,一般是离子移向的那一极,通常是活泼性较的金属,电极上发生反应。(2)正极:电子、电流的一极,电解质溶液内,一般是离子移向的那一极,通常是活泼性较的金属,电极上发生反应。【举题说法】例题1(2015·苏州一模)用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(盛有KNO3-琼脂的U形管)构成一个原电池,见下图。以下有关该原电池的叙述正确的是()①在外电路上,电流由铜电极流向银电极②正极反应:Ag++e-Ag③盐桥中的N移向AgNO3溶液,K+移向Cu(NO3)2溶液④将铜片浸入AgNO3溶液中发生的化学反应与该原电池的总反应相同A.①②B.②③C.②④D.③④【答案】C【解析】由于活泼性:Cu>Ag,故Cu电极为电源的负极,电流由银电极流向铜电极,①错误;正极是Ag,电极反应式为Ag++e-Ag,②正确;原电池中,阴离子移向负极,阳离子移向正极,③错误;该原电池反应的原理是Cu+2AgNO3Cu(NO3)2+2Ag,④正确。变式1(2015·安徽高考)常温下,将除去表面氧化膜的Al、Cu片插入浓硝酸中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。0~t1时,原电池的负极是Al片,此时,正极的电极反应式是,溶液中的H+向极移动。t1时,原电池中电子流动方向发生改变,其原因是。图1图2【答案】2H++N+e-NO2↑+H2O正Al在浓硝酸中发生钝化,氧化膜阻止了Al的进一步反应【解析】0~t1时,原电池的负极是Al片,溶液中产生的红棕色气体是二氧化氮,故正极反应式为2H++N+e-NO2↑+H2O,此时溶液中的氢离子移向正极;一段时间后,由于Al在浓硝酸中发生钝化,导致原电池中Al作正极,Cu作负极,电子流动方向改变。原电池正、负极的判断方法考点2常见的化学电源【基础梳理】1.一次电池:只能使用一次,不能充电复原继续使用。(1)干电池总反应:Zn+2MnO2+2NH4ClZnCl2+Mn2O3+2NH3+H2O负极:正极:2N+2e-2NH3+H2↑、2MnO2+H2Mn2O3+H2O(2)碱性锌锰电池总反应:Zn+2MnO2+H2OZn(OH)2+Mn2O3负极:正极:2.二次电池:放电后能充电复原继续使用。铅蓄电池总反应:Pb+PbO2+2H2SO42PbSO4+2H2O放电时——原电池负极:正极:充电时——电解池阴极:阳极:放电时原电池的负极作充电时电解池的极。3.燃料电池:将燃料燃烧的化学能直接转化为电能的装置。(1)氢氧燃料电池总反应:①酸性介质负极:正极:②碱性介质负极:正极:③熔融的金属氧化物作介质负极:正极:④碳酸盐作介质负极:正极:(2)乙醇-氧气燃料电池(正极反应式与氢氧燃料电池正极反应式相同,下面只需写出负极反应式即可)①(碱性介质)②(酸性介质)③(碳酸盐作介质)④(熔融的金属氧化物作介质)【举题说法】例题2(2015·江苏高考)一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是()A.反应CH4+H2O3H2+CO,每消耗1molCH4转移12mol电子B.电极A上H2参与的电极反应为H2+2OH--2e-2H2OC.电池工作时,C向电极B移动D.电极B上发生的电极反应为O2+2CO2+4e-2C【答案】D【解析】反应CH4+H2O3H2+CO,C元素化合价由-4价升高到+2价,H元素化合价由+1价降低到0价,每消耗1molCH4转移6mol电子,故A错误;电解质为熔融碳酸盐,H2参与的反应为H2+C-2e-H2O+2CO2,故B错误;电池工作时,C向负极移动,即向电极A移动,故C错误;B为正极,氧气得电子结合CO2生...