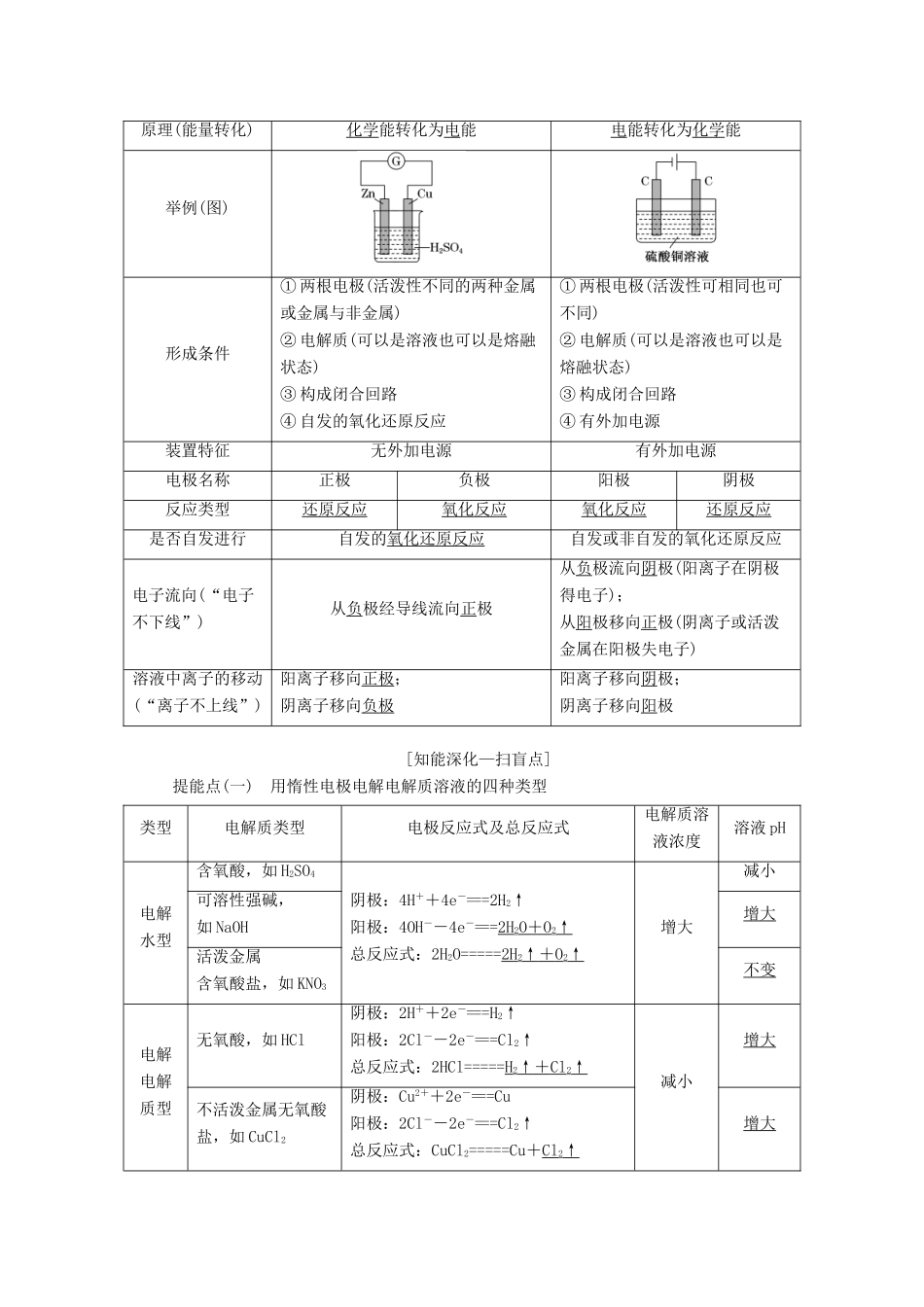
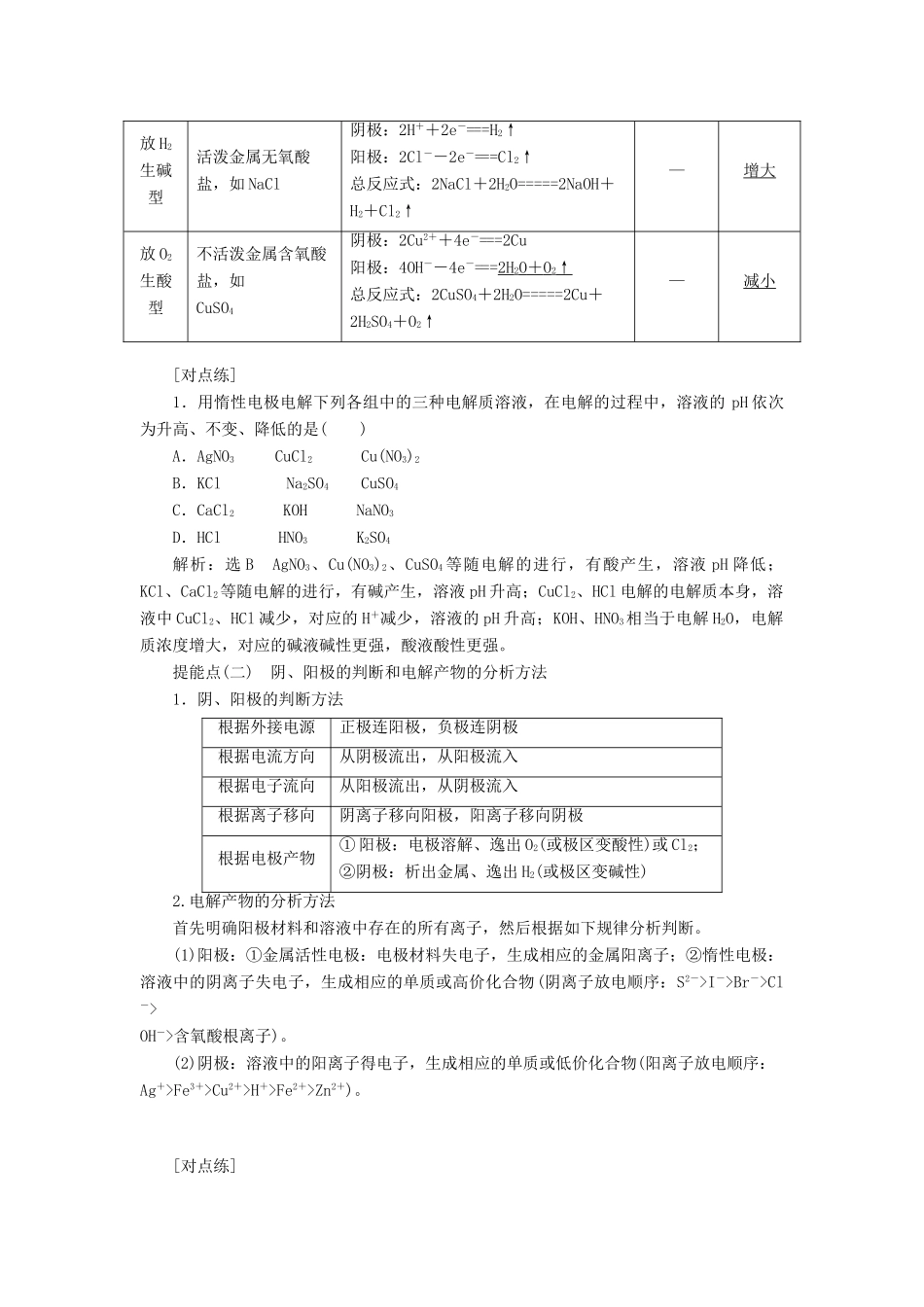
电解池金属的腐蚀与防护[江苏考纲要求]————————————————————————————————————1.理解电解池的工作原理,能写出简单电极反应式和电池反应方程式。2.认识金属腐蚀的危害,理解金属发生电化学腐蚀的原理,能运用恰当的措施防止铁、铝等金属腐蚀。[教材基础—自热身]1.电解使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。在此过程中,能转化为化学能。2.电解池(1)概念:电解池是把电能转化为化学能的装置。(2)电解池的构成条件:①有外接电源;②有与电解质溶液或熔融的电解质相连的两个电极;③形成闭合回路。[注意]其中与电源正极相连的为阳极,与电源负极相连的为阴极。阴极材料分为两类,一类为惰性电极,如石墨、Pt、Ti、Au等导体构成;另一类为活性电极,电极材料参与反应,包括Cu、Ag及比Cu、Ag活泼的金属。(3)电极名称及电极反应式(以电解CuCl2溶液为例)总反应方程式:CuCl2=====Cu+Cl2↑。(4)电解池中电子和离子的移动:①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流向电源的正极。②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。3.在惰性电极上离子的放电顺序(1)阴极(与电极材料无关):(2)阳极(与电极材料有关):4.原电池和电解池的比较装置类别原电池电解池电解原理原理(能量转化)化学能转化为电能电能转化为化学能举例(图)形成条件①两根电极(活泼性不同的两种金属或金属与非金属)②电解质(可以是溶液也可以是熔融状态)③构成闭合回路④自发的氧化还原反应①两根电极(活泼性可相同也可不同)②电解质(可以是溶液也可以是熔融状态)③构成闭合回路④有外加电源装置特征无外加电源有外加电源电极名称正极负极阳极阴极反应类型还原反应氧化反应氧化反应还原反应是否自发进行自发的氧化还原反应自发或非自发的氧化还原反应电子流向(“电子不下线”)从负极经导线流向正极从负极流向阴极(阳离子在阴极得电子);从阳极移向正极(阴离子或活泼金属在阳极失电子)溶液中离子的移动(“离子不上线”)阳离子移向正极;阴离子移向负极阳离子移向阴极;阴离子移向阳极[知能深化—扫盲点]提能点(一)用惰性电极电解电解质溶液的四种类型类型电解质类型电极反应式及总反应式电解质溶液浓度溶液pH电解水型含氧酸,如H2SO4阴极:4H++4e-===2H2↑阳极:4OH--4e-===2H2O+O2↑总反应式:2H2O=====2H2↑+O2↑增大减小可溶性强碱,如NaOH增大活泼金属含氧酸盐,如KNO3不变电解电解质型无氧酸,如HCl阴极:2H++2e-===H2↑阳极:2Cl--2e-===Cl2↑总反应式:2HCl=====H2↑+Cl2↑减小增大不活泼金属无氧酸盐,如CuCl2阴极:Cu2++2e-===Cu阳极:2Cl--2e-===Cl2↑总反应式:CuCl2=====Cu+Cl2↑增大放H2生碱型活泼金属无氧酸盐,如NaCl阴极:2H++2e-===H2↑阳极:2Cl--2e-===Cl2↑总反应式:2NaCl+2H2O=====2NaOH+H2+Cl2↑—增大放O2生酸型不活泼金属含氧酸盐,如CuSO4阴极:2Cu2++4e-===2Cu阳极:4OH--4e-===2H2O+O2↑总反应式:2CuSO4+2H2O=====2Cu+2H2SO4+O2↑—减小[对点练]1.用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的pH依次为升高、不变、降低的是()A.AgNO3CuCl2Cu(NO3)2B.KClNa2SO4CuSO4C.CaCl2KOHNaNO3D.HClHNO3K2SO4解析:选BAgNO3、Cu(NO3)2、CuSO4等随电解的进行,有酸产生,溶液pH降低;KCl、CaCl2等随电解的进行,有碱产生,溶液pH升高;CuCl2、HCl电解的电解质本身,溶液中CuCl2、HCl减少,对应的H+减少,溶液的pH升高;KOH、HNO3相当于电解H2O,电解质浓度增大,对应的碱液碱性更强,酸液酸性更强。提能点(二)阴、阳极的判断和电解产物的分析方法1.阴、阳极的判断方法根据外接电源正极连阳极,负极连阴极根据电流方向从阴极流出,从阳极流入根据电子流向从阳极流出,从阴极流入根据离子移向阴离子移向阳极,阳离子移向阴极根据电极产物①阳极:电极溶解、逸出O2(或极区变酸性)或Cl2;②阴极:析出金属、逸出H2(或极区变碱性)2.电解产物的分析方法首先明确阳极材料和溶液中存在的所有离子,然后根据如下规律分析判...