第1节化学反应的热效应(第三课时)学习目标:掌握盖斯定律,并会计算反应的焓变
【复习】写出下列反应的热化学方程式(1)1molC2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366
(2)18g葡萄糖与适量O2(g)反应,生成CO2(g)和H2O(l),放出280
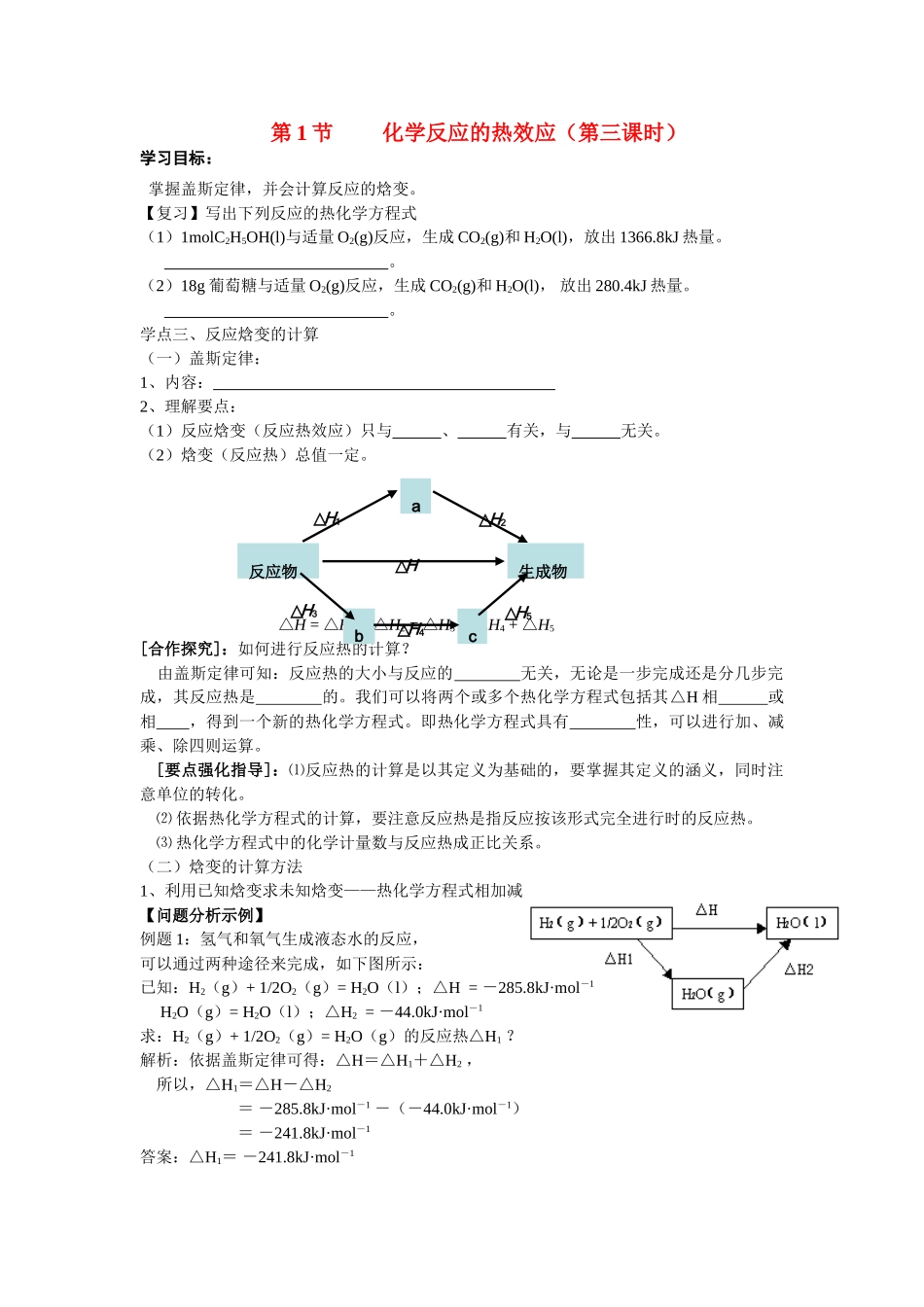
学点三、反应焓变的计算(一)盖斯定律:1、内容:2、理解要点:(1)反应焓变(反应热效应)只与、有关,与无关
(2)焓变(反应热)总值一定
△H=△H1+△H2=△H3+△H4+△H5[合作探究]:如何进行反应热的计算
由盖斯定律可知:反应热的大小与反应的无关,无论是一步完成还是分几步完成,其反应热是的
我们可以将两个或多个热化学方程式包括其△H相或相,得到一个新的热化学方程式
即热化学方程式具有性,可以进行加、减乘、除四则运算
[要点强化指导]:⑴反应热的计算是以其定义为基础的,要掌握其定义的涵义,同时注意单位的转化
⑵依据热化学方程式的计算,要注意反应热是指反应按该形式完全进行时的反应热
⑶热化学方程式中的化学计量数与反应热成正比关系
(二)焓变的计算方法1、利用已知焓变求未知焓变——热化学方程式相加减【问题分析示例】例题1:氢气和氧气生成液态水的反应,可以通过两种途径来完成,如下图所示:已知:H2(g)+1/2O2(g)=H2O(l);△H=-285
8kJ·mol-1H2O(g)=H2O(l);△H2=-44
0kJ·mol-1求:H2(g)+1/2O2(g)=H2O(g)的反应热△H1
解析:依据盖斯定律可得:△H=△H1+△H2,所以,△H1=△H-△H2=-285
8kJ·mol-1-(-44
0kJ·mol-1)=-241
8kJ·mol-1答案:△H1=-241
8kJ·mol-1反应物a生成物△H△H2△H1cb△H5△H4△H3【例2