第一节常见的金属材料第2课时炼铁的原理【学习目标】1、了解炼铁的原理,知道还原反应的概念2、掌握含杂质的化学方程式的计算【学习重点】含杂质的化学方程式的计算【学习过程】学习任务一:探究炼铁的化学反应原理活动1、阅读P30一、二自然段的内容,回答:⑴铁在自然界中大多以形式存在⑵常见的铁矿石主要有哪几种
每种矿石的主要成分分别是什么
活动2、观察P30页活动天地,回答:⑴反应原理:⑵实验现象:、⑶如何判断反应中生成了什么物质
⑷装置中右边的酒精灯起什么作用
⑸在上述反应中氧化铁失而一氧化碳得
小结:还原反应
学习任务二:掌握含杂质的化学方程式的计算例:用2000t含氧化铁75%的赤铁矿石,理论上可以炼出多少吨铁
二、合作共建:讨论交流完成下列各题1、一氧化碳还原氧化铁的实验中为什么先通入一氧化碳再加热
实验后是先停止加热还是先停止通一氧化碳
2、在进行含杂质的有关计算时,应注意什么问题
三、诊断评价:1、常见的铁矿石有、、、等,常用来炼铁的有、等,炼铁的主要原理是
2、用赤铁矿炼铁,CO是()A、助燃剂B、还原剂C、氧化剂D、催化剂3、下列物质中,属于化合物的是()A、生铁B、铁矿石C、赤铁矿D、四氧化三铁4、现有①磁铁矿(主要成分是Fe3O4)、②黄铁矿(主要成分是FeS2)③赤铁矿(主要成分是Fe2O3),请你从多角度分析三种矿石中不适合用来炼铁的是(填序号),原因是
5、某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿(主要成分为Fe2O3)、空气等,主要反应过程如下所示:焦炭⑴在上面方框中写出有关反应中生成物的化学式⑵写出②③两步反应的化学方程式
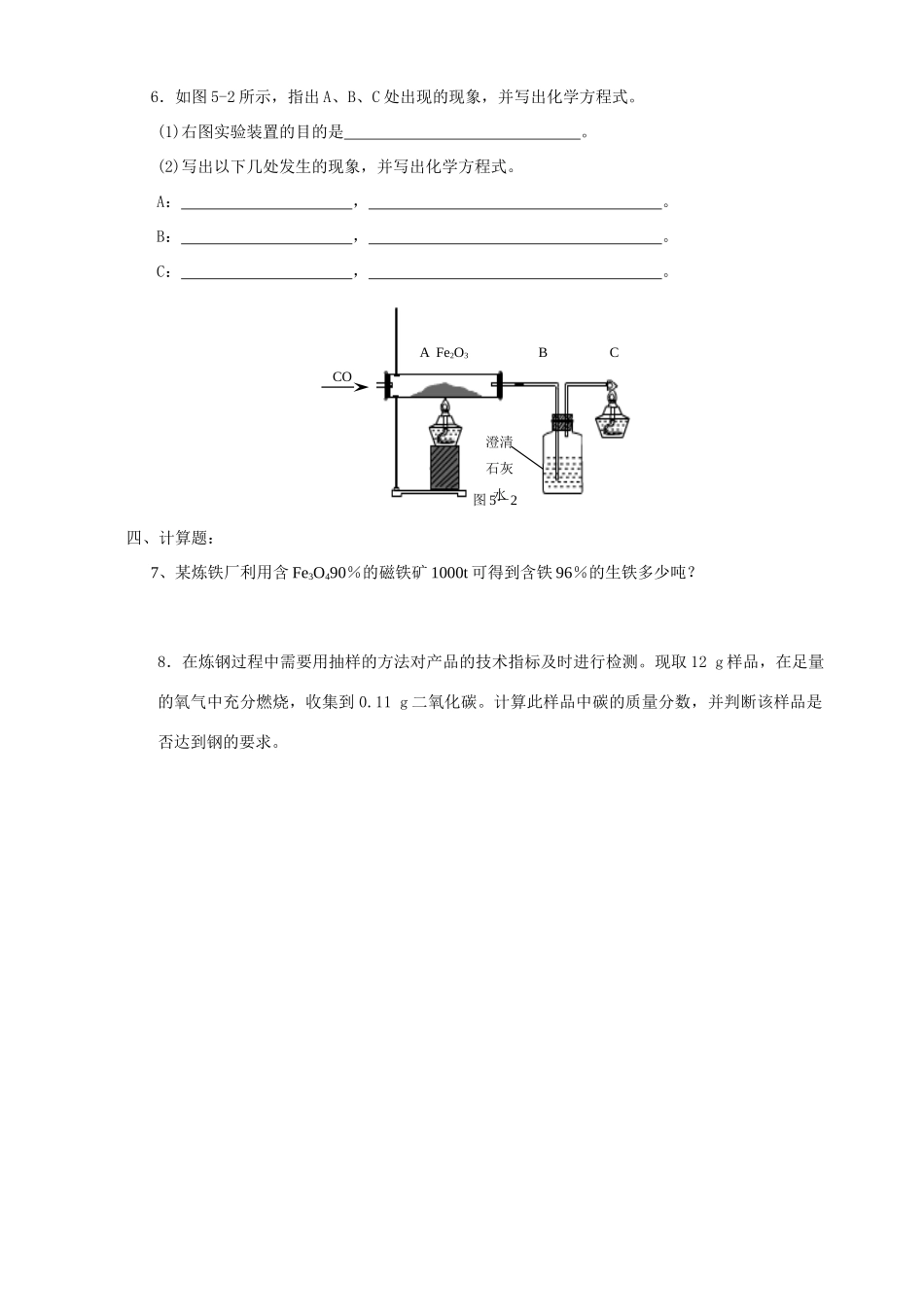
②③铁过量空气、高温①焦炭、高温赤铁矿、高温②③6.如图5-2所示,指出A、B、C处出现的现象,并写出化学方程式
(1)右图实验装置的目的是
(2)写出以下几处发生的现象,并写出化学方程式