离子晶体教案课题:第四节离子晶体授课班级课时一课时教学目的知识与技能1、理解离子晶体的结构模型及其性质的一般特点
2、了解离子晶体中离子晶体配位数及其影响因素
3、了解决定离子晶体结构的重要因素
过程与方法通过学习离子晶体的结构与性质,培养运用知识解决实际问题的能力,培养学生的空间想像能力情感态度价值观通过学习离子晶体的结构与性质,激发学生探究热情与精神
进一步认识“结构决定物质性质”的客观规律重点离子晶体的结构模型及其性质的一般特点;离子晶体配位数及其影响因素;难点离子晶体配位数及其影响因素;知识结构与板书设计第四节离子晶体一、离子晶体1、定义:由阳离子和阴离子通过离子键结合而成的晶体
2、构成微粒:阴阳离子3、微粒间的作用:阴阳离子间以离子键结合,离子内可能有共价键4、配位数:与中心离子(或原子)直接成键的离子(或原子)称为配位离子(原子)
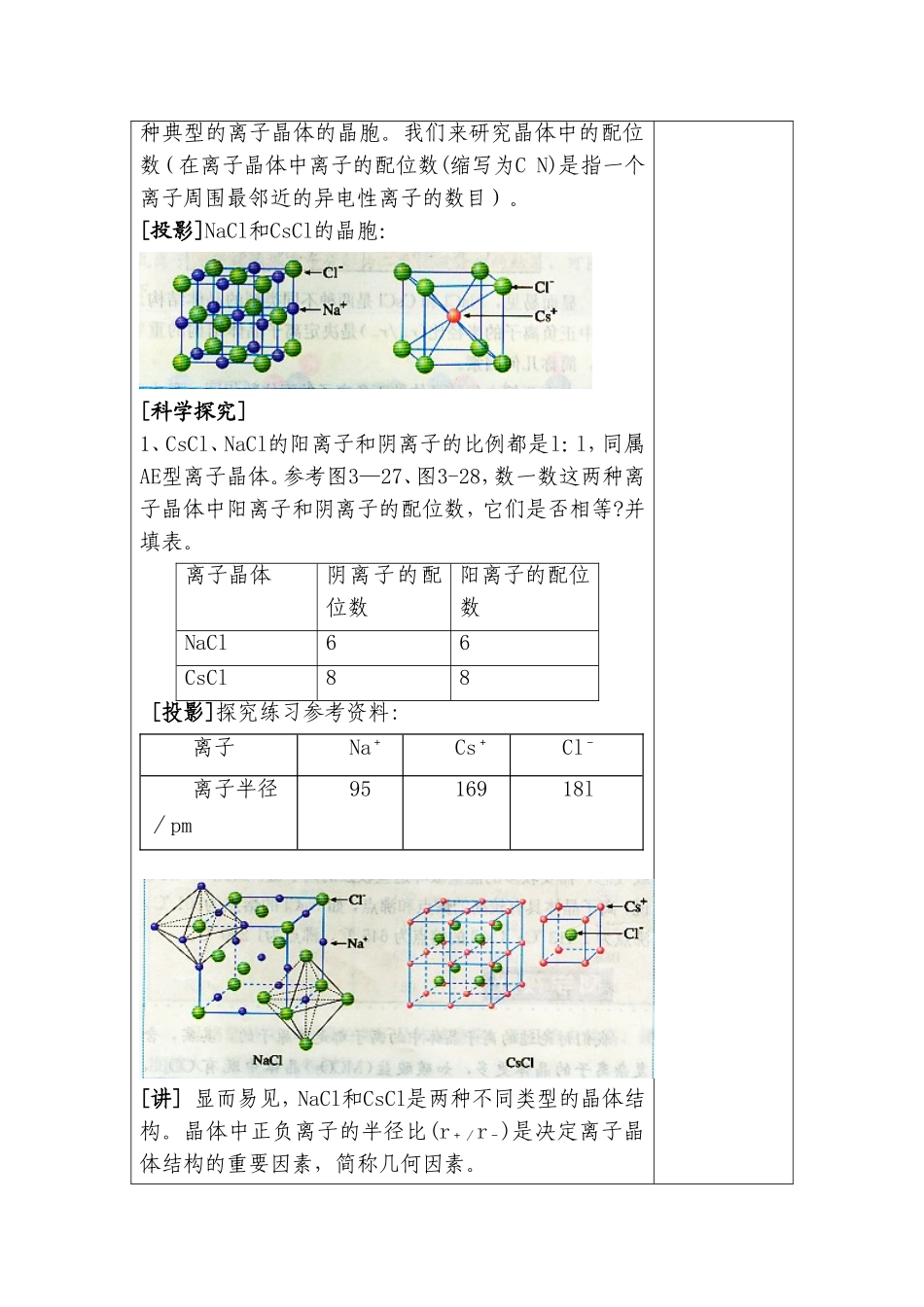
5、结构模型:(1)氯化钠晶体(2)氯化铯晶体6、影响因素:(1)几何因素:晶体中正负离子的半径比(r+/r-)
(2)电荷因素:正负离子的电荷比
(3)键性因素:离子键的纯粹程度
7、离子晶体特点:(1)较高的熔点和沸点,难挥发、难于压缩
(2)硬而脆(3)不导电,但熔化后或溶于水后能导电
(4)大多数离子晶体易溶于极性溶剂中,难溶于非极性溶剂中
教学过程教学步骤、内容[复习]分子晶体、原子晶体、金属晶体的有关理论
[过渡]在晶体中,若微粒为离子,通过离子键形成的晶体为离子晶体,今天我们来研究离子晶体
[板书]第四节离子晶体一、离子晶体1、定义:由阳离子和阴离子通过离子键结合而成的晶体
[讲]在离子晶体中,阴阳离子间只存在离子键
不存在分子,而化学式表示为晶体中阴阳离子个数的最简化
[板书]2、构成微粒:阴阳离子3、微粒间的作用:阴阳离子间以离子键结合,离子内可能有共价键[讲]离子晶体不一定含有金属阳离子,如NH4Cl为离子晶体,