第4讲难溶电解质的沉淀溶解平衡【2020·备考】最新考纲:1
理解难溶电解质的沉淀溶解平衡
能够运用溶度积(Ksp)进行简单计算
新课标要求:认识难溶电解质在水溶液中存在沉淀溶解平衡,了解沉淀的生成、溶解与转化
最新考情:沉淀溶解平衡是近几年的高考热点
考查的主要内容是沉淀的生成、溶解和转化、溶度积和浓度商的关系及应用
考查方式以选择题为主,一是考查Ksp的应用,2017年T12C、2016年T13B;二是以图像分析题的形式出现,如2018T13、2013年T14;三是在填空题中考查溶度积常数的计算以及沉淀溶解平衡在工业生产中的应用,如2015年T18(2)、2015年T20(4),预测2020年高考延续这一命题特点,应给予重点关注
考点一沉淀的溶解平衡及应用[知识梳理]1
沉淀溶解平衡(1)含义在一定温度下的水溶液中,当沉淀溶解和生成的速率相等时,即建立了溶解平衡状态
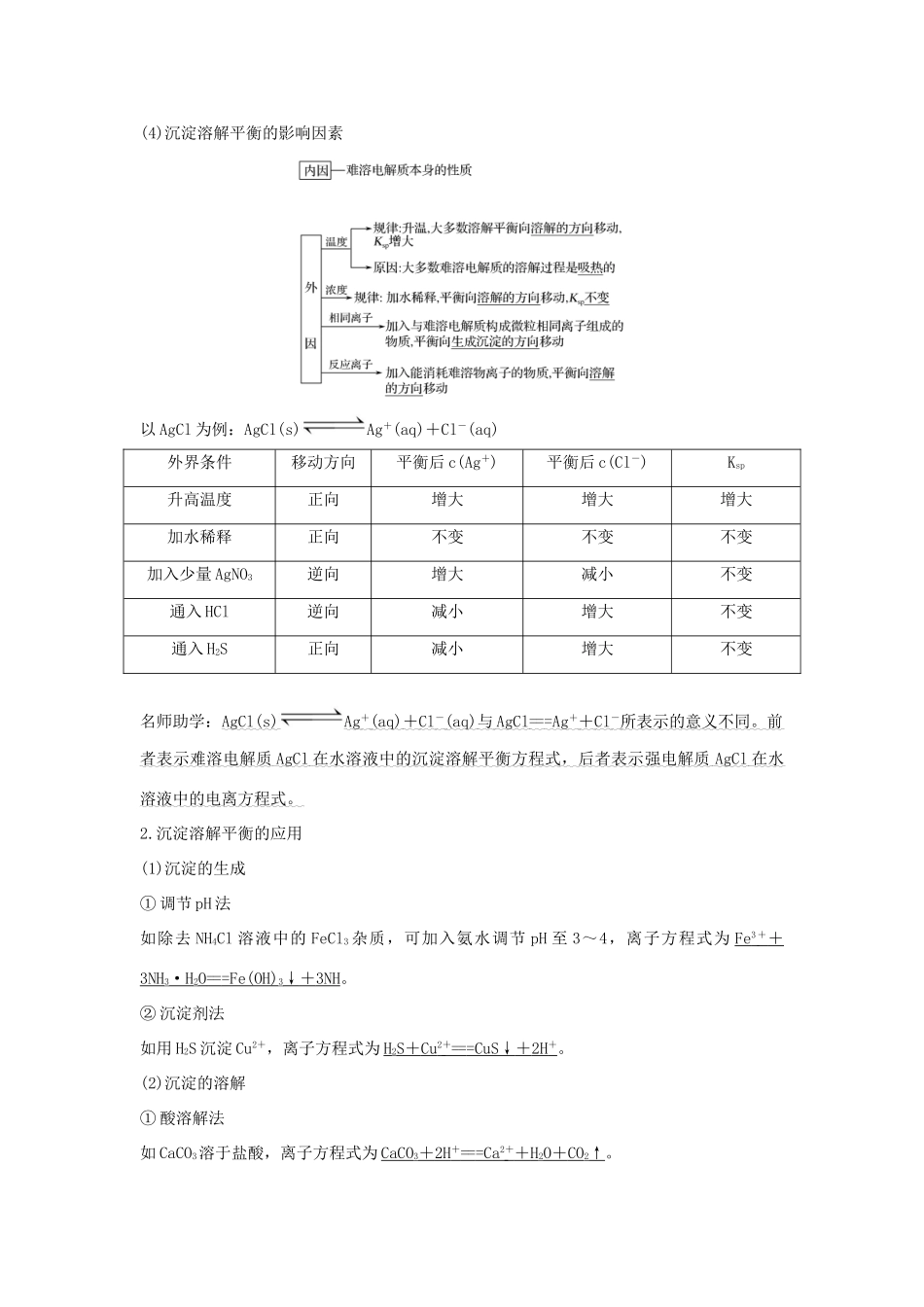
(2)建立过程固体溶质溶液中的溶质(3)特征(4)沉淀溶解平衡的影响因素以AgCl为例:AgCl(s)Ag+(aq)+Cl-(aq)外界条件移动方向平衡后c(Ag+)平衡后c(Cl-)Ksp升高温度正向增大增大增大加水稀释正向不变不变不变加入少量AgNO3逆向增大减小不变通入HCl逆向减小增大不变通入H2S正向减小增大不变名师助学:AgCl(s)Ag+(aq)+Cl-(aq)与AgCl===Ag++Cl-所表示的意义不同
前者表示难溶电解质AgCl在水溶液中的沉淀溶解平衡方程式,后者表示强电解质AgCl在水溶液中的电离方程式
沉淀溶解平衡的应用(1)沉淀的生成①调节pH法如除去NH4Cl溶液中的FeCl3杂质,可加入氨水调节pH至3~4,离子方程式为Fe3++3NH3·H2O===Fe(OH)3↓+3NH
②沉淀剂法如用H2S沉淀Cu2+,离子方程式为H2S+Cu2+===CuS↓+2H+