1原电池性质的系列实验探究郑理贺济琼潘震赵可嘉北京十二中高一(2)班指导教师:郑晓红首都师范大学附属丽泽中学摘要:利用数据采集器和传感器等仪器,测试了原电池中温度的变化、电压大小的变化,以及不同电池的使用寿命等,并对实验数据进行了分析和讨论
关键词:原电池传感器实验探究1问题的提出原电池是将化学能转化成电能的装置
根据我们近来所学原电池的相关内容,对原电池的相关性能进行了探究
当化学能转化为电能的过程中,温度的变化是否明显
化学能主要转化为电能还是热能
什么因素与原电池电压的大小有关
通过试验能定性总结出什么相关的规律
普通锌锰电池与碱性锌锰电池哪一种更耐用
购买时选择那种电池更实惠
⋯⋯为了弄清这些问题,我们利用数据采集器和传感器等仪器,通过以下几个实验进行了探究
2材料与仪器2
1药品、材料:1mol/LCuSO4溶液,1mol/LZnSO4溶液,1mol/LMgCl2溶液,1mol/LFeCl3溶液,1mol/LAgNO3溶液,饱和KNO3溶液,Cu片,Zn片,Mg粉,Mg条,Fe片,镀Ag铁片,1
5V、5号普通锌锰电池和碱性锌锰电池(三圈牌,福建厦门产)
2仪器:计算机,威尼尔牌(Vernier,美国)数据采集器以及电流、电压、2温度传感器;磁力搅拌器等
3实验方法与结果分析3
1化学反应、原电池反应中能量变化的测定3
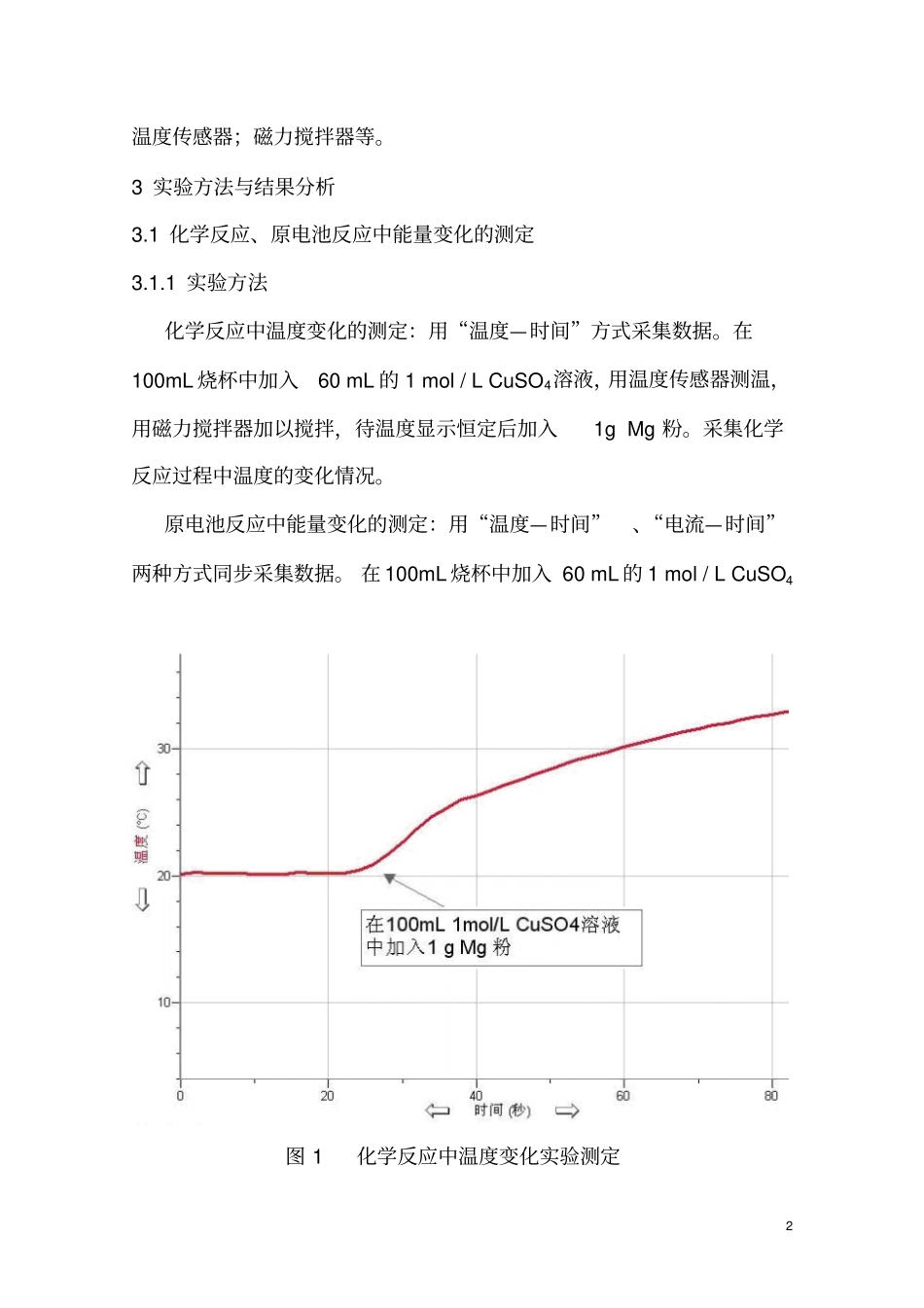
1实验方法化学反应中温度变化的测定:用“温度—时间”方式采集数据
在100mL烧杯中加入60mL的1mol/LCuSO4溶液,用温度传感器测温,用磁力搅拌器加以搅拌,待温度显示恒定后加入1gMg粉
采集化学反应过程中温度的变化情况
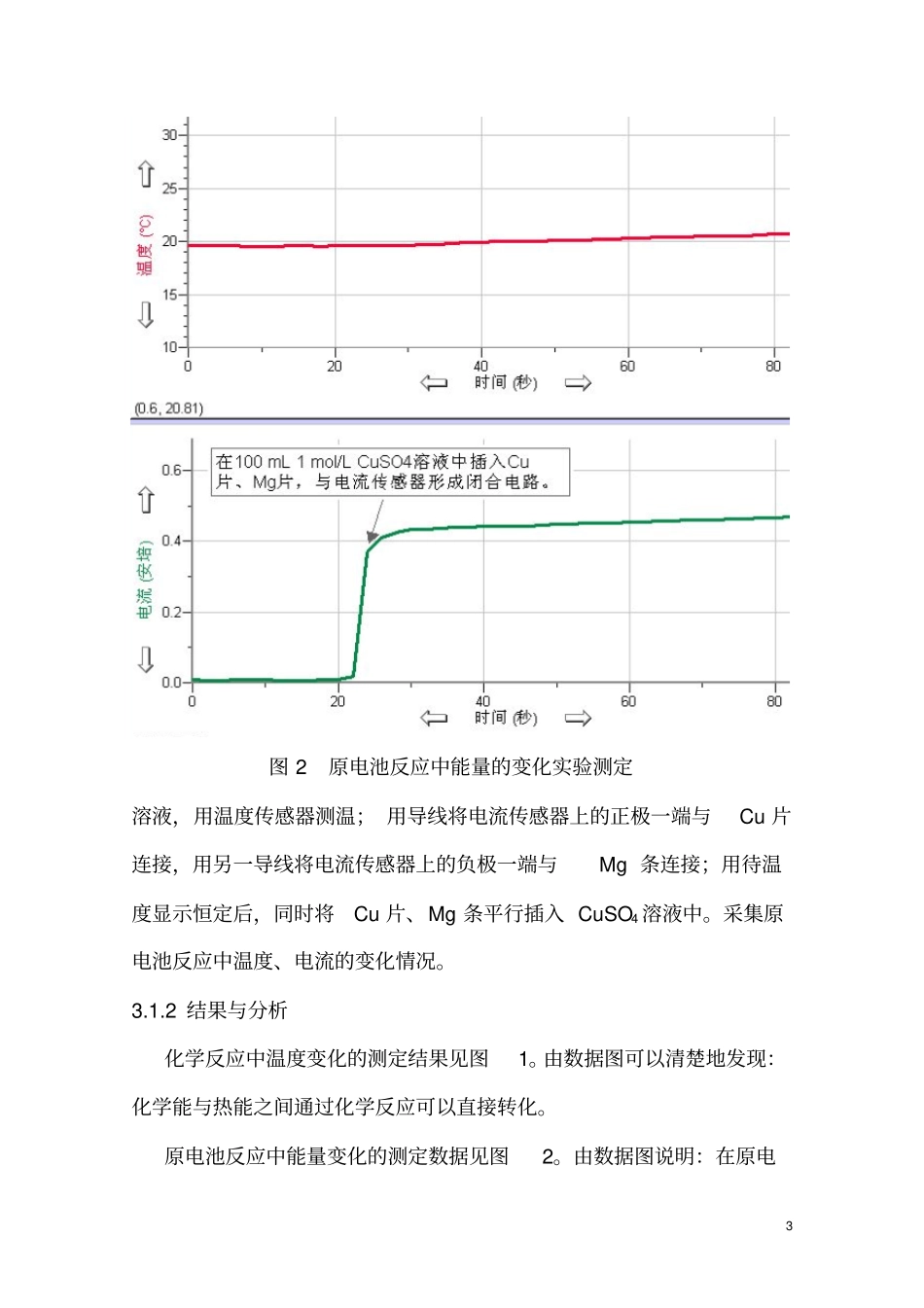
原电池反应中能量变化的测定:用“温度—时间”、“电流—时间”两种方式同步采集数据
在100mL烧杯中加入60mL的1mol/LCuSO4图1化学反应中温度变化实验测定3图2原电池反应中能量的变化实验测定溶液,用温