第二节几种重要的金属化合物(导学案)青春寄语:世上最重要的事,不在于我们在何处,而在于我们朝什么方向走
【学习目标】知识与技能:(1)了解几种铁的氧化物的性质和应用(2)掌握氢氧化亚铁、氢氧化铁的实验室制法,化学性质;(3)掌握Fe3+、Fe2+的检验方法,Fe3+的氧化性;Fe3+、Fe2+相互转化原理
过程与方法:(1)利用列表比较的方法,掌握铁的重要化合物的性质
(2)通过实验探究,了解对比试验方法
情感态度与价值观:通过实验探究,让学生体会科学研究的乐趣
在相互交流与评价中,养成团结合作的品质
【学习重点】氢氧化亚铁、氢氧化铁的化学性质;氢氧化亚铁的实验室制法Fe3+、Fe2+的检验方法;Fe3+、Fe2+相互转化原理【学习难点】Fe3+、Fe2+相互转化原理【知识链接】1
铁在地壳中的含量仅次于、和,位于第位,主要以和形式存在
在Fe2O3中铁的化合价是,FeO中铁的化合价是,Fe3O4中铁的化合价是
铁在空气中容易,因为不能保护内层金属
常见的还原剂有,常见的氧化剂有
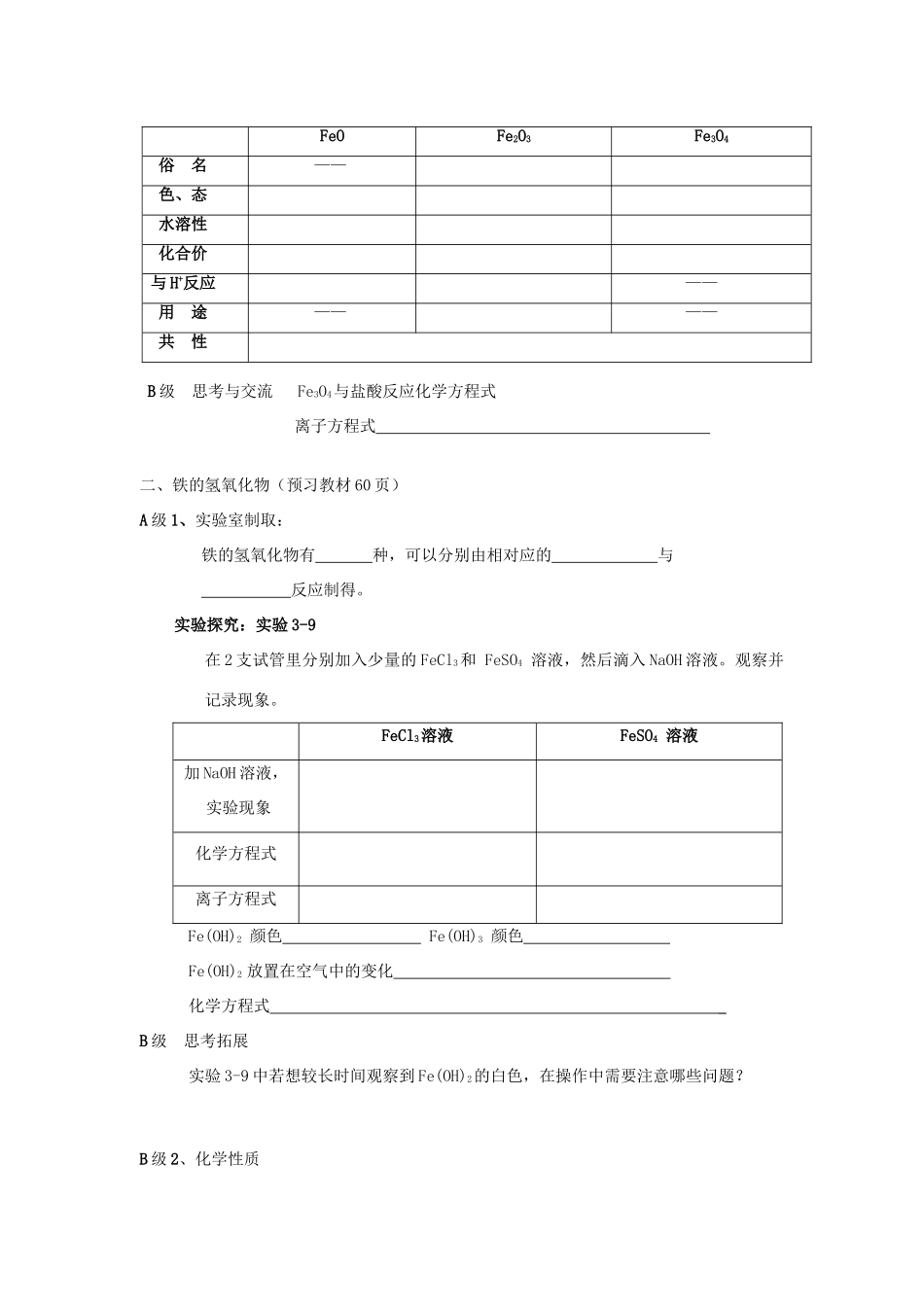
【探求新知】一、铁的几种氧化物(预习教材59页)A级知识梳理B级思考与交流Fe3O4与盐酸反应化学方程式离子方程式二、铁的氢氧化物(预习教材60页)A级1、实验室制取:铁的氢氧化物有种,可以分别由相对应的与反应制得
实验探究:实验3-9在2支试管里分别加入少量的FeCl3和FeSO4溶液,然后滴入NaOH溶液
观察并记录现象
FeCl3溶液FeSO4溶液加NaOH溶液,实验现象化学方程式离子方程式Fe(OH)2颜色Fe(OH)3颜色Fe(OH)2放置在空气中的变化化学方程式_B级思考拓展实验3-9中若想较长时间观察到Fe(OH)2的白色,在操作中需要注意哪些问题
B级2、化学性质FeOFe2O3Fe3O4俗名——色、态水溶性化合价与H+反应——用途————共性Fe(OH)2和Fe(OH)3