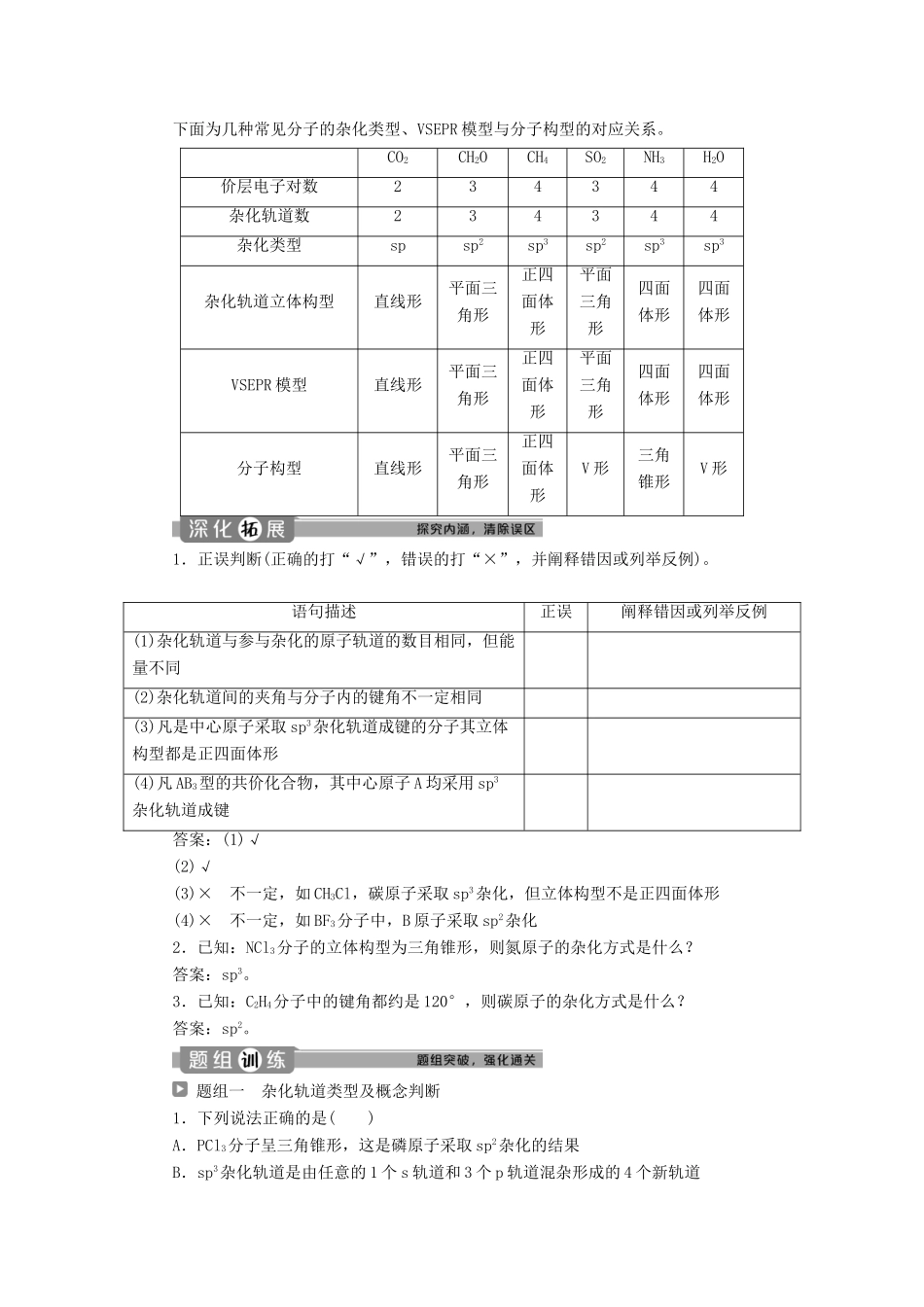
第2课时杂化轨道理论简介配合物理论简介1.了解杂化轨道理论及常见的杂化轨道类型(sp,sp2,sp3),并能根据杂化轨道理论判断简单分子或者离子的构型。2.能正确叙述配位键的概念及其形成条件,会分析配位化合物的形成及应用。3.熟知几种常见的配离子:[Cu(H2O)4]2+、[Cu(NH3)4]2+、[Fe(SCN)n](3-n)+、[Ag(NH3)2]+等的颜色及性质。杂化轨道理论简介1.轨道的杂化与杂化轨道(1)概念①轨道的杂化:原子内部能量相近的原子轨道重新组合形成与原轨道数相等的一组新轨道的过程。②杂化轨道:杂化后形成的新的能量相同的一组原子轨道。(2)杂化轨道类型杂化类型spsp2sp3参与杂化的原子轨道及数目1个s轨道和1个p轨道1个s轨道和2个p轨道1个s轨道和3个p轨道杂化轨道的数目234(3)杂化轨道的四点理解①在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道(ns,np)发生杂化,双原子分子中,不存在杂化过程。②杂化过程中,原子轨道总数不变,即杂化轨道的数目与参与杂化的原子轨道数目相等。③杂化过程中,轨道的形状发生变化,但杂化轨道的形状相同,能量相等。④杂化轨道只用于形成σ键或用来容纳未参与成键的孤电子对,且杂化轨道之间要满足最小排斥原理。2.杂化轨道类型与分子立体构型的关系杂化类型spsp2sp3杂化轨道间的夹角180°120°109°28′分子立体构型名称直线形平面三角形正四面体形实例CO2、C2H2BF3、HCHOCH4、CCl4当杂化轨道中有未参与成键的孤电子对时,由于孤电子对参与互相排斥,会使分子的构型与杂化轨道的形状有所区别。如水分子中氧原子的sp3杂化轨道有2个是由孤电子对占据的,其分子不呈正四面体构型,而呈V形,氨分子中氮原子的sp3杂化轨道有1个由孤电子对占据,氨分子不呈正四面体构型,而呈三角锥形。3.杂化轨道的立体构型与微粒的立体构型下面为几种常见分子的杂化类型、VSEPR模型与分子构型的对应关系。CO2CH2OCH4SO2NH3H2O价层电子对数234344杂化轨道数234344杂化类型spsp2sp3sp2sp3sp3杂化轨道立体构型直线形平面三角形正四面体形平面三角形四面体形四面体形VSEPR模型直线形平面三角形正四面体形平面三角形四面体形四面体形分子构型直线形平面三角形正四面体形V形三角锥形V形1.正误判断(正确的打“√”,错误的打“×”,并阐释错因或列举反例)。语句描述正误阐释错因或列举反例(1)杂化轨道与参与杂化的原子轨道的数目相同,但能量不同(2)杂化轨道间的夹角与分子内的键角不一定相同(3)凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体形(4)凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键答案:(1)√(2)√(3)×不一定,如CH3Cl,碳原子采取sp3杂化,但立体构型不是正四面体形(4)×不一定,如BF3分子中,B原子采取sp2杂化2.已知:NCl3分子的立体构型为三角锥形,则氮原子的杂化方式是什么?答案:sp3。3.已知:C2H4分子中的键角都约是120°,则碳原子的杂化方式是什么?答案:sp2。题组一杂化轨道类型及概念判断1.下列说法正确的是()A.PCl3分子呈三角锥形,这是磷原子采取sp2杂化的结果B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混杂形成的4个新轨道C.中心原子采取sp3杂化的分子,其立体构型可能是四面体形或三角锥形或V形D.AB3型分子的立体构型必为平面三角形解析:选C。PCl3分子的中心原子磷的价层电子对数=σ键电子对数+孤电子对数=3+=4,因此PCl3分子中磷原子采取sp3杂化,A项错误。sp3杂化轨道是原子最外电子层上的s轨道和3个p轨道混杂形成的4个新轨道,B项错误。一般采取sp3杂化的分子,其立体构型呈四面体形,但如果有杂化轨道被中心原子上的孤电子对占据,则分子的立体构型会发生变化,如NH3、PCl3分子呈三角锥形,H2O分子呈V形,C项正确,D项错误。2.(2019·瓦房店高级中学高二期中)有关杂化轨道的说法不正确的是()A.杂化前后的轨道数目不变,但轨道的形状发生了改变B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°C.四面体形、三角锥形、V形分子的结构都可以用sp3杂化轨道解释D.杂化轨道全部参与形成化学键解析:选D。杂化轨道用于形成σ键或容纳未参与成键的孤电子对。题组二杂...