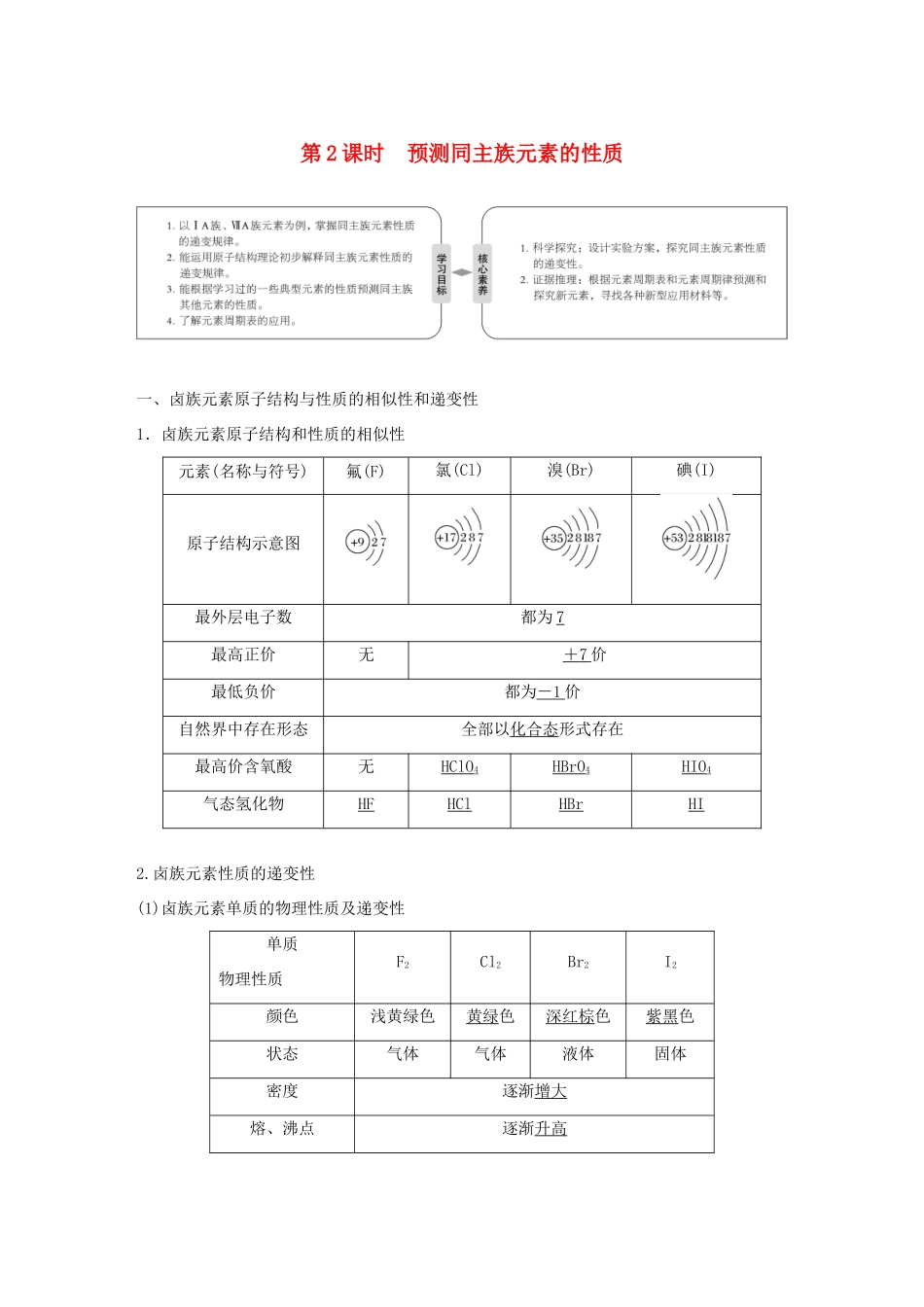
第2课时预测同主族元素的性质一、卤族元素原子结构与性质的相似性和递变性1.卤族元素原子结构和性质的相似性元素(名称与符号)氟(F)氯(Cl)溴(Br)碘(I)原子结构示意图最外层电子数都为7最高正价无+7价最低负价都为-1价自然界中存在形态全部以化合态形式存在最高价含氧酸无HClO4HBrO4HIO4气态氢化物HFHClHBrHI2
卤族元素性质的递变性(1)卤族元素单质的物理性质及递变性单质物理性质F2Cl2Br2I2颜色浅黄绿色黄绿色深红棕色紫黑色状态气体气体液体固体密度逐渐增大熔、沸点逐渐升高(2)结构及化学性质的递变性结构及化学性质规律原子半径――――――――→单质的氧化性――――――→阴离子的还原性―――――――→与H2化合的难易程度―――――――→氢化物的稳定性―――――――→最高价氧化物对应水化物的酸性―――――――→(1)卤素性质的相似性卤素原子都能得一个电子;单质都能与氢气发生化合反应;除F外,最高价氧化物对应的水化物的化学式为HXO4(X代表卤素原子),且为强酸
(2)卤素性质的递变性从F到I,随核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,得电子能力逐渐减弱,元素非金属性逐渐减弱
例1(2017·枣庄高一检测)关于卤素X(依次为Cl、Br、I)的下列叙述不正确的是()A.卤素单质与水反应均可用X2+H2O===HXO+HX表示B.HX都极易溶于水,它们的热稳定性随核电荷数增加而增强C.卤素单质的颜色按相对分子质量增大而加深D.相对分子质量小的卤素单质可将相对分子质量大的卤素从它的卤化物溶液里置换出来考点卤素的性质题点卤素性质的变化规律答案B解析HX的热稳定性随核电荷数的增加而减弱
特别提示——卤素的特性(1)氟元素无正价,无含氧酸,而氯、溴、碘元素有最高正价和含氧酸
(2)X2+H2O===HX+HXO(X代表C