第二课时铁的重要化合物学习目标:1
了解铁的氧化物的性质及应用
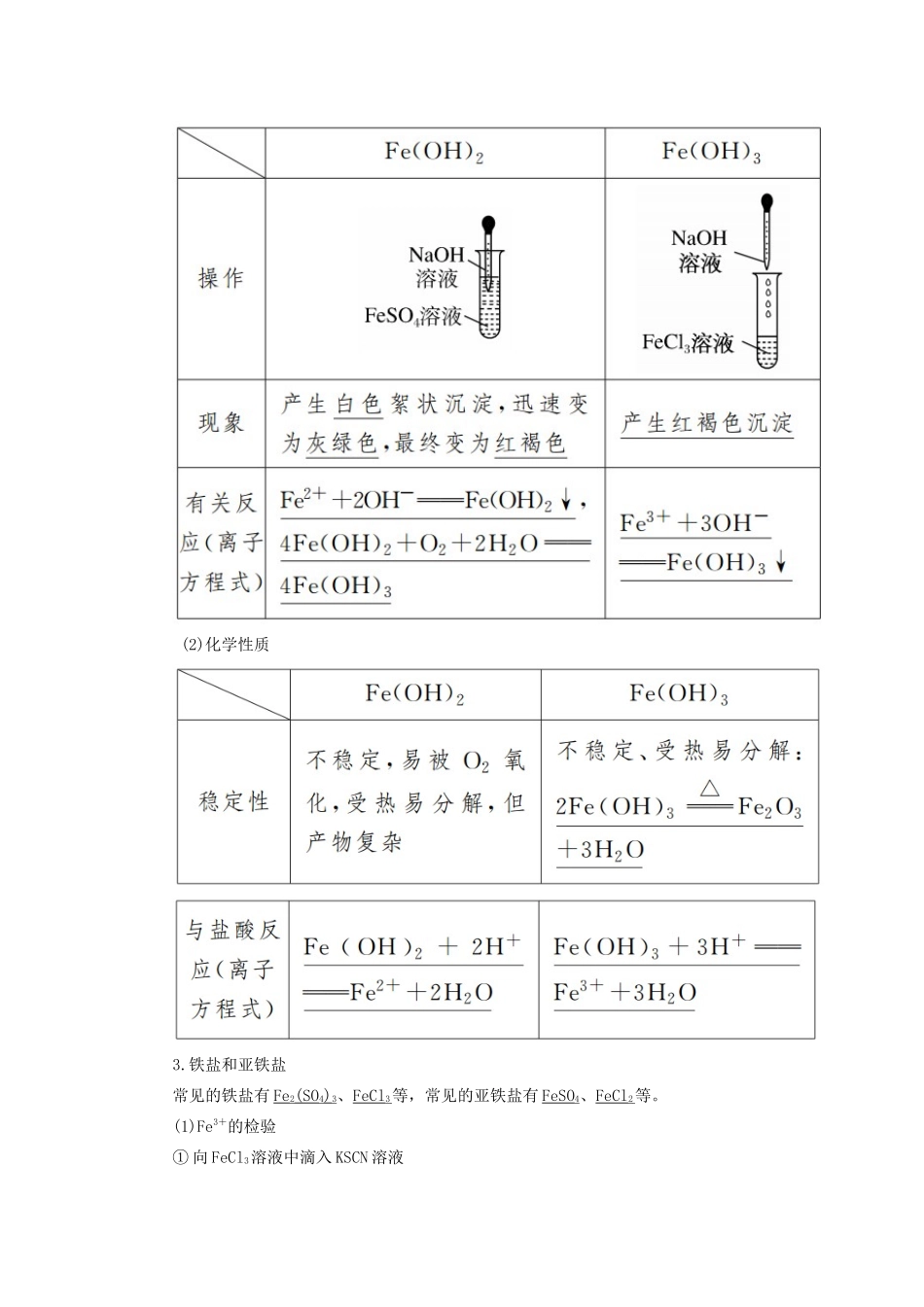
了解Fe(OH)2、Fe(OH)3的制备原理及化学性质
掌握Fe2+、Fe3+间的相互转化以及Fe3+、Fe2+的检验方法
1.铁的氧化物(1)物理性质(2)化学性质①氧化亚铁不稳定,在空气中受热易被氧化为Fe3O4
②氧化亚铁和氧化铁属于碱性氧化物,与非强氧化性酸反应生成Fe2+和Fe3+
③写出氧化亚铁和氧化铁分别与盐酸反应的离子方程式:a.氧化亚铁:FeO+2H+===Fe2++H2O
b.氧化铁:Fe2O3+6H+===2Fe3++3H2O
(3)主要用途氧化铁俗称铁红,常用作红色油漆和涂料
2.铁的氢氧化物(1)铁的氢氧化物的制备(2)化学性质3
铁盐和亚铁盐常见的铁盐有Fe2(SO4)3、FeCl3等,常见的亚铁盐有FeSO4、FeCl2等
(1)Fe3+的检验①向FeCl3溶液中滴入KSCN溶液现象:溶液显血红色;化学反应方程式:FeCl3+3KSCN===Fe(SCN)3+3KCl
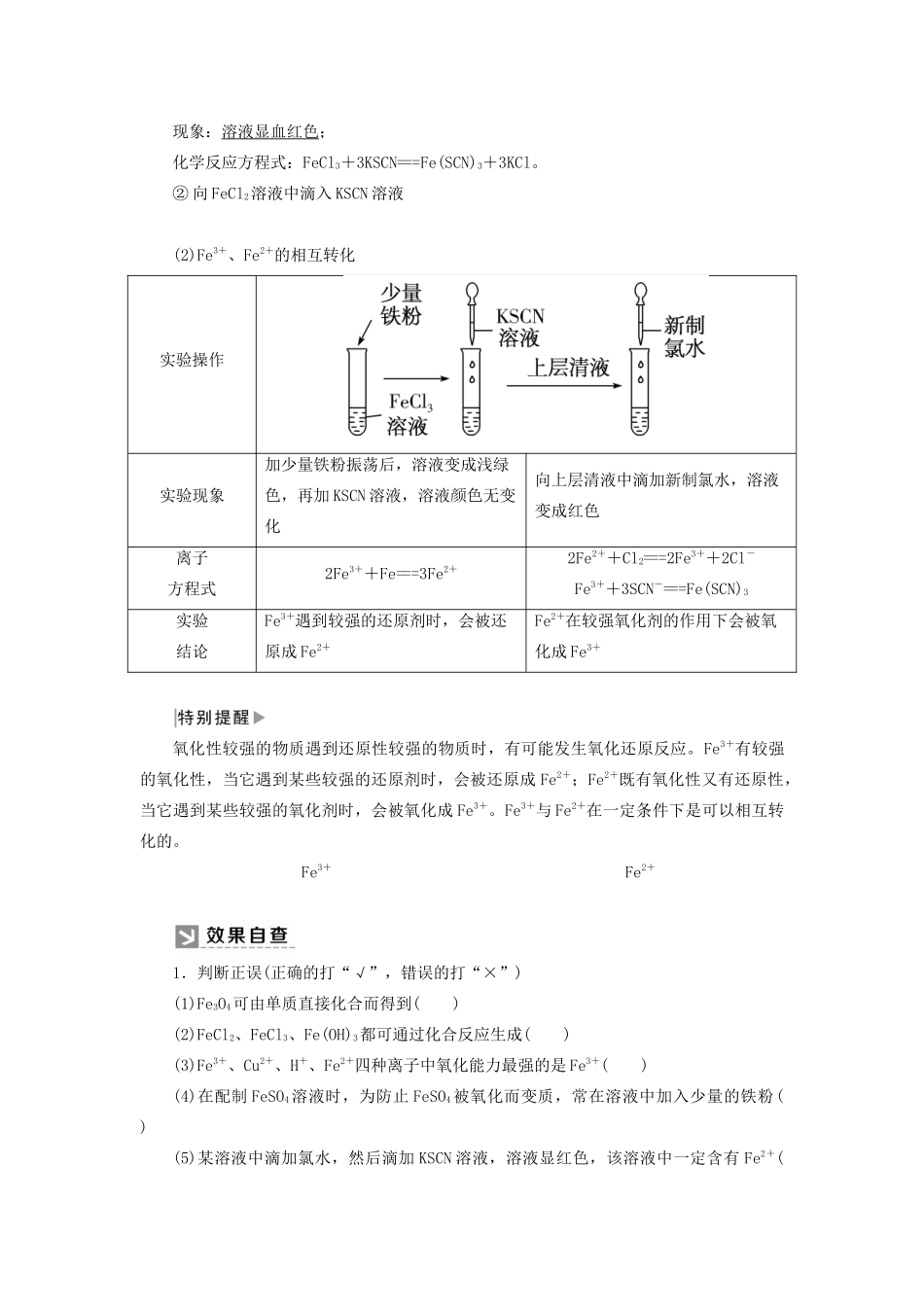
②向FeCl2溶液中滴入KSCN溶液(2)Fe3+、Fe2+的相互转化实验操作实验现象加少量铁粉振荡后,溶液变成浅绿色,再加KSCN溶液,溶液颜色无变化向上层清液中滴加新制氯水,溶液变成红色离子方程式2Fe3++Fe===3Fe2+2Fe2++Cl2===2Fe3++2Cl-Fe3++3SCN-===Fe(SCN)3实验结论Fe3+遇到较强的还原剂时,会被还原成Fe2+Fe2+在较强氧化剂的作用下会被氧化成Fe3+氧化性较强的物质遇到还原性较强的物质时,有可能发生氧化还原反应
Fe3+有较强的氧化性,当它遇到某些较强的还原剂时,会被还原成Fe2+;Fe2+既有氧化性又有还原性,当它遇到某些较强的氧化剂时,会被氧化成Fe3+
Fe3+与Fe2+在一定条件下是可以相互转化的
Fe3+