第三节生活中两种常见的有机物【学习目标】1.认识乙醇在日常生活中的存在,体会乙醇的重要作用
2.掌握乙醇的主要性质,通过对乙醇性质的探究,体会化学探究的一般思路与方法
3.了解官能团的概念,能利用乙醇性质推测乙醇结构,感受物质结构与性质之间的辩证关系
【重点难点】乙醇的化学性质【活动方案】活动一:根据生活常识,归纳总结乙醇的物理性质工业酒精约含乙醇96%以上(质量分数)无水酒精99
5%以上(质量分数)医用酒精75%(体积分数)饮用酒视度数而定体积分数
俗称气味状态密度(与水相比)挥发性溶解性(在水中)思考:两种不同的液体互溶在一起时,可用什么方法分离
如何检验酒精中是否含有水
如何用工业酒精制得无水乙醇
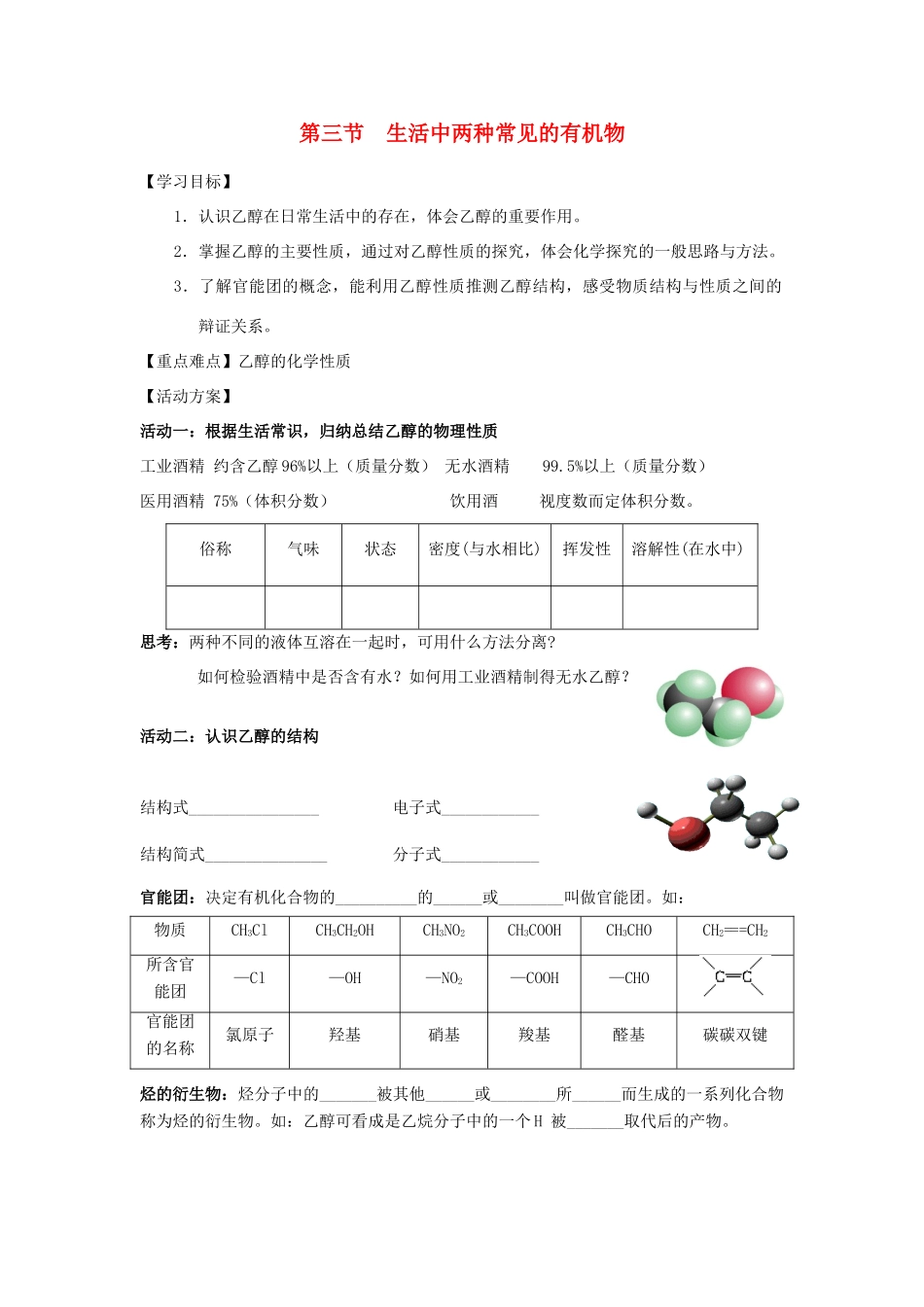
活动二:认识乙醇的结构结构式________________电子式____________结构简式_______________分子式____________官能团:决定有机化合物的__________的______或________叫做官能团
如:物质CH3ClCH3CH2OHCH3NO2CH3COOHCH3CHOCH2===CH2所含官能团—Cl—OH—NO2—COOH—CHO官能团的名称氯原子羟基硝基羧基醛基碳碳双键烃的衍生物:烃分子中的_______被其他______或________所______而生成的一系列化合物称为烃的衍生物
如:乙醇可看成是乙烷分子中的一个H被_______取代后的产物
活动三:实验探究乙醇的化学性质1.乙醇的氧化反应(1)[问题提出]乙醇能否在体外被氧化
实验现象:________________________________________________________________反应原理:________________________________________________________________(2)[问