第二单元元素性质的递变规律第1课时原子核外电子排布的周期性1
周期表中原子结构和位置、价态、元素种数等之间的关系
能把握周期表中各区、周期、族元素的原子核外电子排布的规律
周期表中各区、周期、族元素的原子结构和位置间的关系
(重难点)主族元素的原子核外电子排布与性质的周期性[基础·初探](1)ⅦA族的外围电子排布式为ns2np5
()(2)O的最外层电子数为6,故最高正价为+6价
()(3)原子外围电子排布式为ns2的元素一定在ⅡA族
()(4)同周期的含氧酸从左到右的酸性逐渐增强
()【答案】(1)√(2)×(3)×(4)×[题组·冲关]题组主族元素的核外电子排布和元素性质1
第三周期元素R,它的原子最外电子层上达到饱和所需电子数小于次外层和最内层电子数之差,但等于最内层电子数的正整数倍
下列说法正确的是()A
常温下,能稳定存在的R的氧化物都能与烧碱溶液反应B
R的最高价氧化物对应的水化物都是强酸C
R的外围电子层上未成对电子数不同D
在常温下,R的气态氢化物都能在空气中稳定存在【解析】依题意推导知:R可能是Si或S;然后逐项分析,应知:硅酸是弱酸、硫酸是强酸;Si和S的外围电子层上未成对电子都是2个;SiH4不稳定;而SO2、SiO2都是酸性氧化物,都可以与烧碱反应,所以只有A项正确
【答案】A2
短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于ⅠA族,W与X属于同一主族,下列说法正确的是()A
元素X、W的简单阴离子具有相同的电子层结构B
由Y、Z两种元素组成的化合物是离子化合物C
W的简单气态氢化物的热稳定性比Y的强D
原子半径:r(X)r(F),D错误
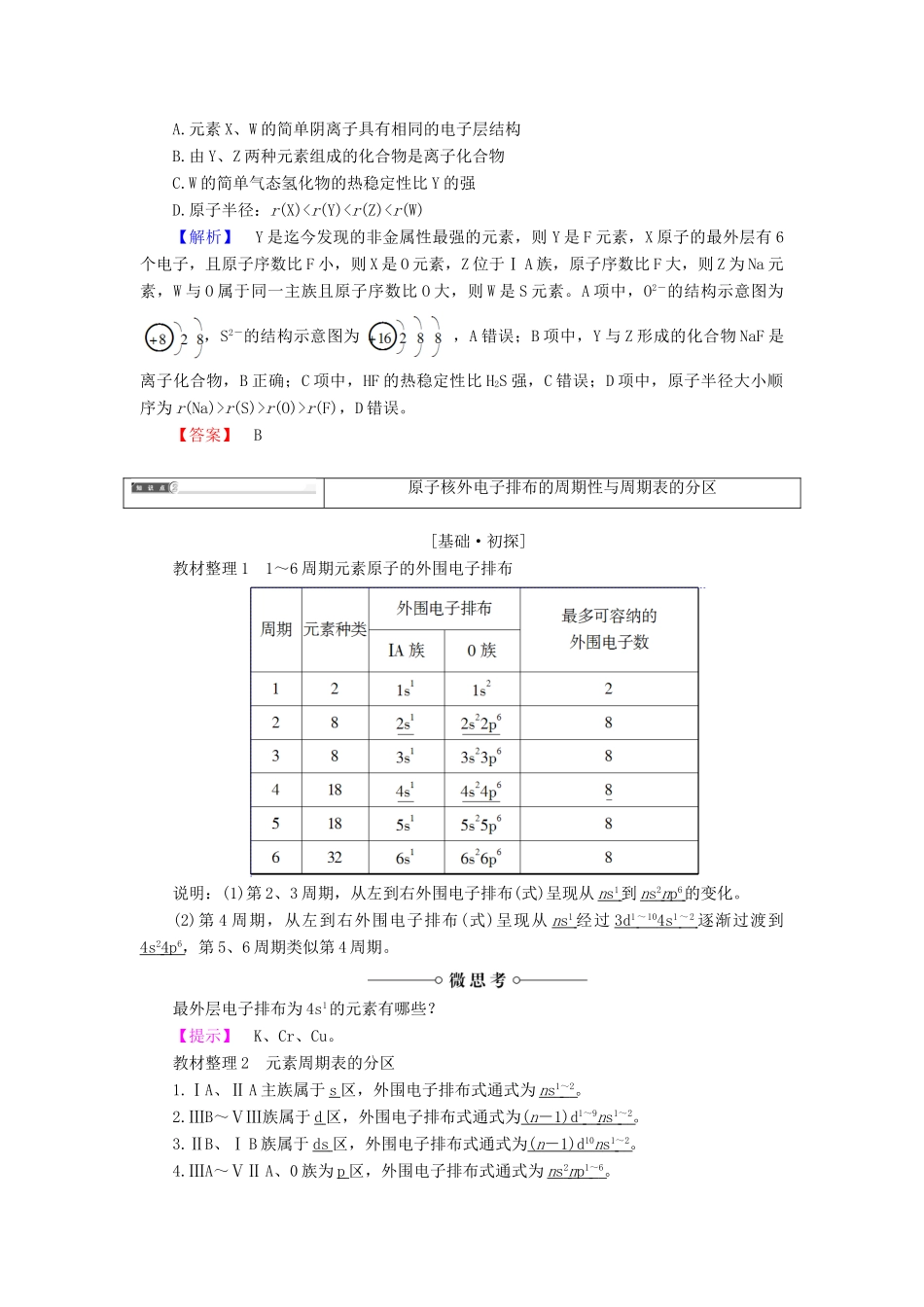
【答案】B原子核外电子排布的周期性与周期表的分区[基础·初探]教材整理11~6周期元素原子的外围电子排布说明:(1