第四部分元素及其化合物专题十七几种重要的金属——铁铜一.铁小结1:(1)铁与氧化剂反应生成Fe3+,如等物质
(2)铁与氧化剂反应生成Fe2+,如等物质
(3)铁与等反应生成四氧化三铁
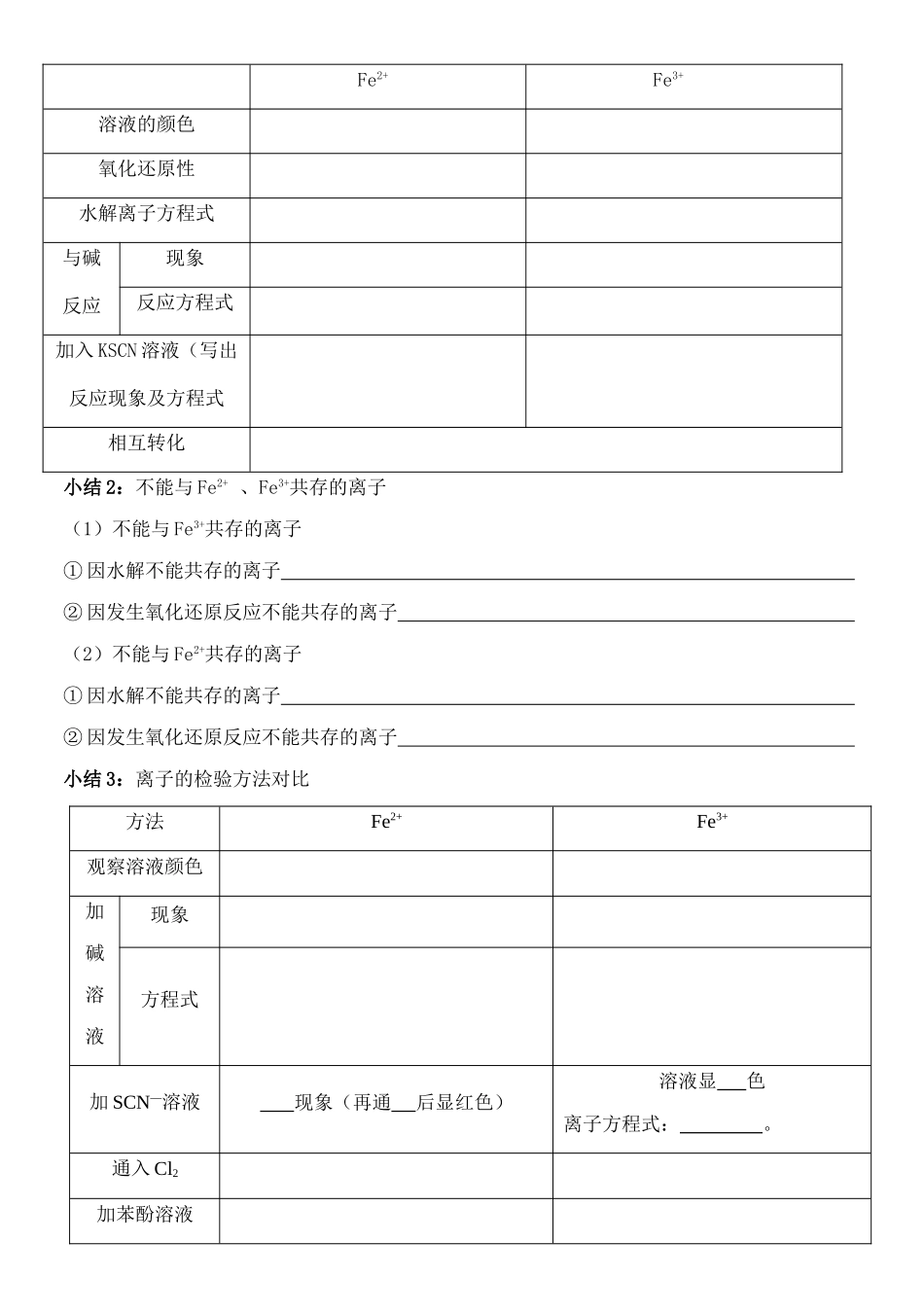
二、Fe2+、Fe3+的比较名称内容项目铁——最重要的过渡元素原子结构在周期表中位置物理性质化学性质与非金属反应O2Cl2S、I2与水反应与酸反应与非氧化性酸与氧化性酸与浓硫酸Fe少量Fe过量与浓硝酸Fe少量Fe过量与盐反应冶炼方法用途Fe2+Fe3+溶液的颜色氧化还原性水解离子方程式与碱反应现象反应方程式加入KSCN溶液(写出反应现象及方程式相互转化小结2:不能与Fe2+、Fe3+共存的离子(1)不能与Fe3+共存的离子①因水解不能共存的离子②因发生氧化还原反应不能共存的离子(2)不能与Fe2+共存的离子①因水解不能共存的离子②因发生氧化还原反应不能共存的离子小结3:离子的检验方法对比方法Fe2+Fe3+观察溶液颜色加碱溶液现象方程式加SCN—溶液现象(再通后显红色)溶液显色离子方程式:
通入Cl2加苯酚溶液小结4:Fe2+溶液的保存方法是;Fe3+溶液的配制方法是
三.铁的化合物和亚铁化合物的相互转变(1
)从以上6各方面选取代表性物质书写方程式(每个方面至少写两个):1
小结5:常见铁的化合物的颜色状态物质FeFeOFe2O3Fe3O4Fe(OH)2Fe(OH)3Fe2+Fe3+Fe(SCN)2+颜色状态四.铁的氧化物和氢氧化物1.铁的氧化物的比较铁的氧化物FeOFe2O3Fe3O4俗称色、态铁的价态水溶性FeFe2+Fe3+稳定性不稳定性6FeO+O2=2Fe3O4稳定稳定与酸反应离子方程式与还原性酸反应(HI)与氧化性酸反应(HNO3)与CO(H2、Al、C等)的反应FexOy+CO=Fe+CO2制取高温熔融,过量的铁与氧