第三章第一节金属的性质教学目的1:1
巩固学习钠、铝等金属及其重要化合物的主要性质,强化训练
教学课时:2
5课时知识体系11.钠及其重要化合物的性质(B)⑴位置和原子结构示意图:第3周期第ⅠA族
⑵钠的物理性质:银白色、有金属光泽的固体;密度小,ρ(Na)=0
97g/cm3,比水的密度小;熔点和沸点低,熔点97
81℃,沸点882
9℃;硬度小,可以用小刀切割;是热和电的良导体
⑶钠的化学性质:①钠与水的反应:2Na+2H2O==2NaOH+H2↑钠与水反应的实验改进装置:②钠与氧气的反应:钠在空气中缓慢氧化:4Na+O2==2Na2O(白色固体)钠在空气中加热或点燃:2Na+O2Na2O2(淡黄色固体)⑷钠的保存及用途①钠的保存:钠很容易跟空气中的氧气和水起反应,因此,在实验室中,通常将钠保存在煤油里,由于ρ(Na)>ρ(煤油),钠沉在煤油下面,将钠与氧气和水隔绝
②钠的用途:钠钾合金(室温下呈液态),用作原子反应堆的导热剂
制备Na2O2
作为强还原剂制备某些稀有金属
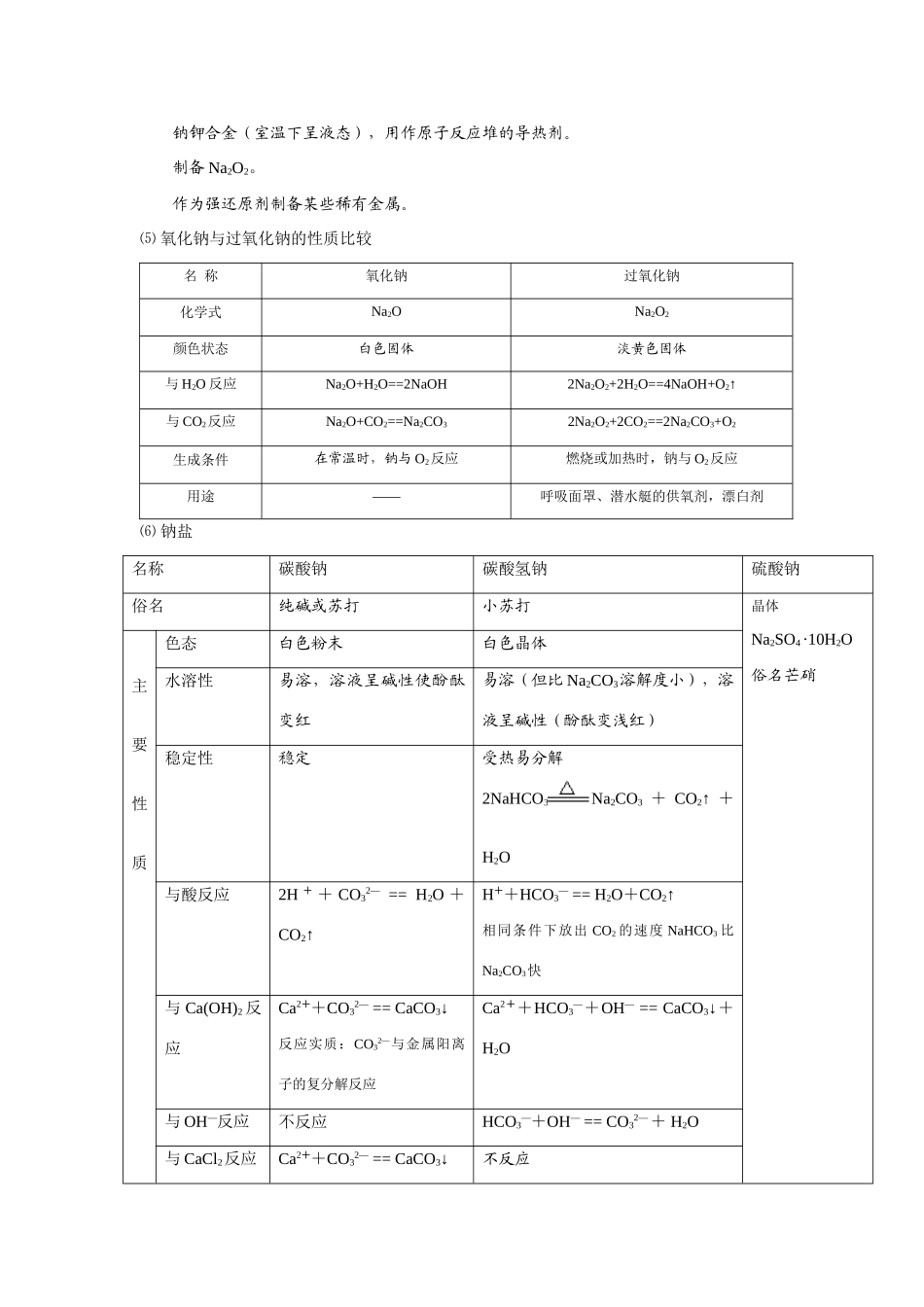
⑸氧化钠与过氧化钠的性质比较名称氧化钠过氧化钠化学式Na2ONa2O2颜色状态白色固体淡黄色固体与H2O反应Na2O+H2O==2NaOH2Na2O2+2H2O==4NaOH+O2↑与CO2反应Na2O+CO2==Na2CO32Na2O2+2CO2==2Na2CO3+O2生成条件在常温时,钠与O2反应燃烧或加热时,钠与O2反应用途——呼吸面罩、潜水艇的供氧剂,漂白剂⑹钠盐名称碳酸钠碳酸氢钠硫酸钠俗名纯碱或苏打小苏打晶体Na2SO4·10H2O俗名芒硝主要性质色态白色粉末白色晶体水溶性易溶,溶液呈碱性使酚酞变红易溶(但比Na2CO3溶解度小),溶液呈碱性(酚酞变浅红)稳定性稳定受热易分解2NaHCO3Na2CO3+CO2↑+H2O与酸反应2H++CO32—==H2O+CO2↑H++HCO3—==H2O+