第2节氮的循环知识·巧学·升华一、氮在自然界中的循环1.氮元素的存在:游离态和化合态
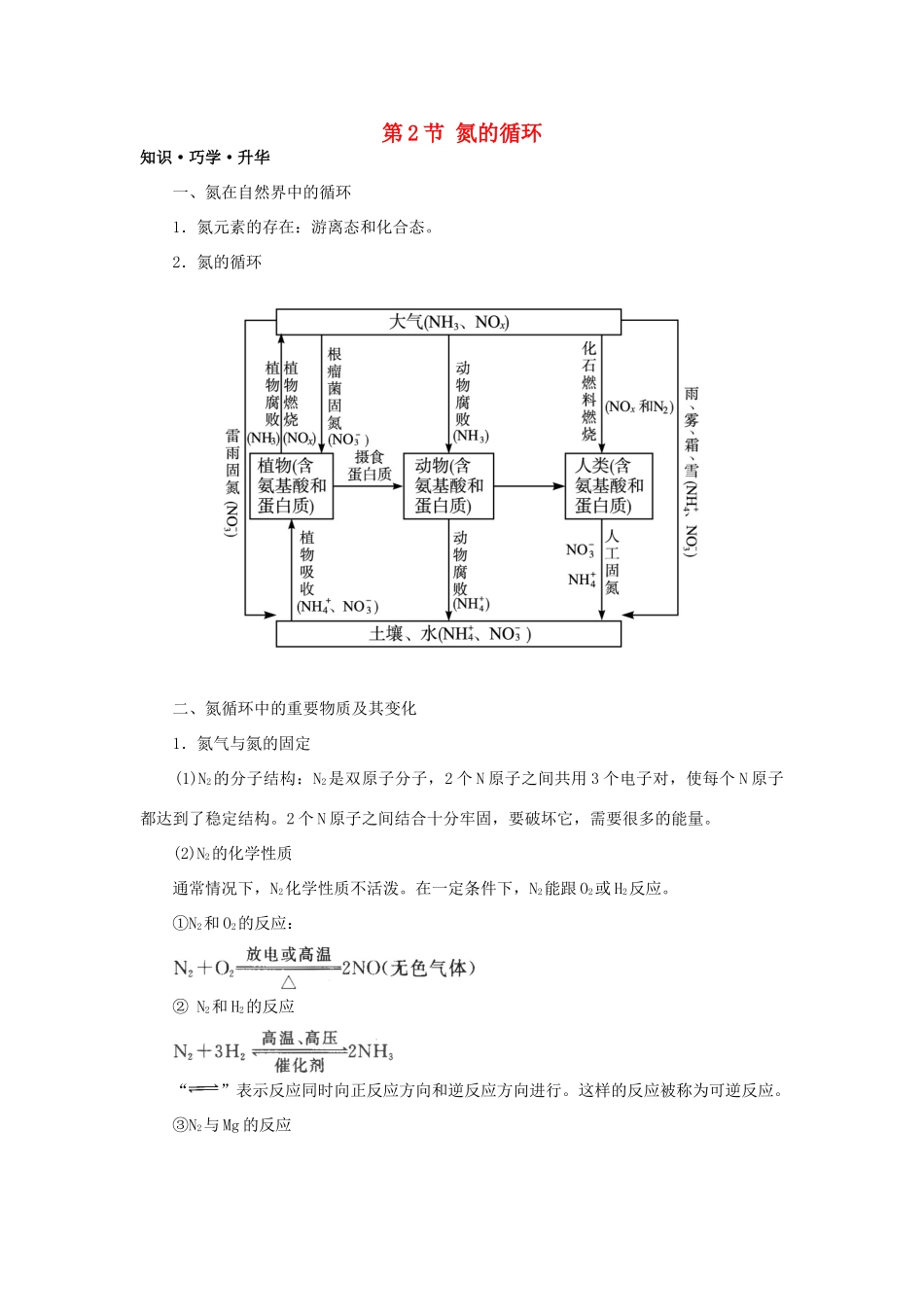
2.氮的循环二、氮循环中的重要物质及其变化1.氮气与氮的固定(1)N2的分子结构:N2是双原子分子,2个N原子之间共用3个电子对,使每个N原子都达到了稳定结构
2个N原子之间结合十分牢固,要破坏它,需要很多的能量
(2)N2的化学性质通常情况下,N2化学性质不活泼
在一定条件下,N2能跟O2或H2反应
①N2和O2的反应:②N2和H2的反应“”表示反应同时向正反应方向和逆反应方向进行
这样的反应被称为可逆反应
③N2与Mg的反应3Mg+N2Mg3N2(3)植物对氮的吸收和氮的固定①通常植物只吸收和②氮的固定:使空气中游离态的氮转化为可利用的含氮化合物的过程叫做氮的固定
游离态氮化合态氮,是氮的固定
如:N2NH3,N2NO等
固氮2.氮的氧化物(1)NO的两面性①NO是大气污染物:是造成光学烟雾的主要气体之一;NO还能与血红蛋白结合,使血红蛋白失去运O2能力
②NO是人体内的信使分子:NO在人体血管系统内具有传送信号的功能,NO能让体内某部位的信号传送到另一部位,人体离不开少量的NO
(2)NO的合成反应N2+O22NO大多数化合反应是放热反应,但该反应却是吸热反应
(3)NO的氧化反应常温下,NO很容易被空气中的O2氧化为NO22NO+O2══2NO2(无色)(红棕色)(4)NO2的性质①物理性质:NO2是红棕色易溶于水的有毒气体,有刺激性气味
②NO2溶于水的反应该反应也是歧化反应,NO2既是氧化剂,又是还原剂
③NO2的自身聚合反应2(红棕色)(无色)(5)NOx+O2+H2O的反应①2NO+O22NO2②3NO2+H2O══2HNO3+NO①+②×2,消去NO得:4NO2+O2+2H2O══4HNO3①×③+②×2,消去NO2得4NO+3O2+2H2O══4HNO3(6)