第2课时预测同主族元素的性质1.以ⅠA族、ⅦA族元素为例,掌握同主族元素性质的递变规律
(重点)2.能运用原子结构理论初步解释同主族元素性质的递变规律
3.掌握由同主族元素的性质特点预测不熟悉元素的性质
(难点)4.了解元素周期表的应用
同主族元素的性质[基础·初探]1.卤族元素原子结构和性质的相似性和递变性(1)相似性最高化合价0均为+7最低化合价均为-1气态氢化物HFHClHBrHI最高价氧化物的水化物无HClO4(强酸)HBrO4(强酸)HIO4(强酸)(2)单质的物理性质及递变性单质物理性质F2Cl2Br2I2颜色浅黄绿色黄绿色深红棕色紫黑色状态气体气体液体固体密度逐渐增大熔、沸点逐渐升高(3)结构及化学性质的递变性结构及性质规律原子半径――→单质的氧化性――→阴离子的还原性――→与H2化合的难易程度――→氢化物的稳定性――→最高价氧化物对应水化物的酸性――→2
碱金属元素原子结构和性质的相似性与递变性(1)相似性①原子的最外电子层都有1个电子
②最高化合价均为+1价
③都是活泼的金属元素,单质都能与氧气、水等物质发生反应
④最高价氧化物对应的水化物一般具有很强的碱性
(2)递变性结构及性质规律原子半径――→单质的还原性――→与水、氧气反应的剧烈程度――→最高价氧化物对应水化物的碱性――→3
同主族元素性质的递变规律[探究·升华][思考探究]1.Li、Na、K在空气中燃烧分别生成Li2O、Na2O2、KO2(超氧化钾)说明什么问题
如何保存钾单质
【提示】说明Li、Na、K活动性依次增强;保存钾时应保存在煤油中,以避免与空气中的O2、H2O反应
2.利用原子结构如何解释F、Cl、Br、I得失电子能力的变化
【提示】F、Cl、Br、I最外层都有7个电子,都易得一个电子达到稳定结构,但原子半径依次增大,得电子能力逐渐减弱
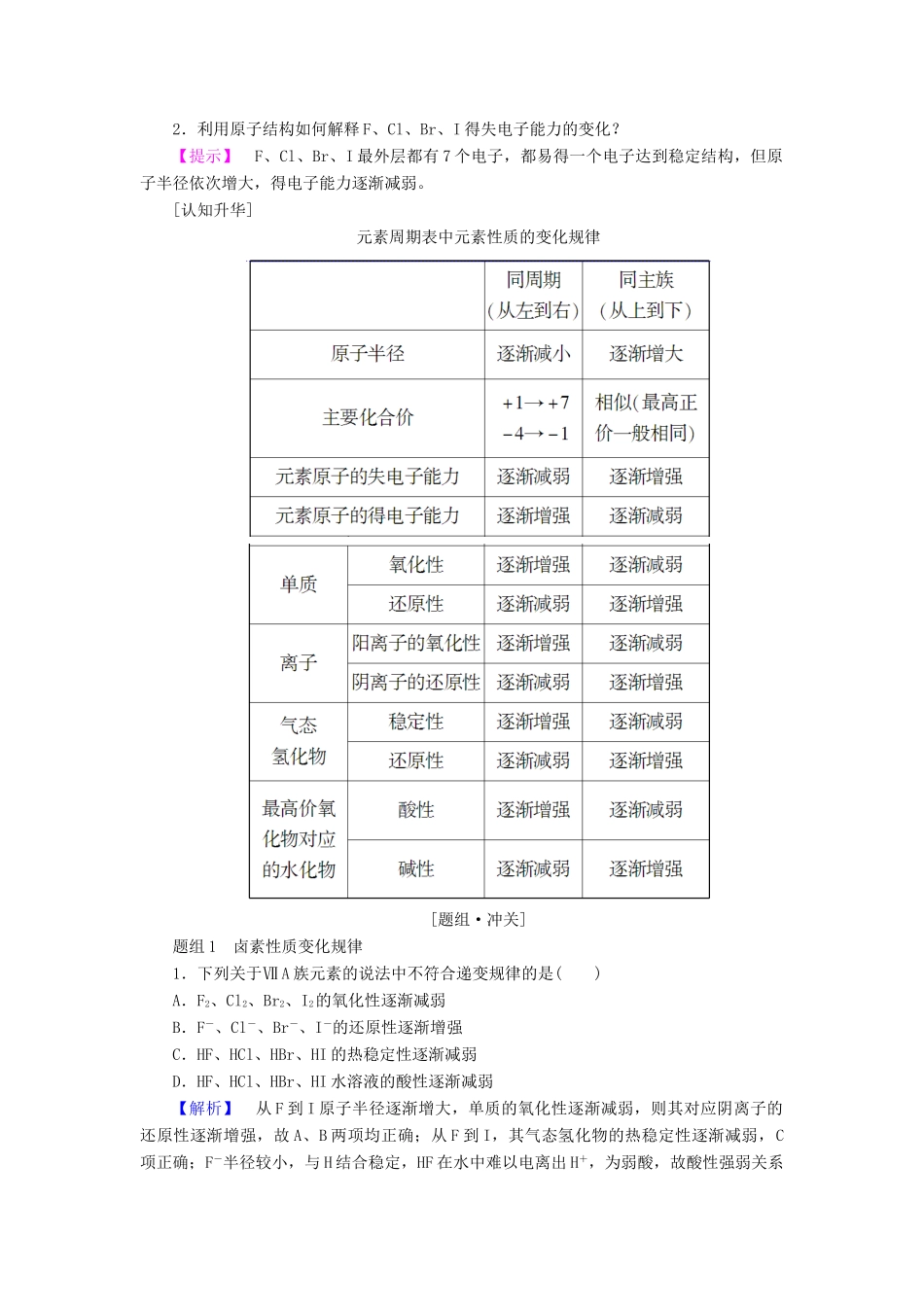
[认知升华]元素周期表中元素性质的变化规律[题组