溶液的配制及分析【学习目标】1、初步学会配制一定物质的量浓度溶液的实验技能
2、通过一定物质的量浓度的溶液的配制,了解溶液的定量分析方法
【重点难点】重点:一定物质的量浓度溶液的配制与分析难点:配制一定物质的量浓度的溶液误差分析【导学流程】一、基础感知1、读取量筒中液体体积时,仰视读数结果会,俯视读数结果会(填“偏高”“偏低”或“无影响”)2、正误判断:(1)配制0
1mol·L-1的H2SO4溶液时,将量取的浓硫酸倒入容量瓶中加水稀释后定容(2)需要240mL1mol·L-1NaOH溶液时,配制前称量NaOH固体的质量为10
0g(3)配制溶液时,若加水超过容量瓶刻度线,应用胶头滴管将多余溶液吸出(4)配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高(5)配制0
100mol·L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流(6)用固体NaCl配制0
5mol·L-1溶液,必要仪器有:烧杯、玻璃棒、胶头滴管、容量瓶(7)可以在50mL量筒中配制50mL0
1000mol·L-1碳酸钠溶液(8)用量筒量取20mL0
50mol·L-1H2SO4溶液于烧杯中,再加入80mL的水,可配制成0
10mol·L-1H2SO4溶液二、探究未知1、配制一定物质的量浓度溶液的主要仪器(1)托盘天平:称量前先,称量时“”,读数精确到g
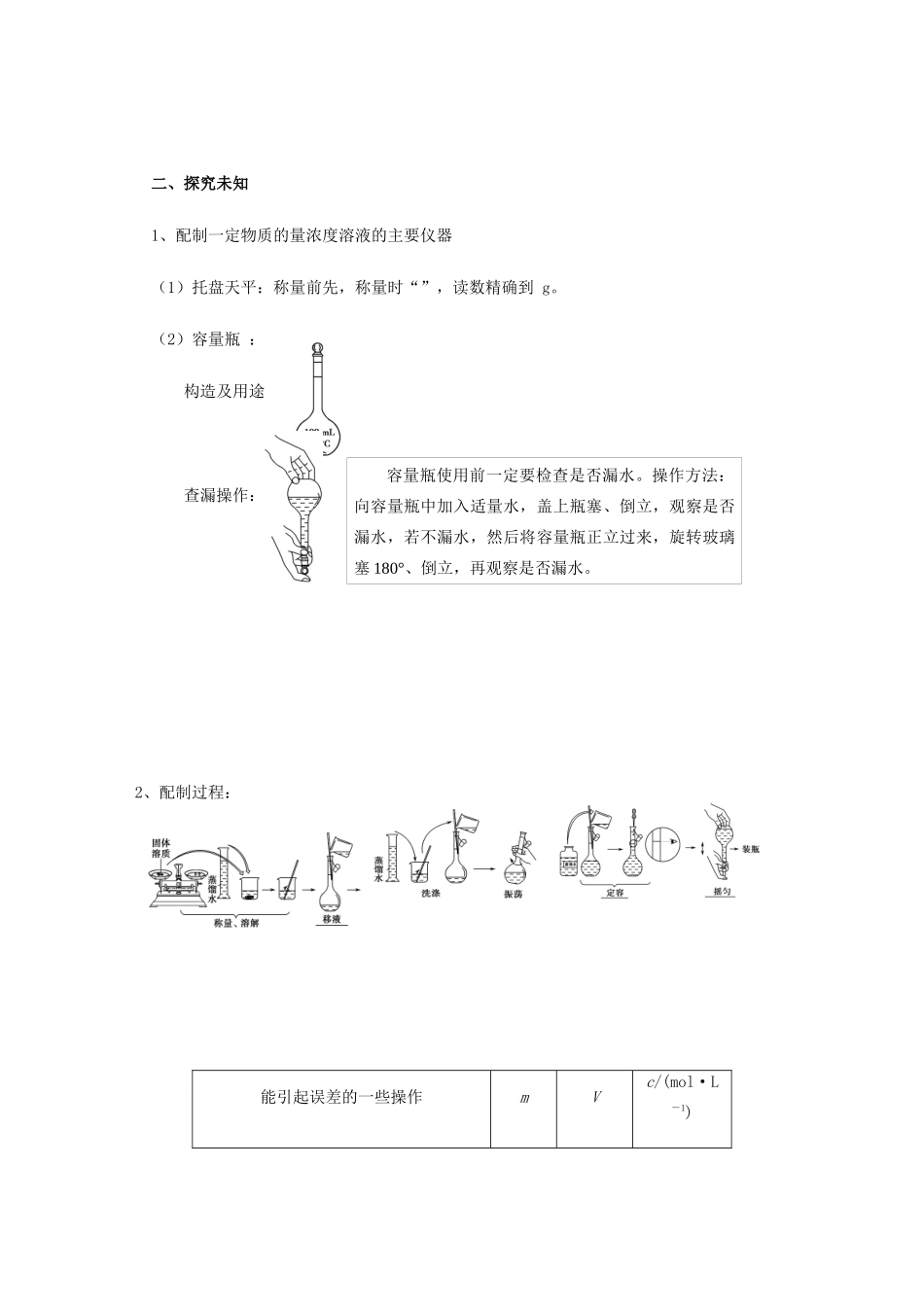
(2)容量瓶:构造及用途查漏操作:2、配制过程:容量瓶使用前一定要检查是否漏水
操作方法:向容量瓶中加入适量水,盖上瓶塞、倒立,观察是否漏水,若不漏水,然后将容量瓶正立过来,旋转玻璃塞180°、倒立,再观察是否漏水
能引起误差的一些操作mVc/(mol·L-1)3、误差分析:以配制NaOH溶液为例三、典型例题【典例1】下列不是容量瓶的瓶身上的标记的是:A.容积B.温度C.物质的量浓度D.刻度线【典例2】用质量分数为98%的浓硫酸(密度为1
84g·cm-