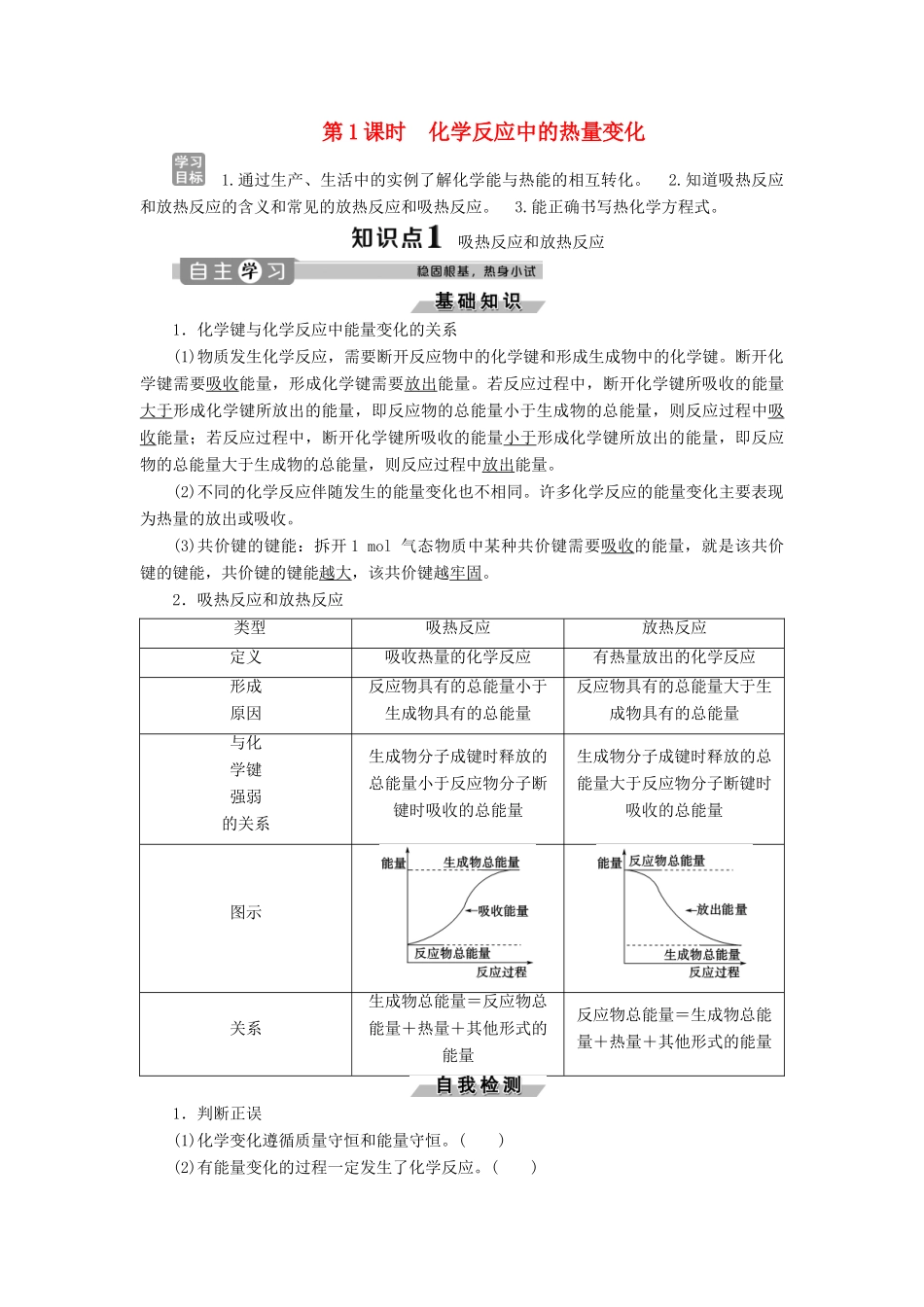
第1课时化学反应中的热量变化1.通过生产、生活中的实例了解化学能与热能的相互转化。2.知道吸热反应和放热反应的含义和常见的放热反应和吸热反应。3.能正确书写热化学方程式。吸热反应和放热反应1.化学键与化学反应中能量变化的关系(1)物质发生化学反应,需要断开反应物中的化学键和形成生成物中的化学键。断开化学键需要吸收能量,形成化学键需要放出能量。若反应过程中,断开化学键所吸收的能量大于形成化学键所放出的能量,即反应物的总能量小于生成物的总能量,则反应过程中吸收能量;若反应过程中,断开化学键所吸收的能量小于形成化学键所放出的能量,即反应物的总能量大于生成物的总能量,则反应过程中放出能量。(2)不同的化学反应伴随发生的能量变化也不相同。许多化学反应的能量变化主要表现为热量的放出或吸收。(3)共价键的键能:拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能,共价键的键能越大,该共价键越牢固。2.吸热反应和放热反应类型吸热反应放热反应定义吸收热量的化学反应有热量放出的化学反应形成原因反应物具有的总能量小于生成物具有的总能量反应物具有的总能量大于生成物具有的总能量与化学键强弱的关系生成物分子成键时释放的总能量小于反应物分子断键时吸收的总能量生成物分子成键时释放的总能量大于反应物分子断键时吸收的总能量图示关系生成物总能量=反应物总能量+热量+其他形式的能量反应物总能量=生成物总能量+热量+其他形式的能量1.判断正误(1)化学变化遵循质量守恒和能量守恒。()(2)有能量变化的过程一定发生了化学反应。()(3)化学反应中化学能只能转变为热能。()(4)需要点燃或加热才能发生的反应一定是吸热反应。()(5)电解水的过程是电能转化为热能。()(6)通过反应物和生成物的键能可以计算出一个化学反应是吸热反应还是放热反应。()答案:(1)√(2)×(3)×(4)×(5)×(6)√2.下列反应属于吸热反应的是()A.铝与CuCl2溶液反应B.NaOH和HCl反应C.NaOH与NH4Cl的反应D.甲烷燃烧解析:选C。需要识记常见的放热反应和吸热反应。3.下列过程一定释放出能量的是()A.两个氢原子结合成一个氢分子B.分解反应C.氮分子拆成两个氮原子D.化合反应答案:A4.在催化剂和加热条件下,SO2与O2化合为SO3并放出热量,同时SO3也分解为SO2和O2,化学方程式如下:2SO2(g)+O2(g)((((((2SO3(g)下列对该反应的叙述中错误的是()A.2molSO2(g)和1molO2(g)的总能量一定高于2molSO3(g)的总能量B.SO3分解为SO2和O2的同时吸收热量C.电子转移、化学键变化和能量转化同步进行D.加热是该反应发生能量变化的主要原因解析:选D。化学反应发生能量变化的原因是反应物总能量不等于生成物总能量,而加热是使化学反应发生的一种外部条件。一、吸热反应和放热反应的比较吸热反应放热反应能量变化反应物的总能量小于生成物的总能量反应物的总能量大于生成物的总能量键能变化生成物的总键能小于反应物的总键能生成物的总键能大于反应物的总键能常见实例①大部分分解反应;②以碳、CO、H2为还原剂的氧化还原反应;③Ba(OH)2·8H2O和①金属和水或酸的反应;②金属氧化物和水或酸的反应;③可燃物的燃烧反应及缓慢氧NH4Cl反应;④盐的水解反应化;④酸和碱的中和反应;⑤铝热反应;⑥大部分化合反应NaOH固体溶于水、浓H2SO4溶于水等属于放热过程,不属于放热反应;NH4NO3固体溶于水、升华、蒸发、分子形成原子等属于吸热过程,不属于吸热反应。二、化学键与化学反应中能量变化的关系当E1>E2,反应吸收能量;当E1