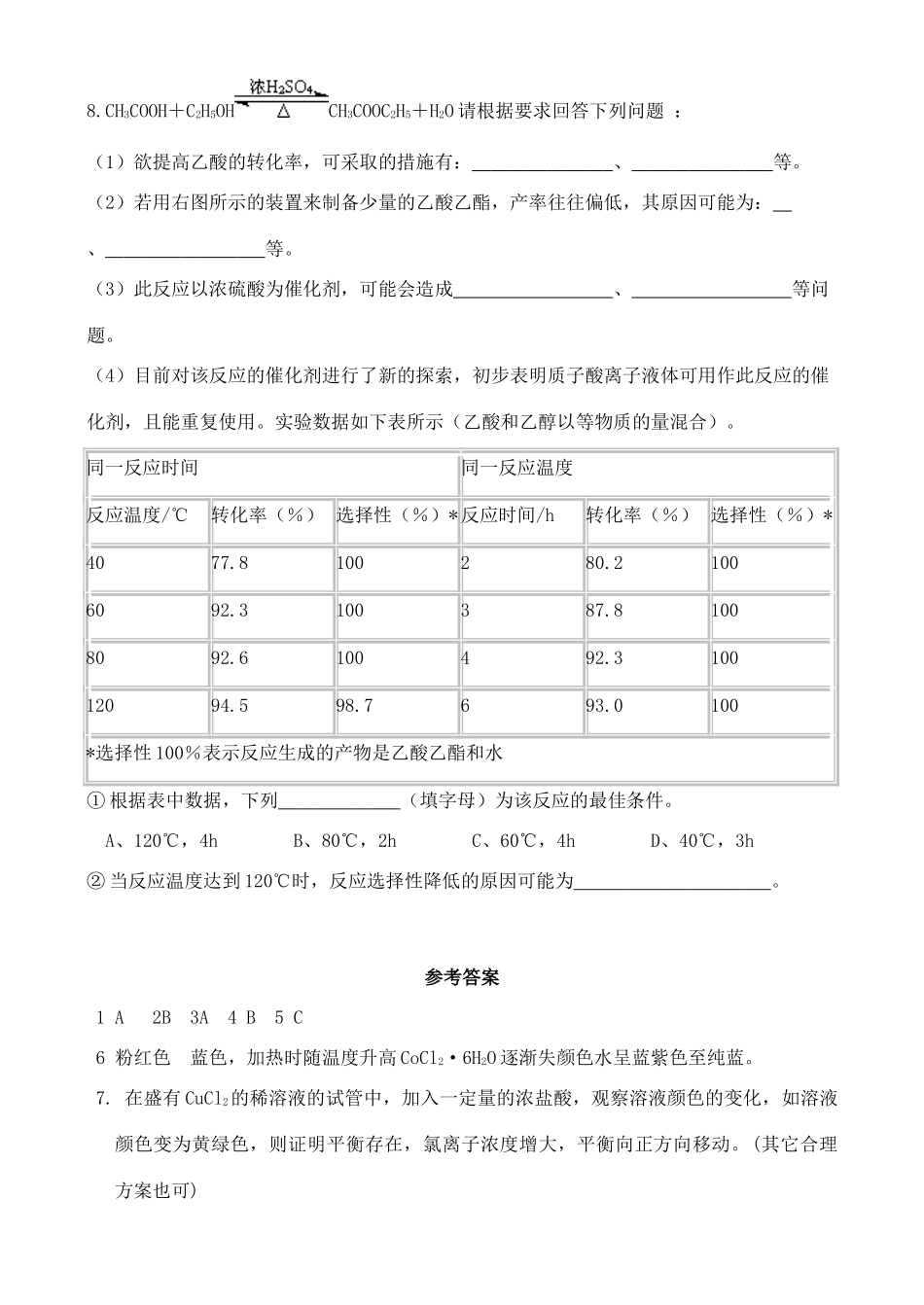
反应条件对化学平衡的影响学习目标:1.巩固平衡移动原理的应用。2.了解反应条件对化学平衡的影响。情感目标:通过反应条件对化学平衡的影响的学习,培养细致,认真的科学态度。学习重点难点:平衡移动原理的应用;反应条件对化学平衡的影响。学习过程:实验1:氯化钴溶液颜色的变化(1)观察稀释酸性CoCl2溶液时颜色的变化实验步骤:向3mL0.5mol·L-1CoCl2溶液中慢慢滴加约6mL浓盐酸,观察现象将上述试管中的溶液分成两份,向其中一溶液中加入约3mL蒸馏水,与另一溶液作对比,观察现象。[CoCl4]2-+6H2O[Co(H2O)6]2++4Cl-蓝色粉红色实验现象现象分析CoCl2+浓盐酸加入3mL蒸馏水(2)观察受热时CoCl2溶液颜色的变化实验步骤:取一支试管,加入3mL95%乙醇溶液和少量(2-3小粒)氯化钴晶体,振荡使其溶解,再滴滴加蒸馏水,至溶液恰好呈粉红色,然后用酒精灯加热该试管片刻。观察上述实验过程中溶液颜色的变化。加乙醇溶解后溶液呈蓝色,稀释时,溶液由蓝色→紫色→很快变成粉红色(平衡向左移动);加热时,又由粉红色→紫色→蓝色(平衡向右移动)。实验改进:实验时间:25分钟练习:1.已知:C(s)+CO2(g)2CO(g)△H>0。该反应的达到平衡后,下列条件有利于反应向正方向进行的是()A、升高温度和减小压强B、降低温度和减小压强C、降低温度和增大压强D、升高温度和增大压强2.下列说法正确的是()A、可逆反应的特征是正反应速率和逆反应速率相等B、在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态C、在其他条件不变时,升高温度可以使平衡向放热反应方向移动D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态3.下列事实不能用勒沙特列原理解释的是()A.钢铁在潮湿的空气中容易生锈B.将FeCl3溶液加热蒸干最终得不到FeCl3固体C.实验室可用排饱和食盐水的方法收集氯气D.常温下,将1mLpH=3的醋酸溶液加水稀释至100mL后,测得其pH<54.在乙酸乙酯中分别加入等体积的下列试剂,乙酸乙酯水解程度最大的是()A2mol/LH2SO4B2mol/LNaOHC蒸馏水D4mol/LCH3COOH5.在盛有氯化钴溶液的试管中,加入一定量的浓盐酸,溶液的颜色的变化是()A蓝色加深B红色加深C由粉红色变为蓝色D由蓝色变为粉红色6.在试管中加入半试管95%乙醇和少量红色氯化钴晶体(CoCl2·6H2O),振荡使其溶解,在常温下所得溶液呈_________色,逐渐加热,则溶液最终会变成________色。原因是_________________________________7.CuCl2的稀溶液呈蓝色,而浓溶液呈黄绿色,有人认为这是因为溶液中存在着下列平衡,[Cu(H2O)4]2+(蓝色)+4Cl-[CuCl4]2-(黄绿色)+4H2O,请你设计一个实验进行验证。____________________________________________________________________________________________________________________________________________________________________________________________________8.CH3COOH+C2H5OHCH3COOC2H5+H2O请根据要求回答下列问题:(1)欲提高乙酸的转化率,可采取的措施有:、等。(2)若用右图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为:、等。(3)此反应以浓硫酸为催化剂,可能会造成、等问题。(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。同一反应时间同一反应温度反应温度/℃转化率(%)选择性(%)*反应时间/h转化率(%)选择性(%)*4077.8100280.21006092.3100387.81008092.6100492.310012094.598.7693.0100*选择性100%表示反应生成的产物是乙酸乙酯和水①根据表中数据,下列(填字母)为该反应的最佳条件。A、120℃,4hB、80℃,2hC、60℃,4hD、40℃,3h②当反应温度达到120℃时,反应选择性降低的原因可能为。参考答案1A2B3A4B5C6粉红色蓝色,加热时随温度升高CoCl2·6H2O逐渐失颜色水呈蓝紫色至纯蓝。7.在盛有CuCl2的稀溶液的试管中,加入一定量的浓盐酸,观察溶液颜色的变化,如溶液颜色变为黄绿色,则证明平衡存在,氯离子浓度增大,平衡向正方向移动。(其它合理方案也可)8.(1)增大乙醇的浓度移去生成物(2)原料来不及反应就被蒸出温度过高,发生了副反应冷凝效果不好,部分产物挥发了(任填两种)(3)产生本量的酸性废液(或造成环境污染)部分原料炭化催化剂重复使用困难催化效果不理想(任填两种)(4)①C②乙醇脱水生成了乙醚