第2课时乙酸1.了解乙酸的组成、物理性质和主要应用
2.掌握乙酸的主要化学性质,掌握酯化反应的原理和实验操作
(重点)乙酸的组成和性质[基础·初探]1.乙酸的组成和结构2
乙酸的物理性质颜色状态气味溶解性熔点俗称无色液体刺激性易溶于水16
6℃冰醋酸3
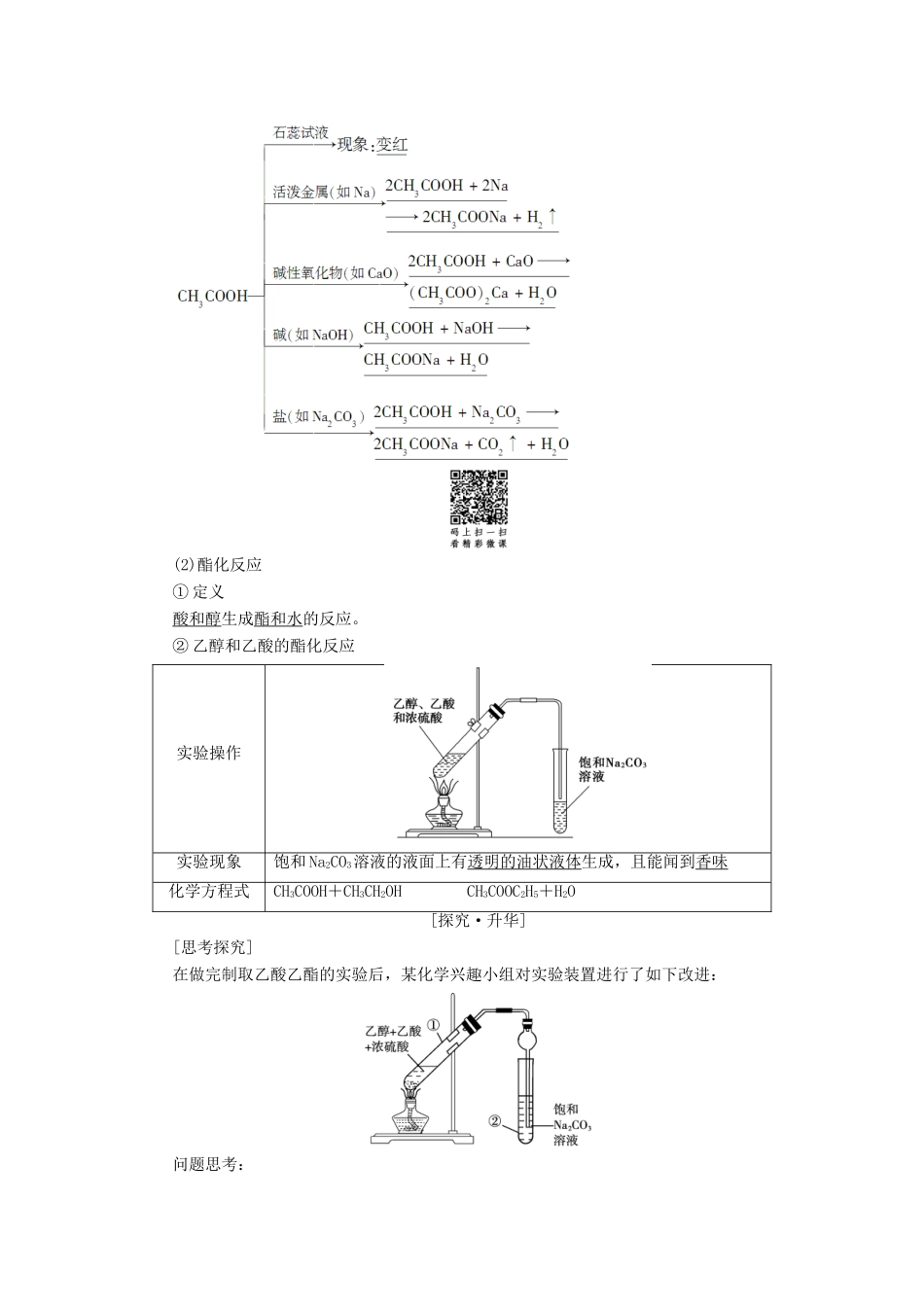
乙酸的化学性质(1)酸的通性(2)酯化反应①定义酸和醇生成酯和水的反应
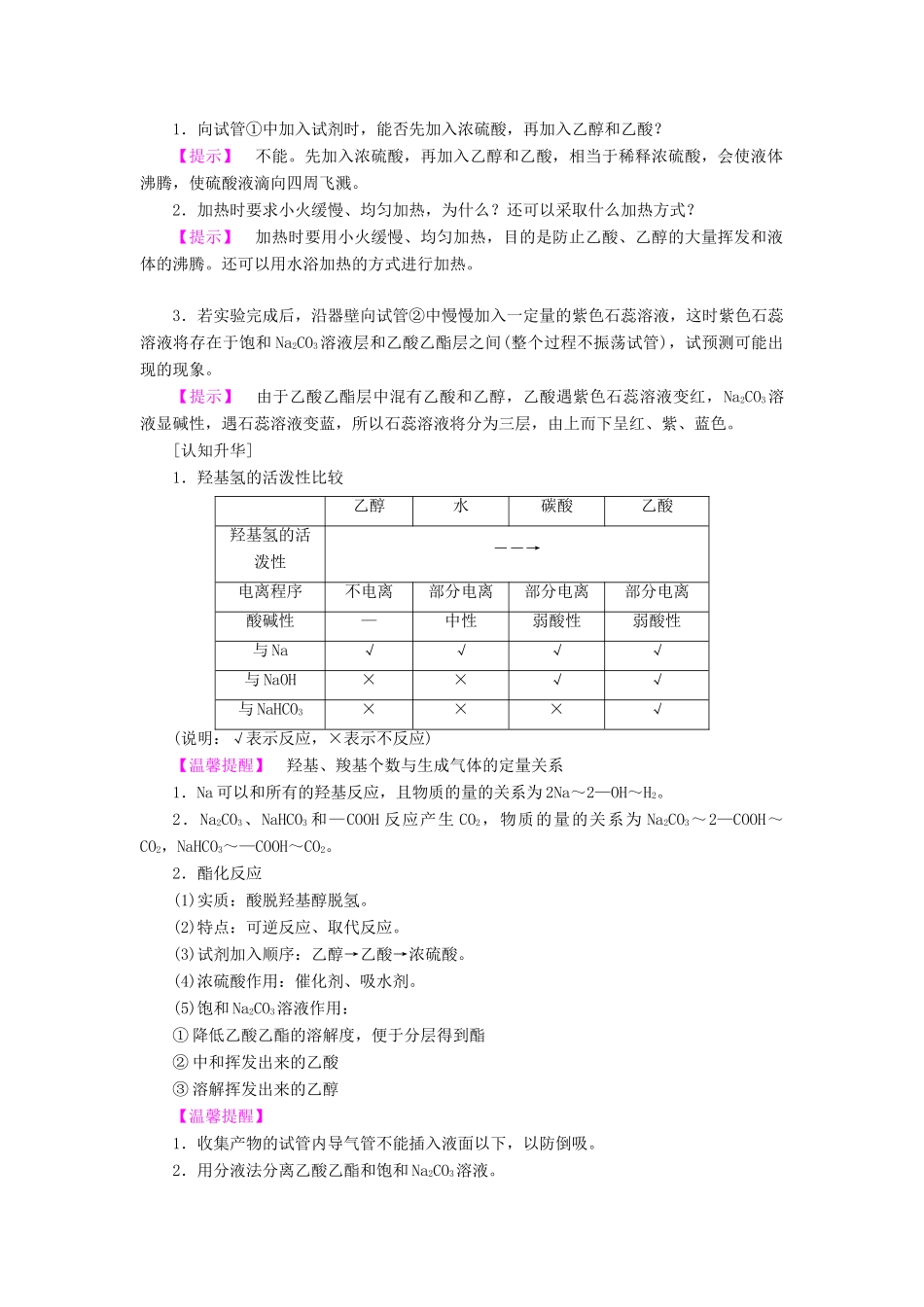
②乙醇和乙酸的酯化反应实验操作实验现象饱和Na2CO3溶液的液面上有透明的油状液体生成,且能闻到香味化学方程式CH3COOH+CH3CH2OHCH3COOC2H5+H2O[探究·升华][思考探究]在做完制取乙酸乙酯的实验后,某化学兴趣小组对实验装置进行了如下改进:问题思考:1.向试管①中加入试剂时,能否先加入浓硫酸,再加入乙醇和乙酸
【提示】不能
先加入浓硫酸,再加入乙醇和乙酸,相当于稀释浓硫酸,会使液体沸腾,使硫酸液滴向四周飞溅
2.加热时要求小火缓慢、均匀加热,为什么
还可以采取什么加热方式
【提示】加热时要用小火缓慢、均匀加热,目的是防止乙酸、乙醇的大量挥发和液体的沸腾
还可以用水浴加热的方式进行加热
3.若实验完成后,沿器壁向试管②中慢慢加入一定量的紫色石蕊溶液,这时紫色石蕊溶液将存在于饱和Na2CO3溶液层和乙酸乙酯层之间(整个过程不振荡试管),试预测可能出现的现象
【提示】由于乙酸乙酯层中混有乙酸和乙醇,乙酸遇紫色石蕊溶液变红,Na2CO3溶液显碱性,遇石蕊溶液变蓝,所以石蕊溶液将分为三层,由上而下呈红、紫、蓝色
[认知升华]1.羟基氢的活泼性比较乙醇水碳酸乙酸羟基氢的活泼性――→电离程序不电离部分电离部分电离部分电离酸碱性—中性弱酸性弱酸性与Na√√√√与NaOH××√√与NaHCO3×××√(说明:√表示反应,×表示不反应)【温馨提醒】羟基、羧基个数与生成气体的定量关系1.Na可以和所有的羟基反应,且物质的量的关系为2Na~2—O