课时2不同类型的晶体【学习目标】:会判断晶体的类型;不同类型晶体的结构特点与性质
【复习回顾】:1、写电子式:Na2O2、H2O2、2、分别举例说明:构成物质的微粒通过什么作用力构成了物质
【新课学习】:观察22页图1-17,思考回答【你知道吗】问题
【阅读理解】教材22-23页【思考回答记忆】下列问题:一、固态物质的存在形态有哪些
决定存在形态的因素是什么
二、晶体有哪些不同的类型
分类依据是什么
请分别举例说明
三、各类晶体的内部存在什么作用力
化学式的含义是什么
1.离子晶体:由通过键结合而成的晶体
【观察思考】(1)在NaCl晶体中,每个Na+吸引个Cl-,每个Cl-吸引个Na+
(2)NaCl晶体中存在“NaCl”分子吗
离子晶体的化学式表示什么意义
2.分子晶体:由通过结合而成的晶体
【观察思考】在干冰结构中存在“CO2”分子吗
分子晶体的化学式表示什么意义
3.原子晶体:由通过结合而成的结构的晶体
【观察思考】教材23页图1-20,完成【交流和讨论】及下面内容:(1)在石英(SiO2)晶体中,每个Si原子与个O原子形成个键;每个O原子与个Si原子形成个键,向伸展,形成结构
(2)石英晶体中存在“SiO2”分子吗
原子晶体的化学式表示什么意义
4、金属晶体:范围:
(补:金属晶体内的作用力为金属键)四、各类型晶体的物理性质的特点:【观察思考】23页表1-10
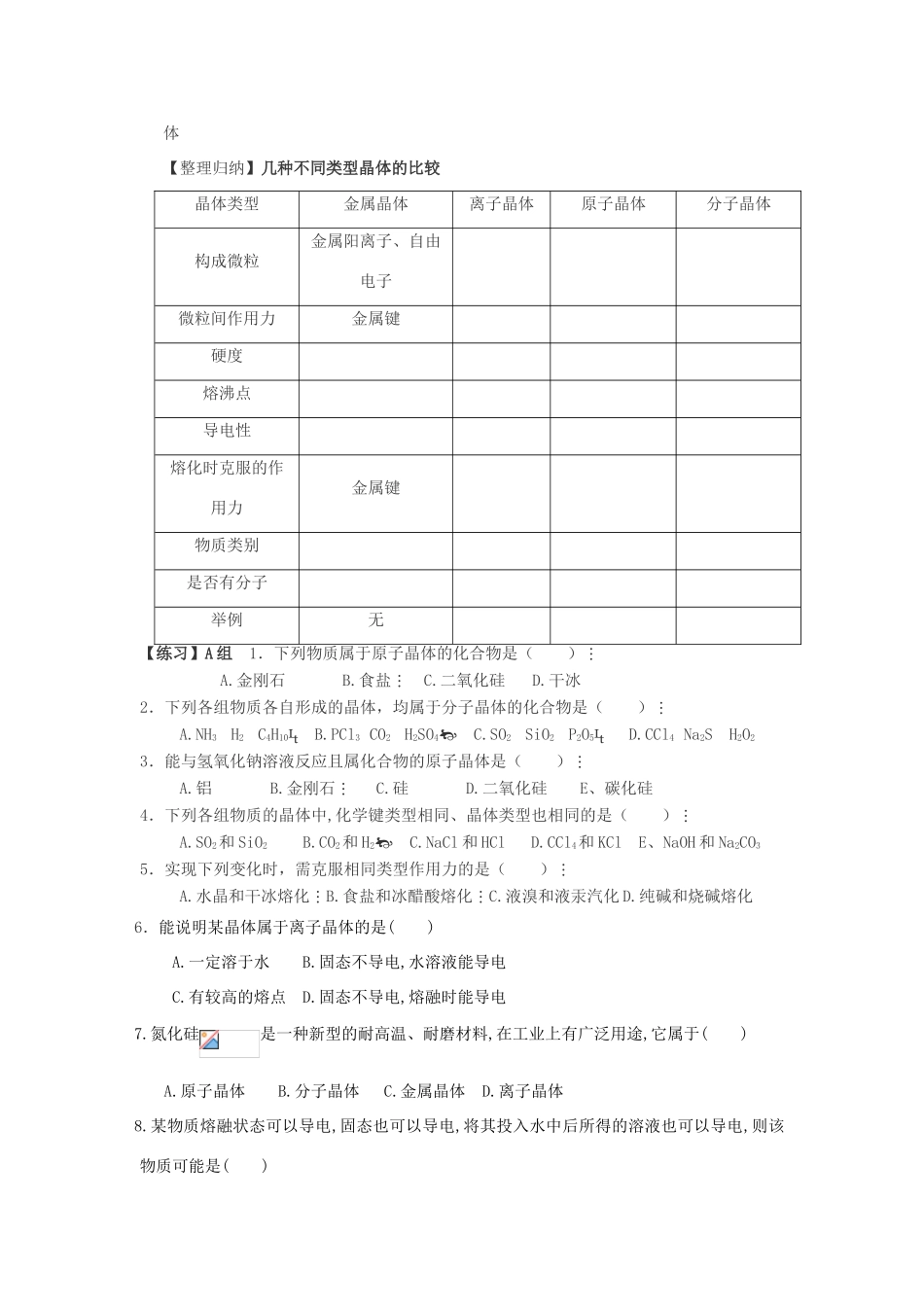
【结论】不同类型晶体的熔沸点高低,一般:晶体>晶体>晶体【整理归纳】几种不同类型晶体的比较晶体类型金属晶体离子晶体原子晶体分子晶体构成微粒金属阳离子、自由电子微粒间作用力金属键硬度熔沸点导电性熔化时克服的作用力金属键物质类别是否有分子举例无【练习】A组1.下列物质属于原子晶体的化合物是()A
干冰2.下列各组物质各自