第3课时探究铁及其化合物的氧化性或还原性1
从氧化还原的角度认识铁及其重要化合物的主要性质
掌握不同价态铁元素的转化途径
重难点3
掌握检验Fe2+、Fe3+的方法
重点铁及其化合物教材整理1铁元素的存在1.含量铁元素在地壳中的质量分数仅次于氧、硅和铝
2.存在形态(1)游离态:存在于陨铁中
(2)化合态①主要化合价:+2、+3
②存在形式:主要以矿石的形式存在
如:黄铁矿(FeS2)、赤铁矿(Fe2O3)、磁铁矿(Fe3O4)
3.单质铁的化学性质教材整理2铁的氧化物和氢氧化物1.铁的氧化物名称氧化亚铁氧化铁四氧化三铁俗名—铁红磁性氧化铁化学式FeOFe2O3Fe3O4(FeO·Fe2O3)颜色黑色红棕色黑色稳定性不稳定稳定稳定铁的化合价+2+3+2(占)+3(占)氧化亚铁和氧化铁都具有碱性氧化物的通性,都能与酸反应生成相应的盐和水
2.铁的氢氧化物名称氢氧化亚铁氢氧化铁化学式Fe(OH)2Fe(OH)3颜色白色红褐色稳定性常温下易被空气氧化(白色迅速变为灰绿色,最后变为红褐色):4Fe(OH)2+O2+2H2O===4Fe(OH)3受热发生分解:2Fe(OH)3=====Fe2O3+3H2O(化学方程式)溶解性不溶于水不溶于水如图所示
向盛有FeSO4溶液的试管中滴加NaOH溶液可以制得Fe(OH)2
但白色的沉淀迅速变成灰绿色,最终变为红褐色
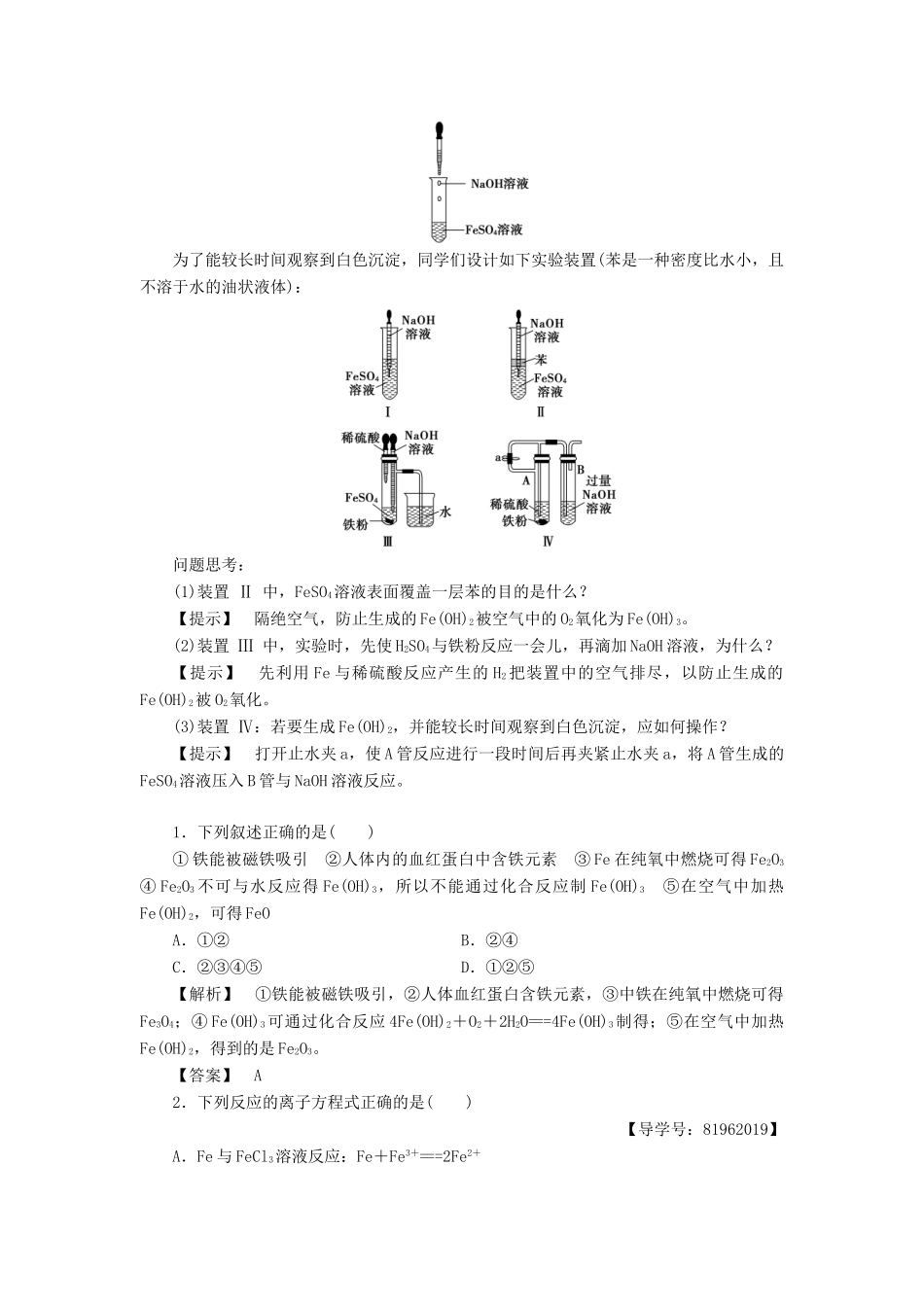
为了能较长时间观察到白色沉淀,同学们设计如下实验装置(苯是一种密度比水小,且不溶于水的油状液体):问题思考:(1)装置Ⅱ中,FeSO4溶液表面覆盖一层苯的目的是什么
【提示】隔绝空气,防止生成的Fe(OH)2被空气中的O2氧化为Fe(OH)3
(2)装置Ⅲ中,实验时,先使H2SO4与铁粉反应一会儿,再滴加NaOH溶液,为什么
【提示】先利用Fe与稀硫酸反应产生的H2把装置中的空气排尽,以防止生成的Fe(OH)2被O2