命题区间三阿伏加德罗常数及应用角度一一定量物质中微粒(共价键)数目的判断1.宏观量(m、V)与微粒数的换算公式物质所含微粒(分子、原子、离子、质子、中子和电子等)数目的计算公式为N=n·NA,因此确定微粒数目(N)的前提是确定目标微粒的物质的量(n),以物质的量为中心的化学计量间的换算关系如下:[说明]①物质的量、质量、微粒数目的多少均与温度、压强无关
②物质的量浓度的大小与所取溶液的体积无关
2.熟悉每摩常考物质中指定微粒(共价键)数目(1)求微粒数目举例判断正误注意事项①1L0
1mol·L-1K2CO3溶液中含有K+数目为0
整体与部分的关系b
溶质中和溶剂中都含有的微粒c
是离子还是官能团②1L0
1mol·L-1H2O2溶液中含有O原子数为0
2NA×③1molNa2O2中含有的阴离子数为2NA×④1mol—OH中含有的电子数为10NA×⑤1molOH-中含有的电子数为10NA√⑥1mol熔融的KHSO4中含有2NA个阳离子×⑦氢原子数为0
4NA的甲醇分子中含有的共×用电子对数为0
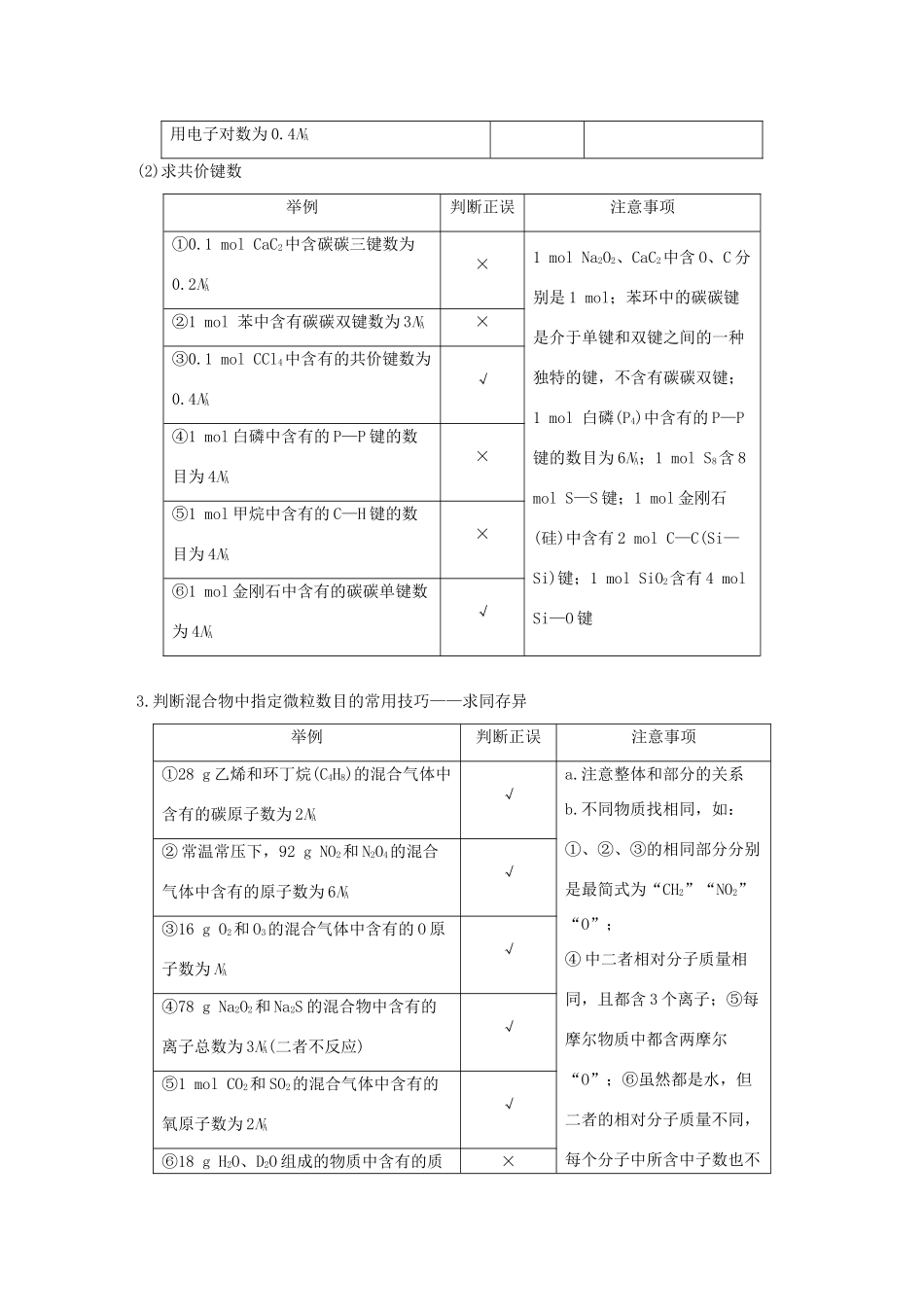
4NA(2)求共价键数举例判断正误注意事项①0
1molCaC2中含碳碳三键数为0
2NA×1molNa2O2、CaC2中含O、C分别是1mol;苯环中的碳碳键是介于单键和双键之间的一种独特的键,不含有碳碳双键;1mol白磷(P4)中含有的P—P键的数目为6NA;1molS8含8molS—S键;1mol金刚石(硅)中含有2molC—C(Si—Si)键;1molSiO2含有4molSi—O键②1mol苯中含有碳碳双键数为3NA×③0
1molCCl4中含有的共价键数为0
4NA√④1mol白磷中含有的P—P键的数目为4NA×⑤1mol甲烷中含有的C—H键的数目为4NA×⑥1mol金刚石中含有的碳碳单键数为4NA√3
判断混合物中指定微粒数目的常用技巧——求同存异举例判断正误