实验9铝及其化合物的性质铝及其化合物性质1、了解铝的两性性质2、学会铝和氢氧化钠的化学反应方程式及离子反应方程式的书写3、学会实验室制取氢氧化铝2Al+6HCl===2AlCl3+3H2↑2Al+2NaOH+2H2O===2NaAlO2+3H2↑Al2(SO4)3+6NH3·H2O===2Al(OH)3↓+3(NH4)2SO4试管、试管架、胶头滴管、剪刀、砂纸、铝片、盐酸(2mol·L1−)、NaOH溶液(2mol·L1−)、Al2(SO4)3溶液(0
5mol·L1−)、氨水实验一铝与盐酸反应铝与氢氧化钠溶液反应实验操作向一支洁净的小试管中加入5ml盐酸,再加入一小段被砂纸打磨过的铝片,观察实验现象
过一段时间后,将点燃的木条放在试管口,你看到什么现象
向一支洁净的小试管中加入5mlNaOH溶液,再加入一小段被砂纸打磨过的铝片,观察实验现象
过一段时间后,将点燃的木条放在试管口,你看到什么现象
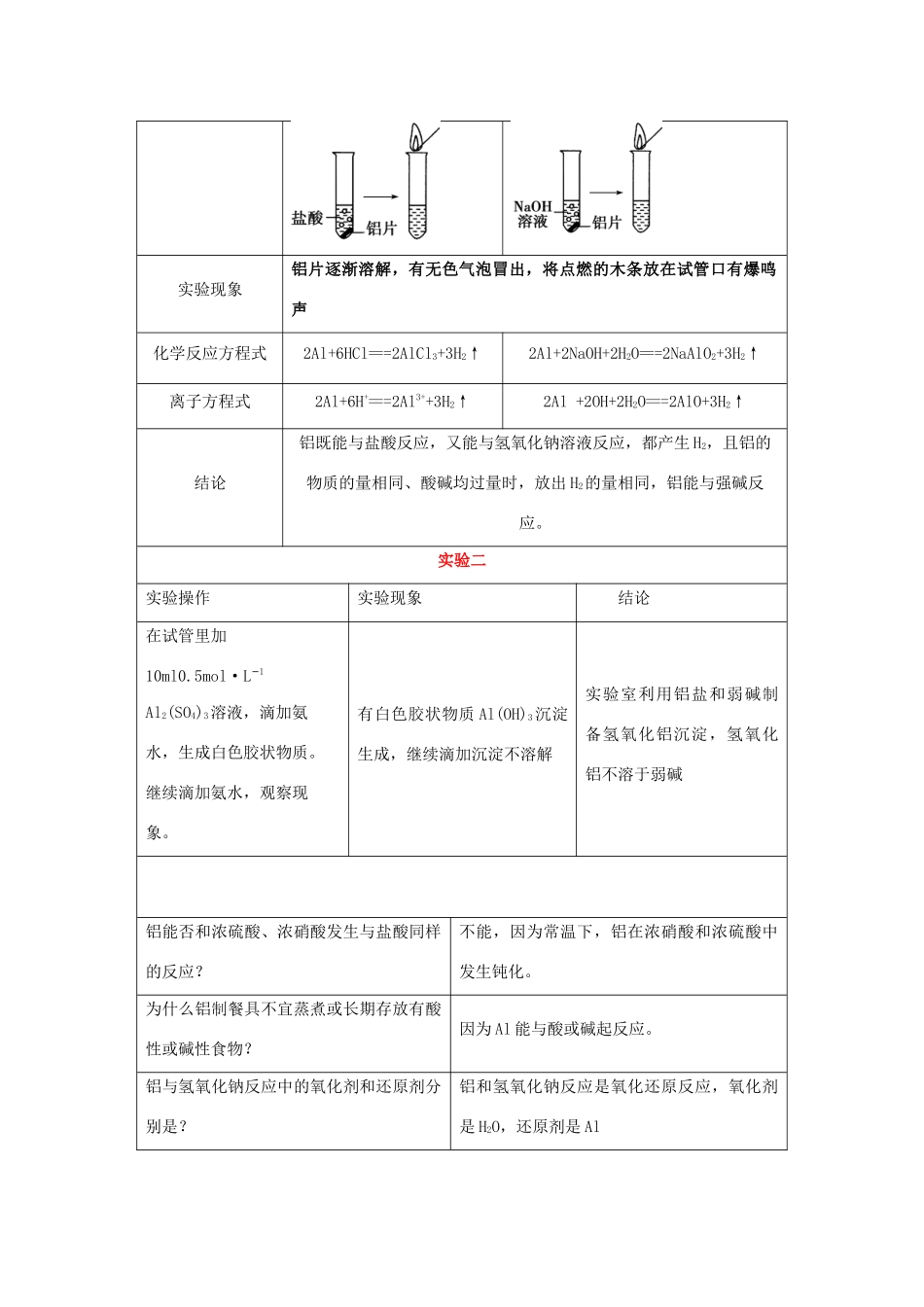
实验现象铝片逐渐溶解,有无色气泡冒出,将点燃的木条放在试管口有爆鸣声化学反应方程式2Al+6HCl===2AlCl3+3H2↑2Al+2NaOH+2H2O===2NaAlO2+3H2↑离子方程式2Al+6H+===2Al3++3H2↑2Al+2OH+2H2O===2AlO+3H2↑结论铝既能与盐酸反应,又能与氢氧化钠溶液反应,都产生H2,且铝的物质的量相同、酸碱均过量时,放出H2的量相同,铝能与强碱反应
实验二实验操作实验现象结论在试管里加10ml0
5mol·L1−Al2(SO4)3溶液,滴加氨水,生成白色胶状物质
继续滴加氨水,观察现象
有白色胶状物质Al(OH)3沉淀生成,继续滴加沉淀不溶解实验室利用铝盐和弱碱制备氢氧化铝沉淀,氢氧化铝不溶于弱碱铝能否和浓硫酸、浓硝酸发生与盐酸同样的反应
不能,因为常温下,铝在浓硝酸和浓硫酸中发生钝化
为什么铝制餐具不宜蒸煮或长期存放有酸性或