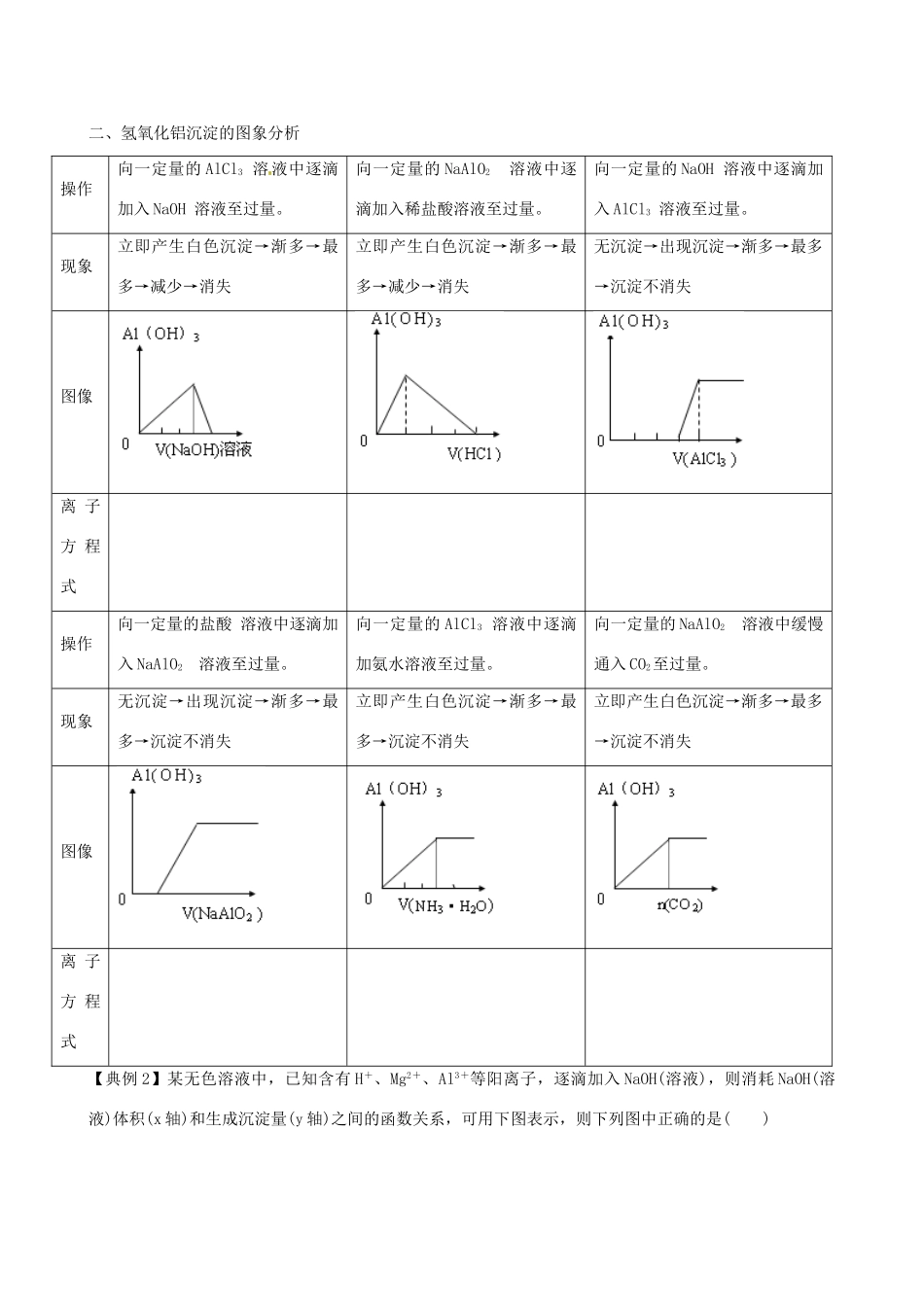
江苏省常州市西夏墅中学高三化学一轮复习学案:从铝土矿到铝合金【复习目标】1、了解铝的主要性质和重要应用
2、了解铝的重要化合物的性质和重要应用【基础知识梳理】一、铝的重要性质1.物理性质铝为银白色金属,熔点,沸点密度,导电性仅次于银、铜和金
化学性质(1)跟非金属单质反应①氧气
常温:在表面生成一层致密的氧化物薄膜,阻止内部的金属继续与氧气反应
点燃:②铝容易和卤素反应,常温下和氯气激烈化合生成三氯化铝:(2)铝与酸反应①与非氧化性强酸(稀硫酸、盐酸)反应:②与氧化性酸常温下,铝、铁遇浓硫酸、浓硝酸发生钝化,加热时,铝与稀硝酸反应不产生H2,与热浓硫酸、浓硝酸反应:(3)铝与强碱溶液反应:(4)铝热反应铝粉和氧化铁粉末的混合物称为铝热剂,铝热反应可用于焊接钢轨,可用于冶炼Ni、Mn、V等难熔金属
二、铝的重要化合物1
氧化铝(1)氧化铝白色固体,高熔点(2045℃),溶于水,氧化物与酸反应:与碱反应:(2)用途:熔点很高,是一种比较好的耐火材料,还可以制作各种宝石
氢氧化铝(1)化学性质:①氢氧化铝是氢氧化物,只溶于酸或碱,而不溶于酸或碱
与酸反应:(离子方程式)与碱反应:(离子方程式)②氢氧化铝受热分解:(2)Al(OH)3的制备:①用弱碱氨水与可溶性铝盐反应
②向偏铝酸盐中通入CO2(3)明矾明矾是含有结晶水的硫酸钾和硫酸铝的复盐
电离方程式:,Al3+容易水解,生成胶状的氢氧化铝Al(OH)3,氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,并形成沉淀,使水澄清
所以,明矾是一种较好的净水剂
【要点名师透析】一、“铝三角”的转化关系及其应用1
应用(1)制取Al(OH)3:A13++3NH3·H2O=Al(OH)3↓+3NH4+3AlO2-+Al3+=4Al(OH)3↓AlO2-+CO2=Al(OH)3↓+HCO3-(2)离子共存问题:A