重庆市万州分水中学高中化学必修一《第1章第2节第2课时物质的量在化学实验中的应用》学案【学习导引】1.阅读教材,填写概念;依据示例,应用公式,进行计算物质的量浓度符号为______,常用单位是______
1molNaOH固体溶于水,配成1L溶液,所得溶液的溶质物质的量浓度为0
1mol/L
练习:①8gNaOH固体溶于水,配成500mL溶液,所得溶液的溶质物质的量浓度为______
②将5mol/L的硫酸20mL稀释成0
5mol/L的稀硫酸______mL
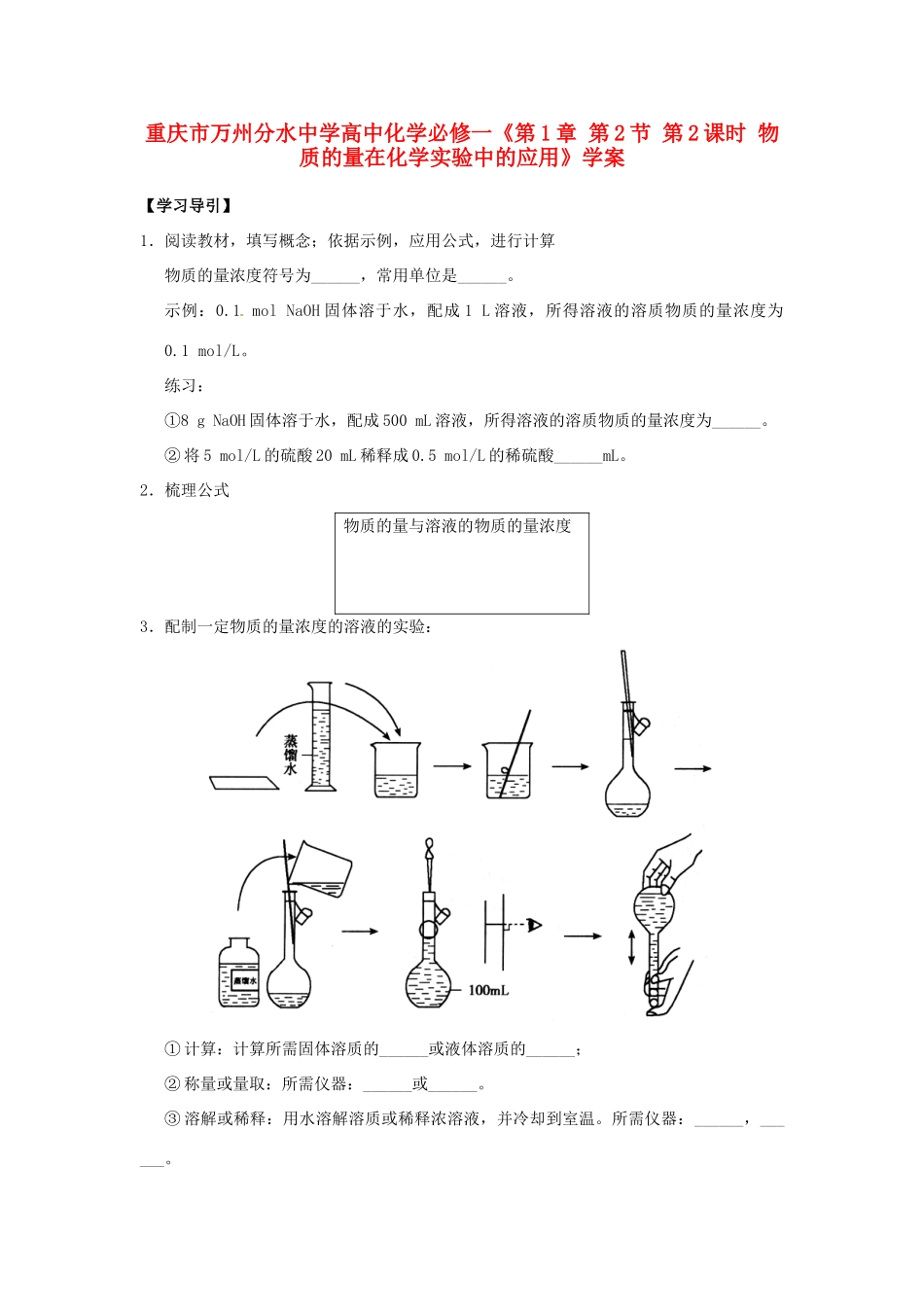
2.梳理公式物质的量与溶液的物质的量浓度3.配制一定物质的量浓度的溶液的实验:①计算:计算所需固体溶质的______或液体溶质的______;②称量或量取:所需仪器:______或______
③溶解或稀释:用水溶解溶质或稀释浓溶液,并冷却到室温
所需仪器:______,______
④转移:将烧杯中的溶液沿______注入______中
⑤洗涤:用蒸馏水洗涤__________________2~3次,并将每次洗涤液都转入______中,振荡,使溶液混合均匀
⑥定容:继续往______中小心地加水,直到液面离______时,改用______滴加蒸馏水至液面与______相切
⑦摇匀:塞好瓶塞,反复上下颠倒,摇匀
【同步训练】1.将0
2molNa2CO3固体溶解于水,制得500mL溶液,所得溶液中Na2CO3的物质的量浓度为()A.0
1mol/LB.0
25mol/LC.0
4mol/LD.1mol/L2.将0
5molNaCl固体溶解于水,制得NaCl的物质的量浓度为2mol/L溶液,则溶液的体积为()A.100mLB.250mLC.400mLD.1000mL3.100ml0
1mol/L的氢氧化钠溶液中溶质的量为()A.质量为4
0gB.质量为0
4gC.物质的量为0
1molD.物质的量为10mo