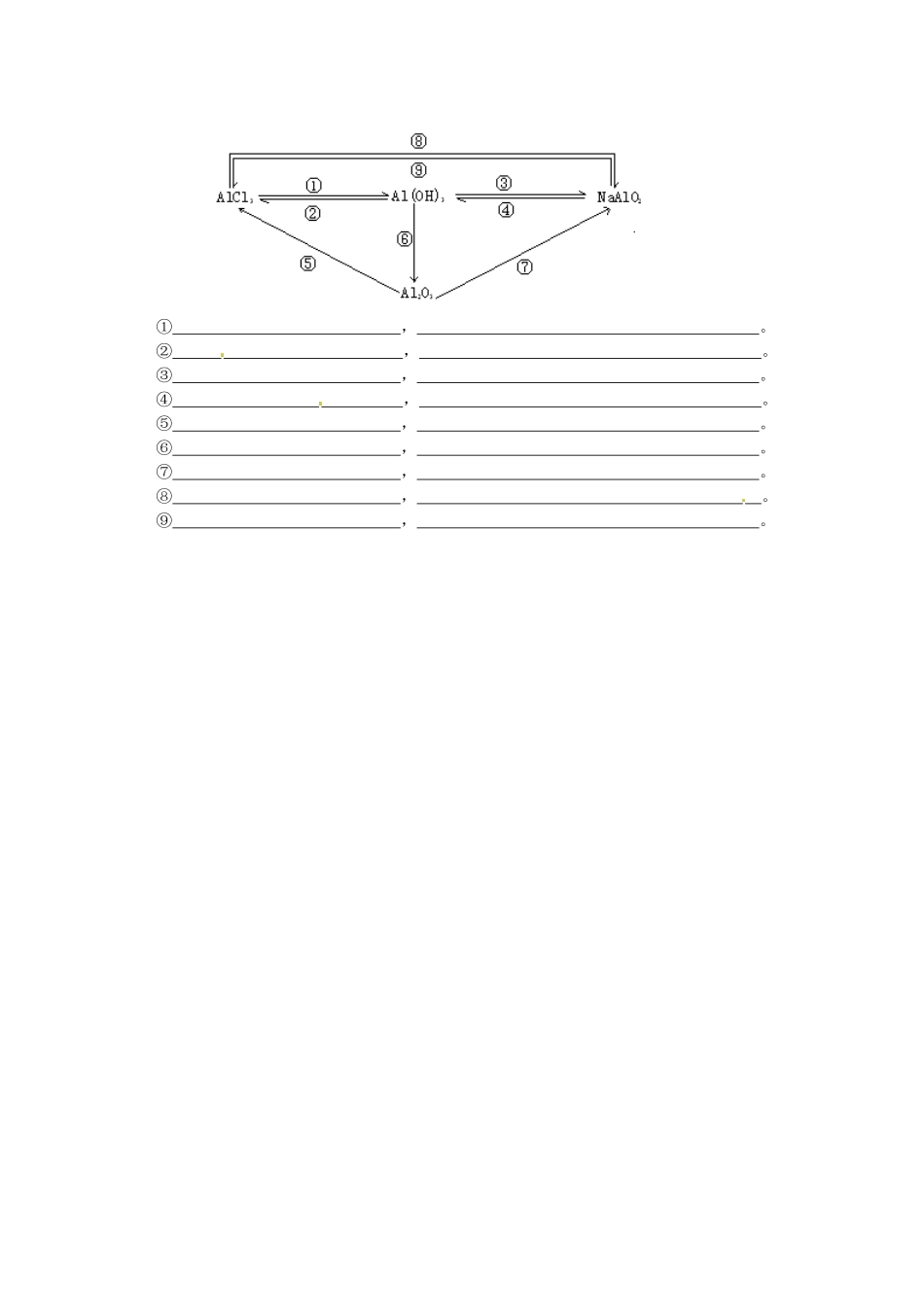
海南省海口市第十四中学高一化学必修一导学案:几种重要的金属化合物【学习目标】1、掌握Al2O3、Al(OH)3的两性
2、掌握Al(OH)3的制备方法
【学习重点】Al(OH)3的性质和与Al(OH)3有关的计算【复习巩固】1、多数的金属氢氧化物不溶于水,除了等几种碱外
2、不溶于水的金属氢氧化物受热分解,写出下列碱受热分解的化学反程式
Fe(OH)3,Cu(OH)2
3、多数金属氢氧化物都可反应,写出下列碱与HCl反应的化学的离子方程式
Fe(OH)3,Cu(OH)2【自主学习】一、铝的重要化合物1、氧化铝Al2O3是一种色熔点的物质,溶于水,能与盐酸、NaOH溶液反应
Al2O3+HCl
离子方程式为:Al2O3+NaOH
离子方程式为:Al2O3是一种性氧化物,因为
2、氢氧化铝[实验探究]1、在试管里加入10mL0
5mol/LAl2(SO4)3溶液,滴加氨水,现象为;继续滴加氨水现象为
2、将1中产生的沉淀分装在两个试管中,往一支试管里滴加2moL/L盐酸,往另一支试管滴加2mol/LNaOH溶液
边加边振荡,现象为
[归纳总结]1、氢氧化铝的实验室制法实验原理:(离子方程式)2、氢氧化铝的性质物理性质:氢氧化铝是一种色状的物质;溶于水
化学性质:①与盐酸等酸反应的化学方程式:
与NaOH等碱溶液反应的化学方程式:
氢氧化铝是一种既能与反应,又能与反应的性氢氧化物
原因:②氢氧化铝受热分解方程式:Al(OH)3用途:①医用中和胃酸:化学方程式:②净水剂,利用了其具有性质,能凝聚水中的悬浮物质
[思考与讨论]①能否用Al2O3与水直接反应制取Al(OH)3
如果不能请你设计用Al2O3制取Al(OH)3的实验方案并且写出反应的化学方程式
H++AlO2-+H2OAl(OH)3Al3++3OH-酸式电离碱式电离(填能与不能)原因、
②能否用AlCl3与水直接反应制取A