山东省武城县第二中学高一化学《第一章原子结构与元素周期》学案(必修二鲁科版)一.概念辨析:1:同位素:相同而不同的互称为同位素
2:同素异形体
易错点:(1)元素的种类由原子核内决定(2)核素的种类由决定(3)同种元素的不同核素性质基本相同,而性质有一定别
(4)原子的表示
(5)同位素指的是而同素异形体是指(6)质量数仅为该种原子的相对原子质量的近似值
判断元素原子失电子能力强弱的方法①比较
置换反应越容易发生,元素原子的失电子能力越
一般说来,碱性越强,元素原子的失电子能力越
其他比较方法如:利用金属活动顺序表,置换反应,阳离子氧化性的强弱,形成原电池等
判断元素原子得电子能力强弱的方法①比较
一般说来,反应越容易进行,生成的气态氢化物越,元素原子得电子能力越
一般说来,酸性越,元素原子得电子的能力越
其他比较方法如:利用置换反应,阴离子还原性的强弱,与金属反应生成金属阳离子的价态等
易错点:(1)得电子数多的,得电子越容易吗
(2)失电子数多的,失电子能力越强吗
三、同周期(第三周期)元素性质的递变规律1、第3周期元素的名称及符号
2、钠、镁、铝金属性相对强弱:元素钠镁铝单质与水反应冷水中剧烈反应热水中反应热水中微弱反应单质与盐酸反应(剧烈程度)逐渐最高价氧化物对应水化物化学式碱性逐渐结论①钠、镁、铝三种元素原子失电子能力逐渐;②同一周期从左到右,元素原子失电子能力逐渐
2、(1)向MgCl2溶液中滴加NaOH溶液,有关现象有关离子方程式(2)向AlCl3溶液中逐滴滴加过量NaOH溶液,有关现象有关离子方程式,3
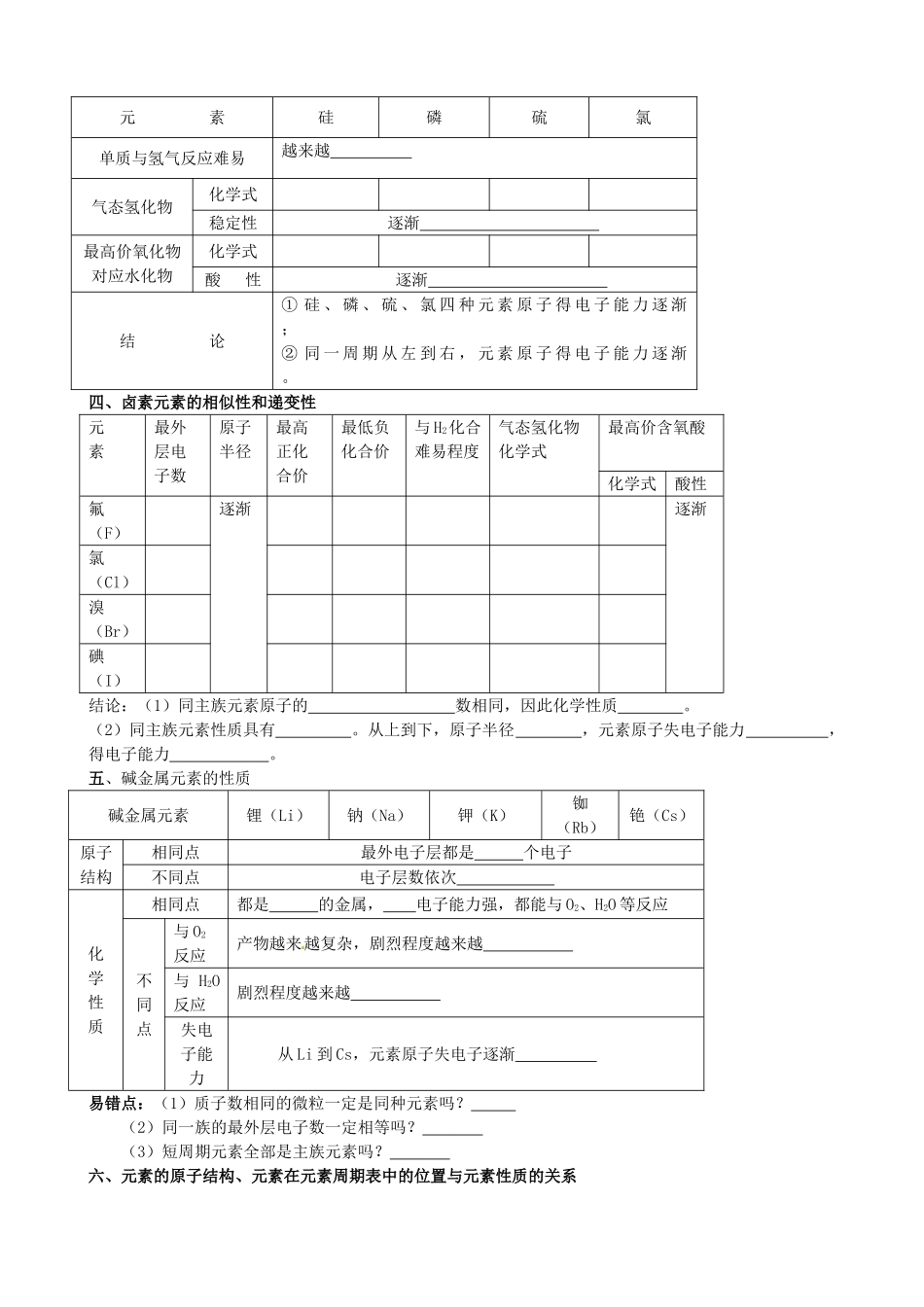
硅、磷、硫、氯四种元素性质的比较:元素硅磷硫氯单质与氢气反应难易越来越气态氢化物化学式稳定性逐渐最高价氧化物对应水化物化学式酸性逐渐结论①硅、磷、硫、氯四种元素原子得电子能力逐渐;②同一周期从左到右,元素原子得电子能力逐渐