浙江省临海市白云高级中学高一化学必修一学案:课题22硫酸的制备和性质学习目标:1、了解接触法制硫酸的反应原理;2、掌握浓硫酸的性质:吸水性、脱水性、强氧化性
学习重点:了解接触法制硫酸的反应原理;掌握浓硫酸的性质:吸水性、脱水性、强氧化性
学习难点:浓硫酸的性质:吸水性、脱水性、强氧化性
【预习案】(阅读书本P90-93)1、硫酸的工业制法古代:
目前工业:接触法制硫酸
归纳完成下表:三阶段1
SO3的吸收三设备三反应注意事项(2)尾气的吸收
通常工业上是用氨水来吸收SO2
2、硫酸的性质(1)物理性质:无色油状的液体,沸点高,密度大,能与水以任意比互溶,溶解时放出大量的热
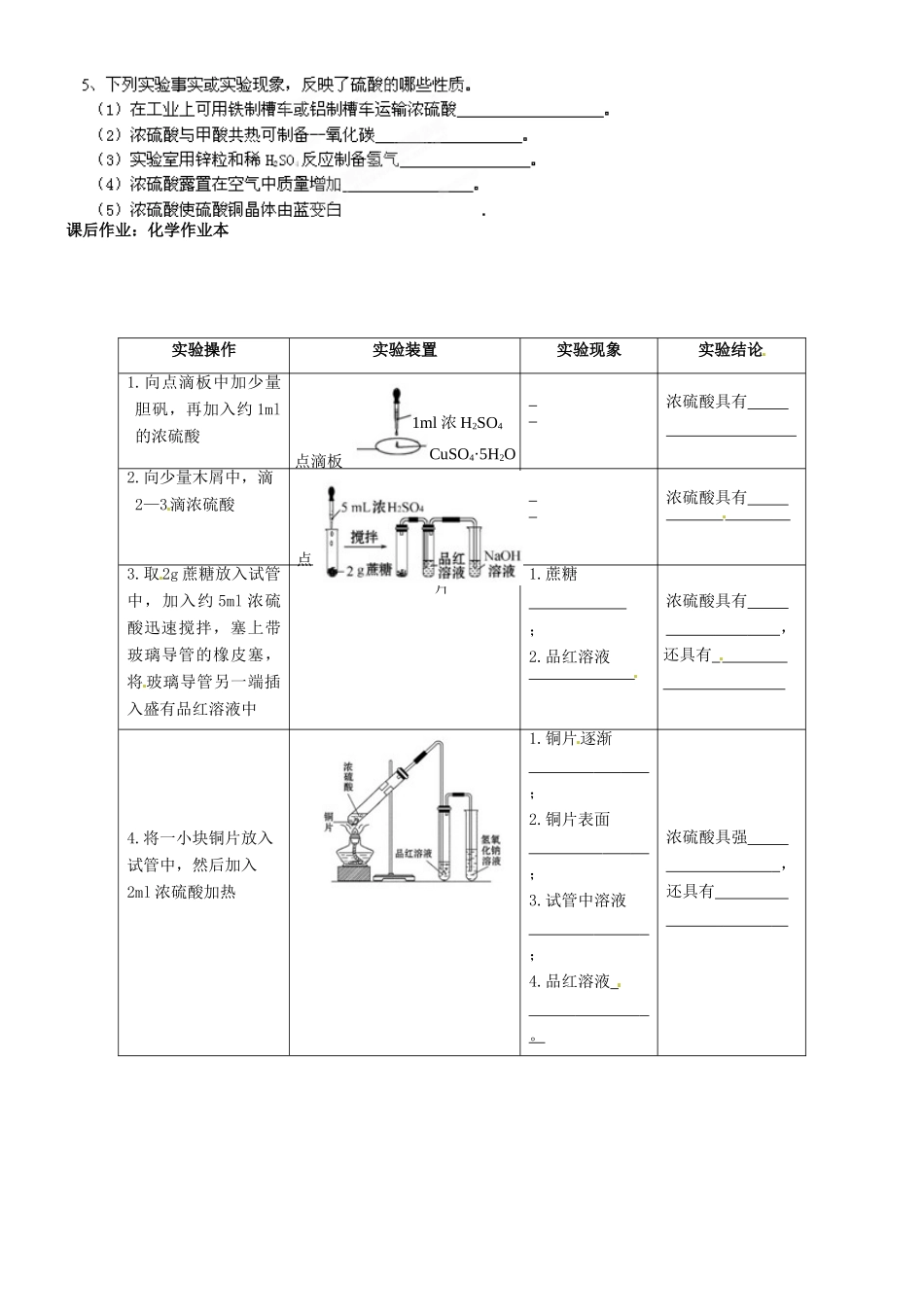
(2)化学性质:①吸水性;②脱水性;③强氧化性;【预习自测】1、区别浓H2SO4和稀H2SO4,既简单又可靠的方法是()A、各取少许溶液分别放入铜片`B、分别与石蕊试液作用C、用玻璃棒各蘸少许液涂在纸上D、各取少许溶液分别放入铝片2、工业上常用稀硫酸清洗铁表面的锈层,这是利用硫酸的()A、强氧化性B、不挥发性C、酸性D、吸水性【问题探究】硫酸性质【总结】浓硫酸的特性:①吸水性:H2SO4+nH2O==H2SO4·nH2O②脱水性:浓硫酸可以使有机化合物中的H、O元素按H2O的组成从有机物中“脱离”出来,结合成水分子
如:C12H22O11(蔗糖)遇浓硫酸发生脱水碳化
③强氧化性:【达标检测】(共50分,每空5分)1、接触发生产H2SO4的过程中,对“三废”处理正确的是()①尾气用氨水处理②污水用石灰乳处理③废渣用来制水泥、炼铁④设置“废热”锅炉产生蒸气、供热或发电A、只有①②B、只有①③④C、只有①②③D、全部2、下列关于硫酸性质的描述中,正确的是()A、浓H2SO4有氧化性,稀H2SO4无氧化性B、由于浓H2SO4具有脱水性,所以可用做干燥剂C、稀H2SO4与铜不反应,但浓H2SO