基础整合考点聚焦返回目录第十单元酸和碱基础整合返回目录考点聚焦一、常见的酸1
盐酸与硫酸性质及用途的比较盐酸硫酸浓酸的性质(1)纯净的浓盐酸是无色有刺激性气味的液体(2)易挥发,在空气中生成白雾(3)有酸味和腐蚀性(1)纯净的浓硫酸是无色、粘稠状的油状液体(2)在空气中不易挥发、有吸水性特性:强腐蚀性、脱水性、溶于水放出大量的热稀酸的化学性质使紫色石蕊溶液变红色,不能使无色酚酞溶液变色(2)与活泼金属反应,与Cu等不反应Zn+2HClZnCl2+H2↑Mg+2HClMgCl2+H2↑(2)与活泼金属反应,与Cu等不反应Zn+H2SO4ZnSO4+H2↑Mg+H2SO4MgSO4+H2↑(3)与金属氧化物反应Fe2O3+6HCl2FeCl3+3H2O(3)与金属氧化物反应Fe2O3+3H2SO4Fe2(SO4)3+3H2O(4)与CaCO3等含有C的物质反应CaCO3+2HClCaCl2+CO2↑+H2ONa2CO3+2HCl2NaCl+H2O+CO2↑(4)与CaCO3等含有C的物质反应Na2CO3+H2SO4Na2SO4+CO2↑+H2O与CaCO3、BaCO3等反应缓慢甚至停止(5)与碱的反应Ca(OH)2+2HClCaCl2+2H2O(5)与碱的反应H2SO4+Ca(OH)2CaSO4+2H2O用途重要化工产品
用于金属表面除锈,制造药物等;人体胃液中含有盐酸,可帮助消化重要化工原料
用于生产化肥、农药、火药、染料以及冶炼金属,精炼石油和金属除锈等
浓硫酸具有吸水性,在实验室常用作干燥剂基础整合返回目录考点聚焦2
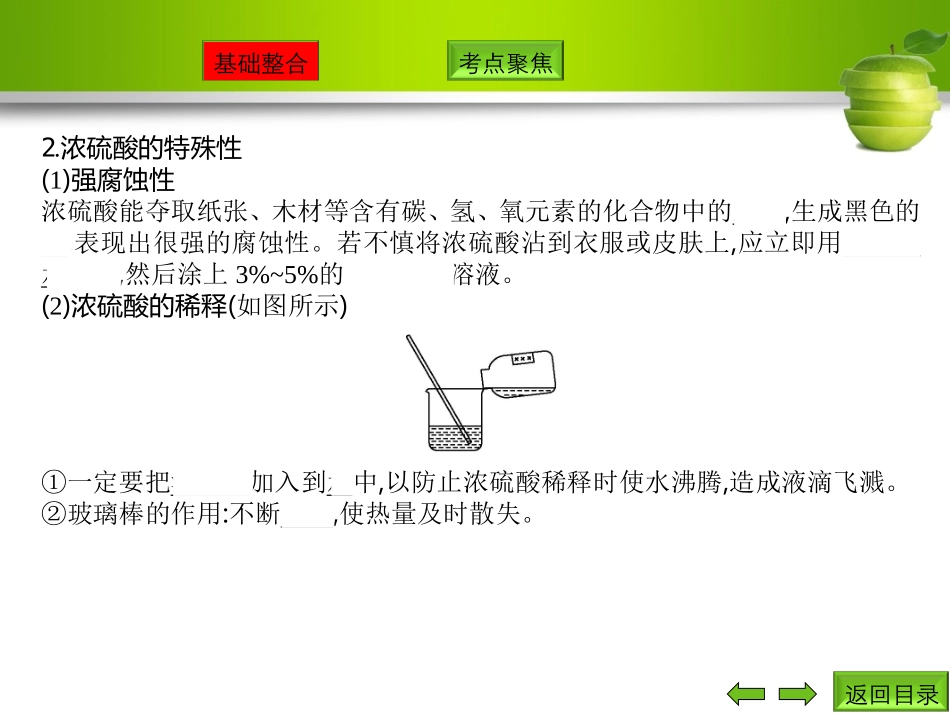
浓硫酸的特殊性(1)强腐蚀性浓硫酸能夺取纸张、木材等含有碳、氢、氧元素的化合物中的水分,生成黑色的炭,表现出很强的腐蚀性
若不慎将浓硫酸沾到衣服或皮肤上,应立即用大量的水冲洗,然后涂上3%~5%的碳酸氢钠溶液
(2)浓硫酸的稀释(如图所示)①一定要把浓硫酸加