电解原理及其应用【学习目标】1.通过电能转化为化学能的探究活动,了解电解池工作原理
2.能正确书写电解池的电极反应式及电解反应方程式
【重点难点】电解原理及其应用【活动方案】活动一:电解原理电解水的成功,使人们意识到电可以用于化学研究
英国科学家戴维在思考:电可以分解水,那么,电对于盐溶液又将产生什么作用呢
1.大胆猜想:在阴、阳两极上可能会出现什么现象
两极上析出或逸出的产物可能是什么
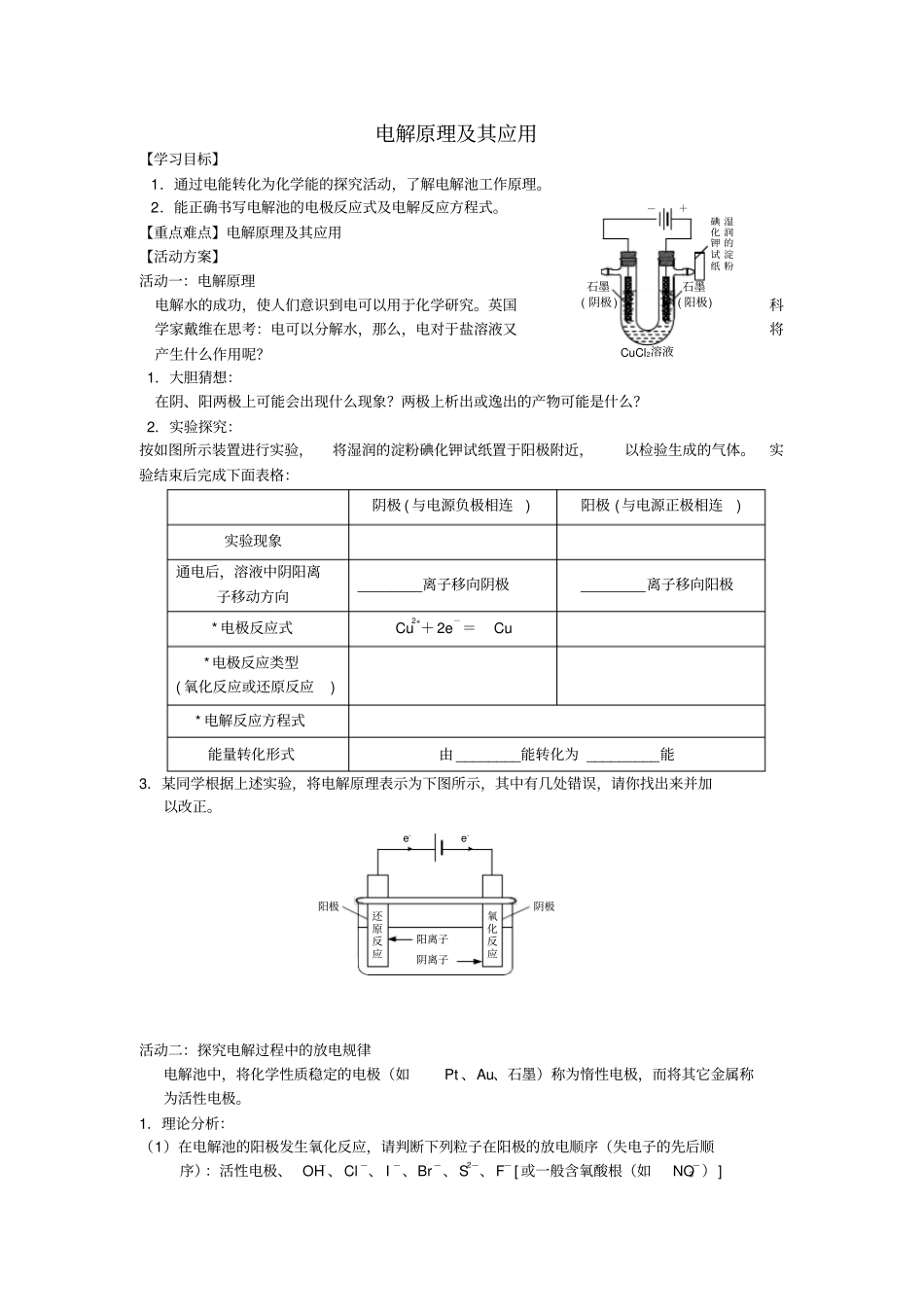
2.实验探究:按如图所示装置进行实验,将湿润的淀粉碘化钾试纸置于阳极附近,以检验生成的气体
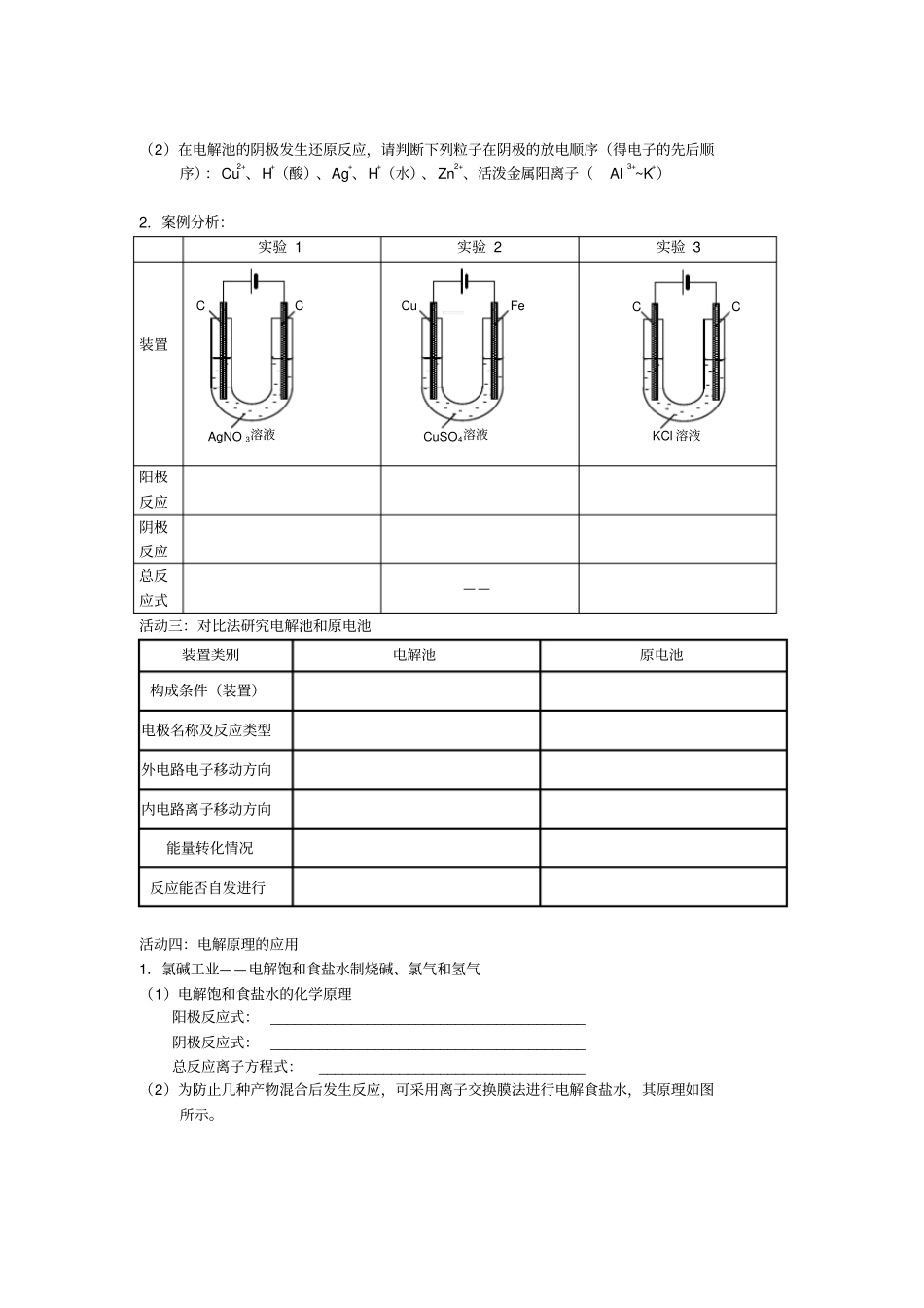
实验结束后完成下面表格:阴极(与电源负极相连)阳极(与电源正极相连)实验现象通电后,溶液中阴阳离子移动方向________离子移向阴极________离子移向阳极*电极反应式Cu2++2e-=Cu*电极反应类型(氧化反应或还原反应)*电解反应方程式能量转化形式由________能转化为_________能3.某同学根据上述实验,将电解原理表示为下图所示,其中有几处错误,请你找出来并加以改正
阳离子阴离子还原反应氧化反应e-e-阳极阴极活动二:探究电解过程中的放电规律电解池中,将化学性质稳定的电极(如Pt、Au、石墨)称为惰性电极,而将其它金属称为活性电极
1.理论分析:(1)在电解池的阳极发生氧化反应,请判断下列粒子在阳极的放电顺序(失电子的先后顺序):活性电极、OH—、Cl—、I—、Br—、S2—、F—[或一般含氧酸根(如NO3—)]石墨石墨CuCl2溶液-+(阴极)(阳极)湿润的淀粉碘化钾试纸(2)在电解池的阴极发生还原反应,请判断下列粒子在阴极的放电顺序(得电子的先后顺序):Cu2+、H+(酸)、Ag+、H+(水)、Zn2+、活泼金属阳离子(Al3+~K+)2.案例分析:实验1实验2实验3装置CCAgNO3溶液CuFeCuSO4溶液CCKCl溶液阳极反应阴极反应总反应式——活动三:对比法研究电