第一章第二节物质的量教学目的2:1
巩固学习物质的量的相关知识,强化训练
重点学习配制一定物质的量浓度的溶液
教学课时:1
5课时知识体系25、物质的量、气体摩尔体积和物质的量浓度⑴物质的量(n)的单位是摩尔(mol)
把含有阿伏加德罗常数(约)个粒子的集体定义为1摩尔(1mol)
①阿伏加德罗常数(NA)与物质的量(n)的关系:※N==(N:微粒数)②摩尔质量(M)与物质的量(n)的关系:※m==(m:物质的质量)⑵气体摩尔体积(Vm):单位物质的量的任何气体在相同条件下占有的体积
单位是L/mol
①单位物质的量的任何气体在相同条件下占有的体积相等
推论1在标况下,任何气体1mol所占有的体积相等,约为L
推论2在相同条件下,任何等物质的量的气体所占有的体积相等,但不一定是22
②气体摩尔体积(Vm)与物质的量(n)的关系:※V==(V:气体的体积)⑶阿伏加德罗定律及应用①定义:在同温同压下,同体积的任何气体都含有相同数目的分子,这就是阿伏加德罗定律
②阿伏加德罗定律的应用同温同压下,任何气体的体积比等于气体的物质的量之比,即V1/V2==同温、定容时,任何气体的压强比等于气体的物质的量之比,即P1/P2==n1/n2同温同压下,任何气体的密度比等于它们的相对分子质量之比,即ρ1/ρ2==同温同压下,任何气体的质量比等于它们的相对分子质量之倒数比,即m1/m2=M1/M2同温、同压下,等质量的任何气体的体积比等于等于它们的相对分子质量之倒数比:V1/V2=M2/M1⑷物质的量浓度(c)即※cB==注意:⑴物质的量的科学表达,它的计算对象是微观粒子
⑵概念要清晰,分清楚物质的量、物质的质量、摩尔质量
⑶注意物理量的单位别混淆
⑷气体摩尔体积22
4L/mol是适用于标准状况下的气体
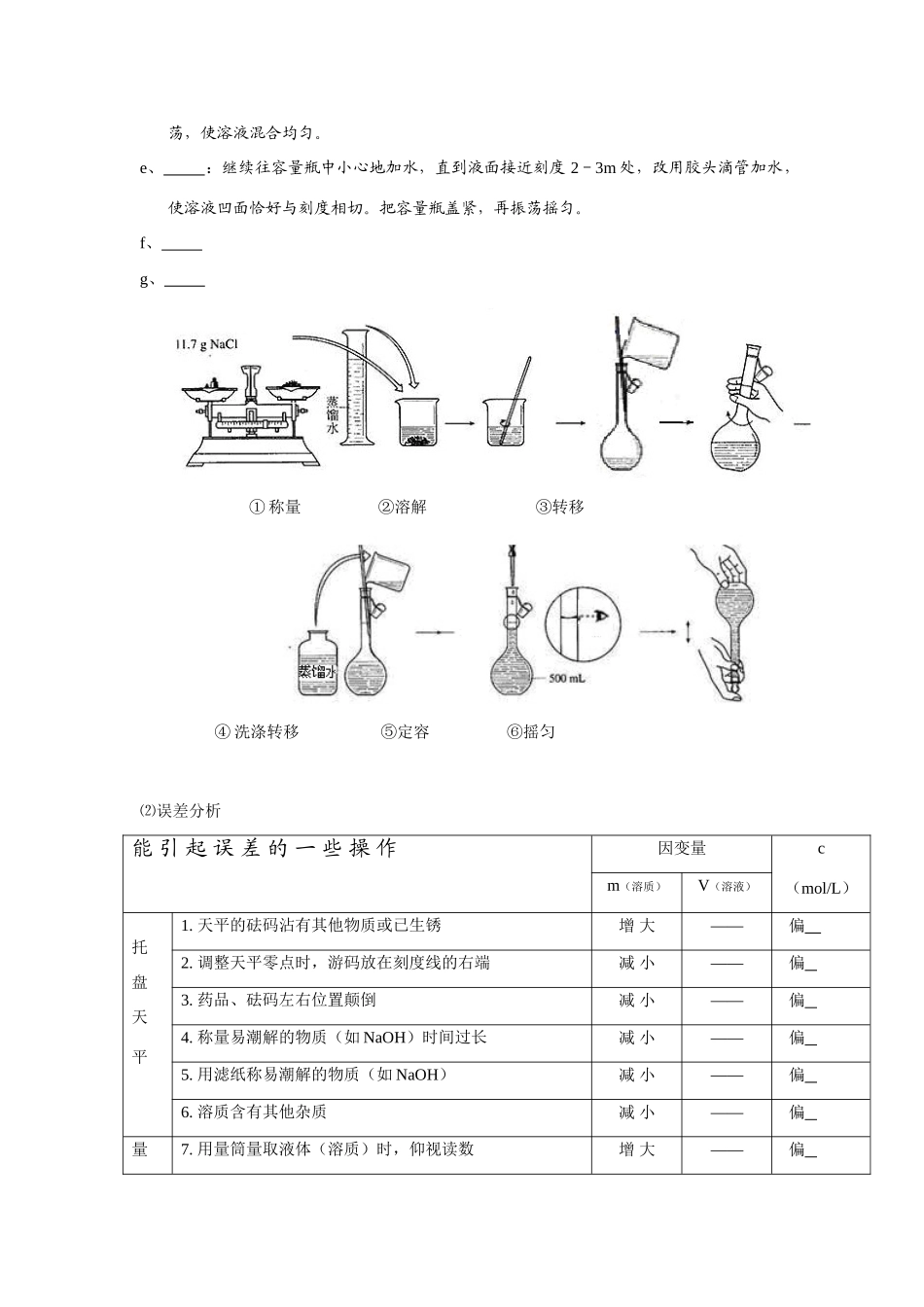
6、配制一定物质的量浓度的溶液(C)⑴配制步骤a、:算出固体溶质的质量或液体溶质