第3节元素周期表的应用第1课时认识同周期元素性质的递变规律1.以第3周期元素为例,掌握同周期元素的性质递变规律
(重点)2.了解原子结构、元素性质及该元素在周期表中的位置三者之间的关系
(重点)3.能运用原子结构理论初步解释同周期元素性质的递变规律
(难点)4.初步学会应用元素周期表进行物质推断
,钠、镁、铝三种金属元素原子失电子能力比较[基础·初探]1.钠、镁、铝与水或酸反应的实验探究2
钠、镁、铝最高价氧化物对应的水化物的碱性比较钠镁铝氢氧化物比较强碱中强碱两性氢氧化物碱性逐渐减弱结论失电子能力:钠>镁>铝[探究·升华][思考探究]1.在化学反应中,金属原子失电子越多,该金属的金属性越强,这句话正确吗
【提示】不正确
金属性强弱的比较,是比较原子失去电子的难易,而不是失去电子的多少
如化学反应中,Na失去一个电子,而Al失去三个电子,但Na的金属性比Al强
2.设计一个简单易行的实验说明锌的金属性比铜强
【提示】向CuSO4溶液中插入锌片,锌能置换出铜单质,说明金属性:Zn>Cu
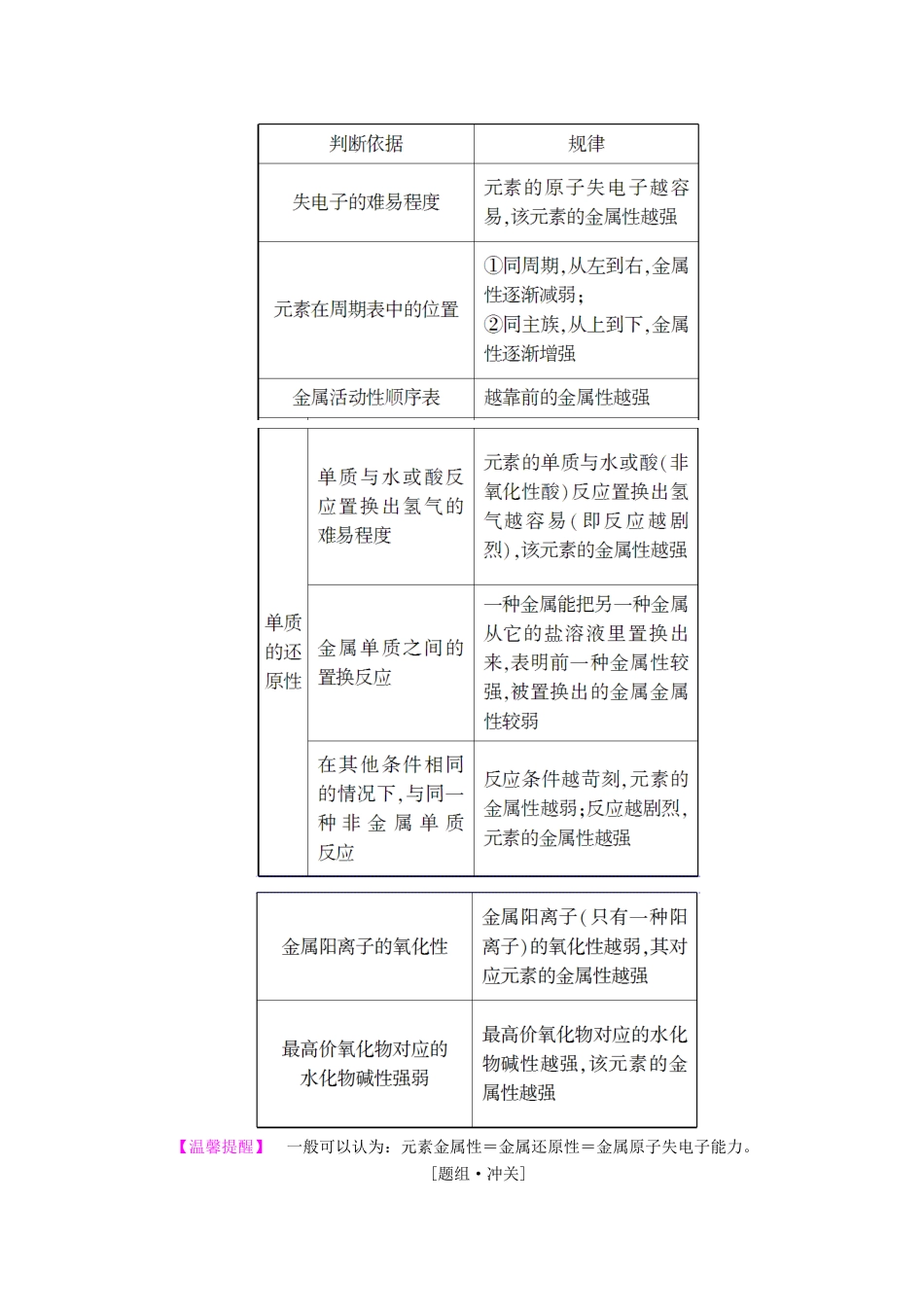
[认知升华]元素金属性强弱的判断方法【温馨提醒】一般可以认为:元素金属性=金属还原性=金属原子失电子能力
[题组·冲关]题组1金属性强弱的判断方法1.能证明Al的金属性比Mg弱的实验事实是()A.Al的导电性比Mg强B.Al的原子半径比Mg小C.Al(OH)3能溶于NaOH溶液,而Mg(OH)2不能D.Mg(OH)2的溶解性比Al(OH)3的溶解性略大【解析】C项说明碱性Mg(OH)2>Al(OH)3,因此可以证明Mg的金属性强于Al的金属性
【答案】C2.下列事实不能用于判断金属元素失电子能力强弱的是()A.金属间发生的置换反应B.1mol金属单质在反应中失去电子的多少C.金属元素的最高价氧化物对应水化物的碱性强弱D.金属元素的单质与水或酸置换出氢的难易【解析】活泼性强的金属能置