第1课时电解质的电离发展目标体系构建1
理解电离的概念,知道酸、碱、盐在水溶液中或熔融状态下会发生电离
建立电离与电解质概念之间的关联,知道酸、碱、盐都是电解质,能从电解质电离的角度认识酸、碱、盐具有的一般性质
初步判断电解质在水溶液中的电离结果,能书写电离方程式
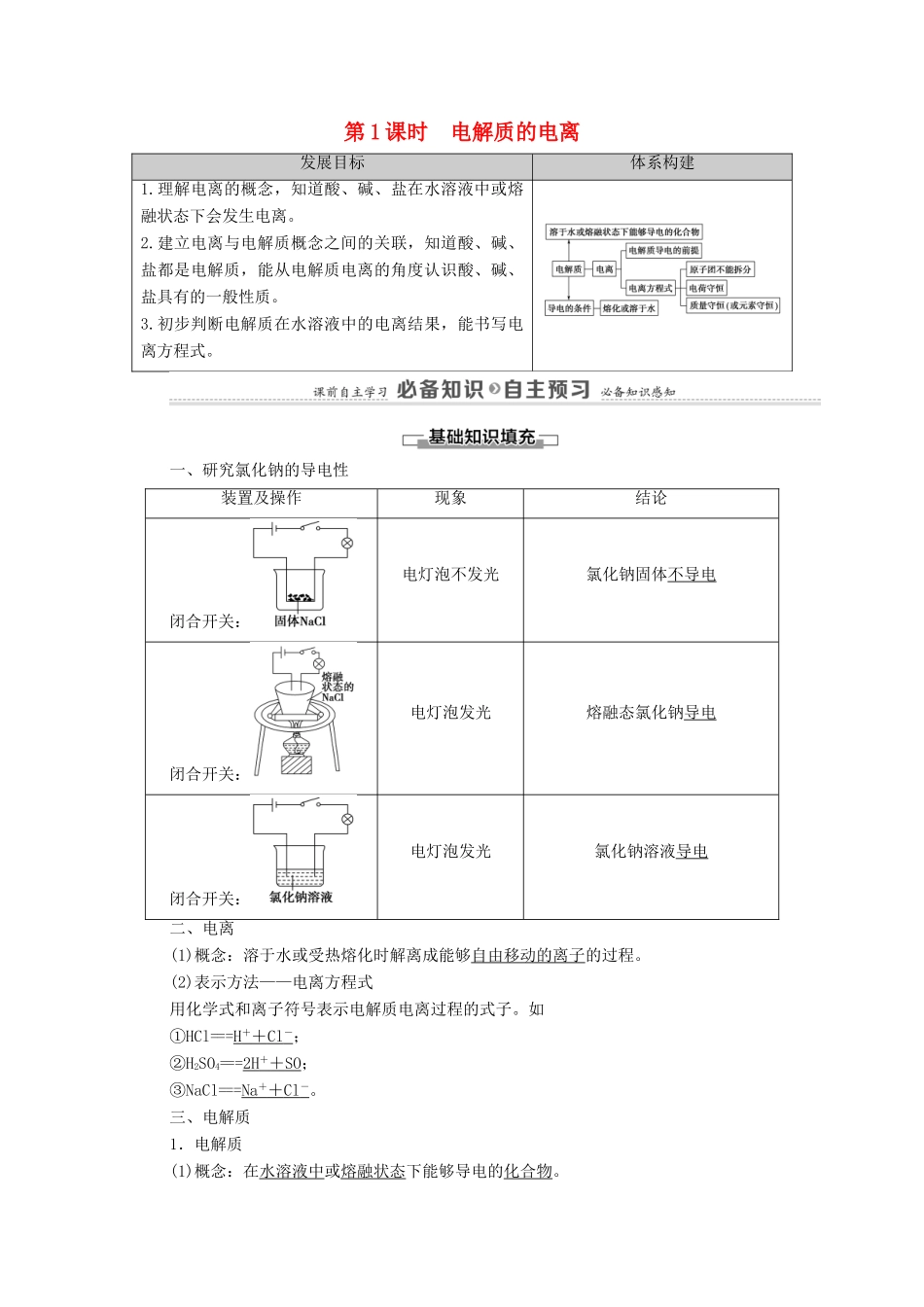
一、研究氯化钠的导电性装置及操作现象结论闭合开关:电灯泡不发光氯化钠固体不导电闭合开关:电灯泡发光熔融态氯化钠导电闭合开关:电灯泡发光氯化钠溶液导电二、电离(1)概念:溶于水或受热熔化时解离成能够自由移动的离子的过程
(2)表示方法——电离方程式用化学式和离子符号表示电解质电离过程的式子
如①HCl===H++Cl-;②H2SO4===2H++SO;③NaCl===Na++Cl-
三、电解质1.电解质(1)概念:在水溶液中或熔融状态下能够导电的化合物
(2)常见物质:酸、碱、盐等
微点拨:(1)电解质都必须是化合物
(2)电解质导电的条件是溶于水或熔融状态,二者具备其一即可
2.从电离的角度认识酸、碱、盐项目酸碱盐定义电离时生成的阳离子全部是H+的化合物电离时生成的阴离子全部是OH-的化合物电离时能生成金属阳离子(或NH)和酸根离子的化合物实例HCl、H2SO4、H2CO3等NaOH、KOH、NH3·H2O等Na2SO4、KCl、BaCO3、NaHCO3等3
强电解质(1)定义:在水溶液中能完全电离的电解质
(2)常见物质:强酸、强碱、大部分盐
(3)电离方程式强电解质的电离方程式用“===”,如H2SO4:H2SO4===2H++SO;KOH:KOH===K++OH-
4.弱电解质(1)定义:在水溶液中部分电离的电解质
(2)常见物质:弱酸、弱碱、水
(3)电离方程式弱电解质的电离方程式用“”,如CH3COOH:CH3COOHCH3COO-+H+,NH3·H2O:NH3·H2ONH+OH-
1.判断正误