第2课时研究同主族元素的性质课程标准核心素养1
以ⅠA、ⅦA族为例,掌握同主族元素性质的递变规律
能运用原子结构理论初步解释同主族元素性质的递变规律
宏观辨识与微观探析建立原子结构、元素性质与物质性质之间的认识模型
证据推理与模型认知构建“位”“构”“性”关系认识模型,发展对元素及其化合物化学性质的认识模型
科学探究与创新意识形成实验探究元素性质递变规律、比较物质性质的思路方法,提高基于理论进行预测、提出假设的能力和基于实验事实概括、推理得出结论的能力
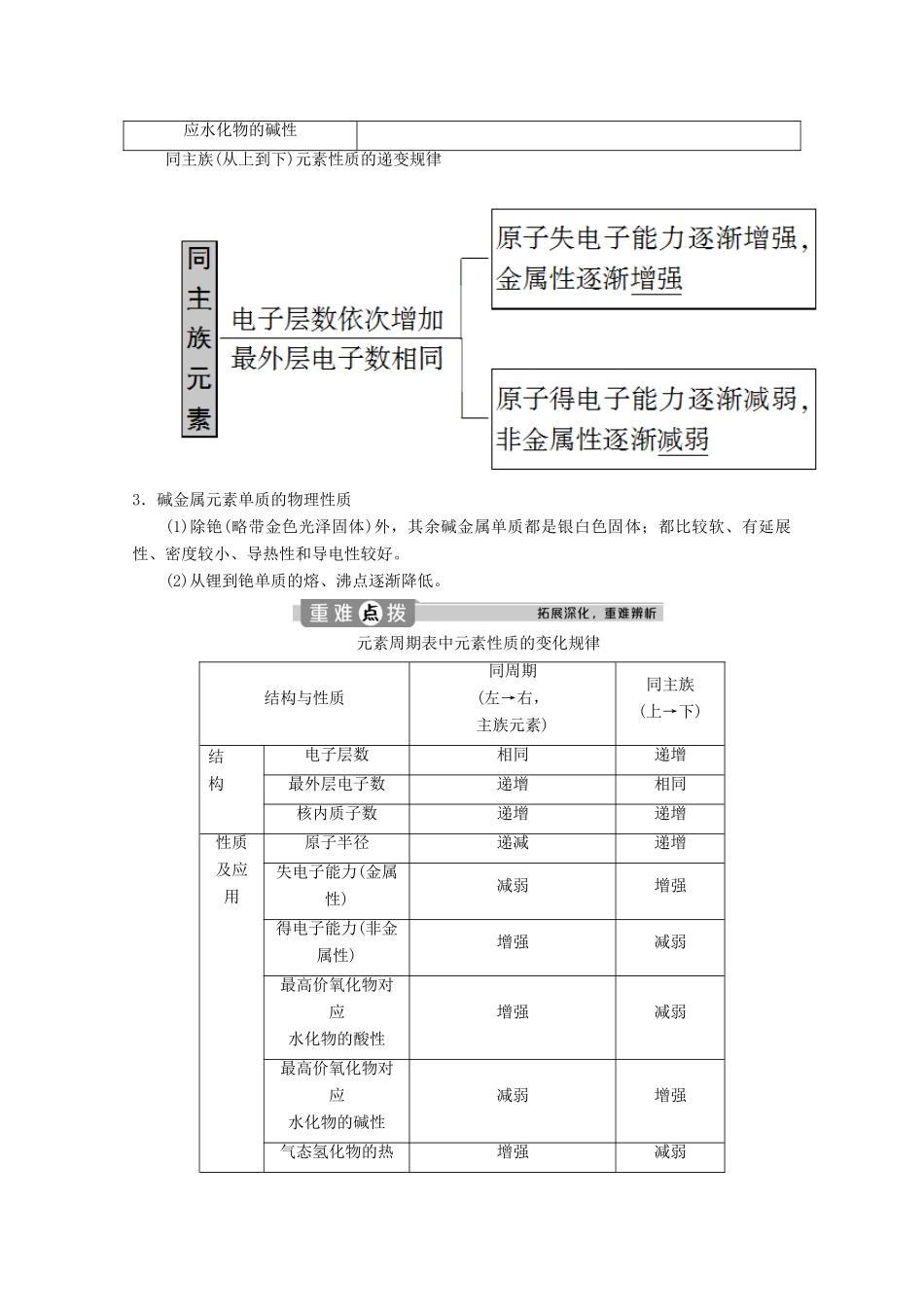
碱金属元素的原子结构与性质碱金属元素原子结构和性质的相似性与递变性(1)(2)递变性结构和性质递变规律原子半径――→单质的还原性――→与H2O或O2反应的剧烈程度――→最高价氧化物对――→应水化物的碱性同主族(从上到下)元素性质的递变规律3.碱金属元素单质的物理性质(1)除铯(略带金色光泽固体)外,其余碱金属单质都是银白色固体;都比较软、有延展性、密度较小、导热性和导电性较好
(2)从锂到铯单质的熔、沸点逐渐降低
元素周期表中元素性质的变化规律结构与性质同周期(左→右,主族元素)同主族(上→下)结构电子层数相同递增最外层电子数递增相同核内质子数递增递增性质及应用原子半径递减递增失电子能力(金属性)减弱增强得电子能力(非金属性)增强减弱最高价氧化物对应水化物的酸性增强减弱最高价氧化物对应水化物的碱性减弱增强气态氢化物的热增强减弱稳定性气态氢化物的还原性减弱增强铯(钫是放射性元素,不予考虑)是最活泼的金属元素;ⅠA族中碱金属元素不包括氢
1.判断正误(1)金属性:Li>Na>K>Rb
()(2)碱性:LiOH>NaOH>KOH>RbOH
()(3)稳定性:NH3>PH3,还原性:SiH4>CH4
()(4)酸性:HNO3Cl->S2-
()答案:(1)×(2)×(3)√(4)×(5)×2.下列关于碱金属元素的说法