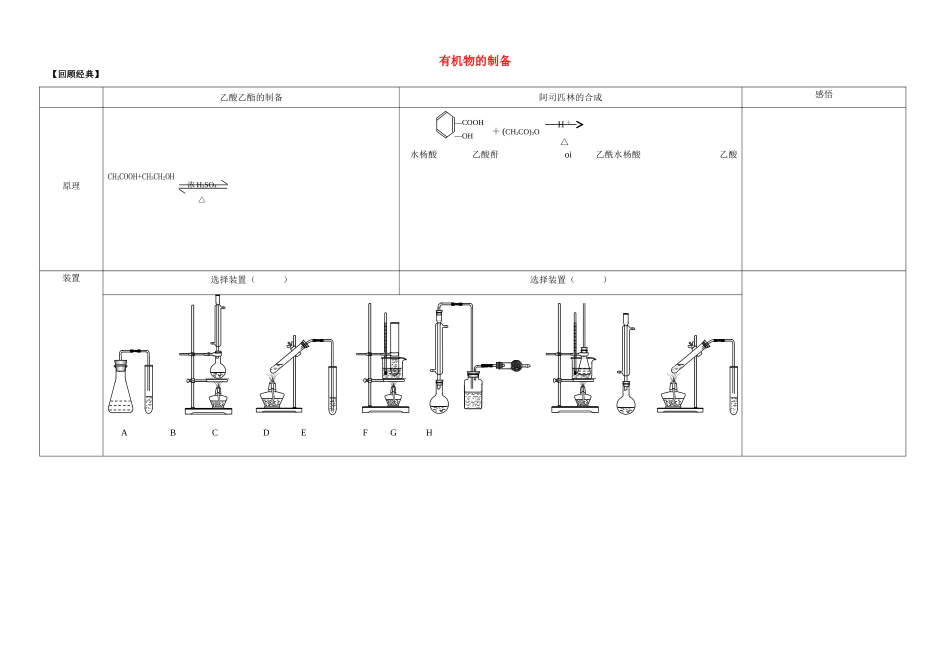
有机物的制备【回顾经典】乙酸乙酯的制备阿司匹林的合成感悟原理CH3COOH+CH3CH2OH装置选择装置()选择装置()浓H2SO4△水杨酸乙酸酐oi乙酰水杨酸乙酸H+△—COOH—OH+(CH3CO)2OABCDEFGH杂质(及来源)分离提纯(操作及操作注意事项)请回答下列问题:1.接收产物的装置中装的试剂为:_____________________________2.该试剂的作用:___________________________________________________________________________________________________________________________________________________________________3.获得产品的操作为:___________________________________________________________________________________________________某同学用如下流程提纯产品,根据要求回答问题:1.加入试剂1后发生反应的化学方程式:___________________________________________________________2.试剂2的作用:__________________________________________3.操作1为:______________________________________________纯度分析如何检验酸性杂质除尽:______________________________________2
000g水杨酸与足量其它原料,最后得到1
566g产品,则产率为:____________乙酰水杨酸粗产品沉淀产品试剂1过滤滤液试剂2操作1_【感