课题:第二节几种重要的金属化合物(第3课时)学习目标1.掌握铁的氧化物、氢氧化物的主要性质及氢氧化物的制法2.掌握Fe3+的检验及氧化性3.明确Fe2+与Fe3+的相互转化学习重点三价铁的氧化性及Fe、Fe2+、Fe3+的转化、氢氧化亚铁的制备和性质学习难点三价铁的氧化性及Fe、Fe2+、Fe3+的转化学法指导1、通过学习学会运用观察、实验等手段获取信息,并运用分类、比较、归纳等方法对信息进行加工
2、初步学会通过探究性实验,使自己进一步掌握应用实验,探究研究物质性质的科学探究方法
使自己敢于质疑、勤于思考、逐步形成独立思考的能力
铁在地壳中的含量仅次于、和,居第位,主要以和化合物形式存在
铁在空气中容易,因为不能保护内层金属3
你知道铁的哪些化合物
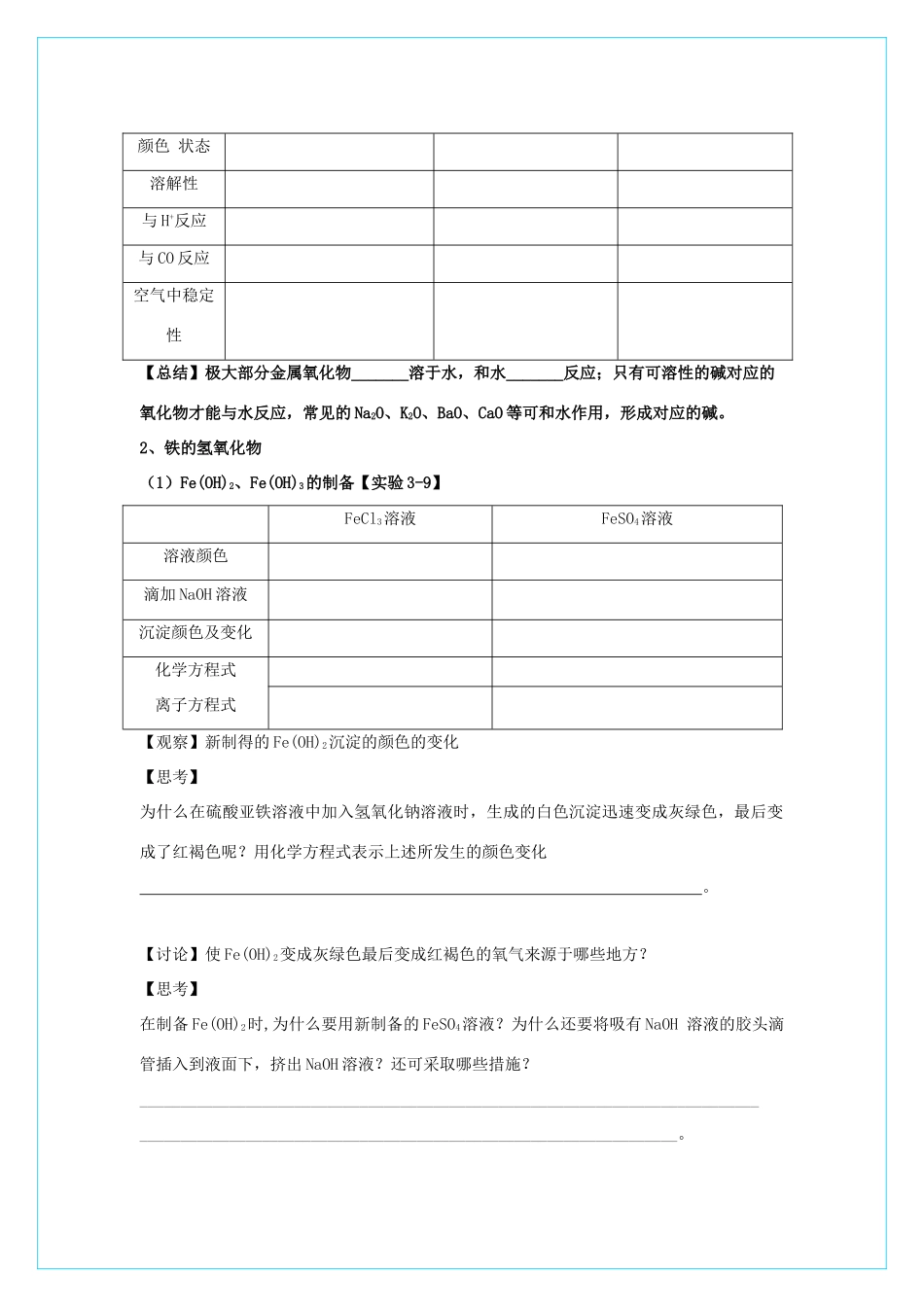
回顾前面所学分类方法的知识,铁的化合物可以分为哪几类自主梳理三、铁的重要化合物1、铁的氧化物名称氧化亚铁氧化铁四氧化三铁俗名―――――――――――化学式铁的化合价颜色状态溶解性与H+反应与CO反应空气中稳定性【总结】极大部分金属氧化物_______溶于水,和水_______反应;只有可溶性的碱对应的氧化物才能与水反应,常见的Na2O、K2O、BaO、CaO等可和水作用,形成对应的碱
2、铁的氢氧化物(1)Fe(OH)2、Fe(OH)3的制备【实验3-9】FeCl3溶液FeSO4溶液溶液颜色滴加NaOH溶液沉淀颜色及变化化学方程式离子方程式【观察】新制得的Fe(OH)2沉淀的颜色的变化【思考】为什么在硫酸亚铁溶液中加入氢氧化钠溶液时,生成的白色沉淀迅速变成灰绿色,最后变成了红褐色呢
用化学方程式表示上述所发生的颜色变化
【讨论】使Fe(OH)2变成灰绿色最后变成红褐色的氧气来源于哪些地方
【思考】在制备Fe(OH)2时,为什么要用新制备的FeSO4溶液
为什么还要将吸有NaOH溶液的胶头滴管插入到液面下,挤出Na