《高中化学高考第一轮模块复习——基本概念和基本理论》专题一物质的组成、性质和分类【课标要求】1.理解物理变化与化学变化的区别与联系
2.理解混合物和纯净物、单质和化合物、金属和非金属的概念
3.理解酸、碱、盐、氧化物的概念及其相互联系
【提前预习】一.物质的分类及转化1、物质的性质(1)物理性质:不需要发生化学反应所表现出来的性质,如:颜色、状态、气味、熔点、沸点、硬度、密度、导电、导热、溶解性等
(2)化学性质:在化学反应中所表现出来的性质
如:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性等
(3)物理变化与化学变化的本质区别是前者没有新物质生成,后者生成了新的物质
物质发生物理变化时不一定发生了化学变化,但发生化学变化时一定伴随着物理变化
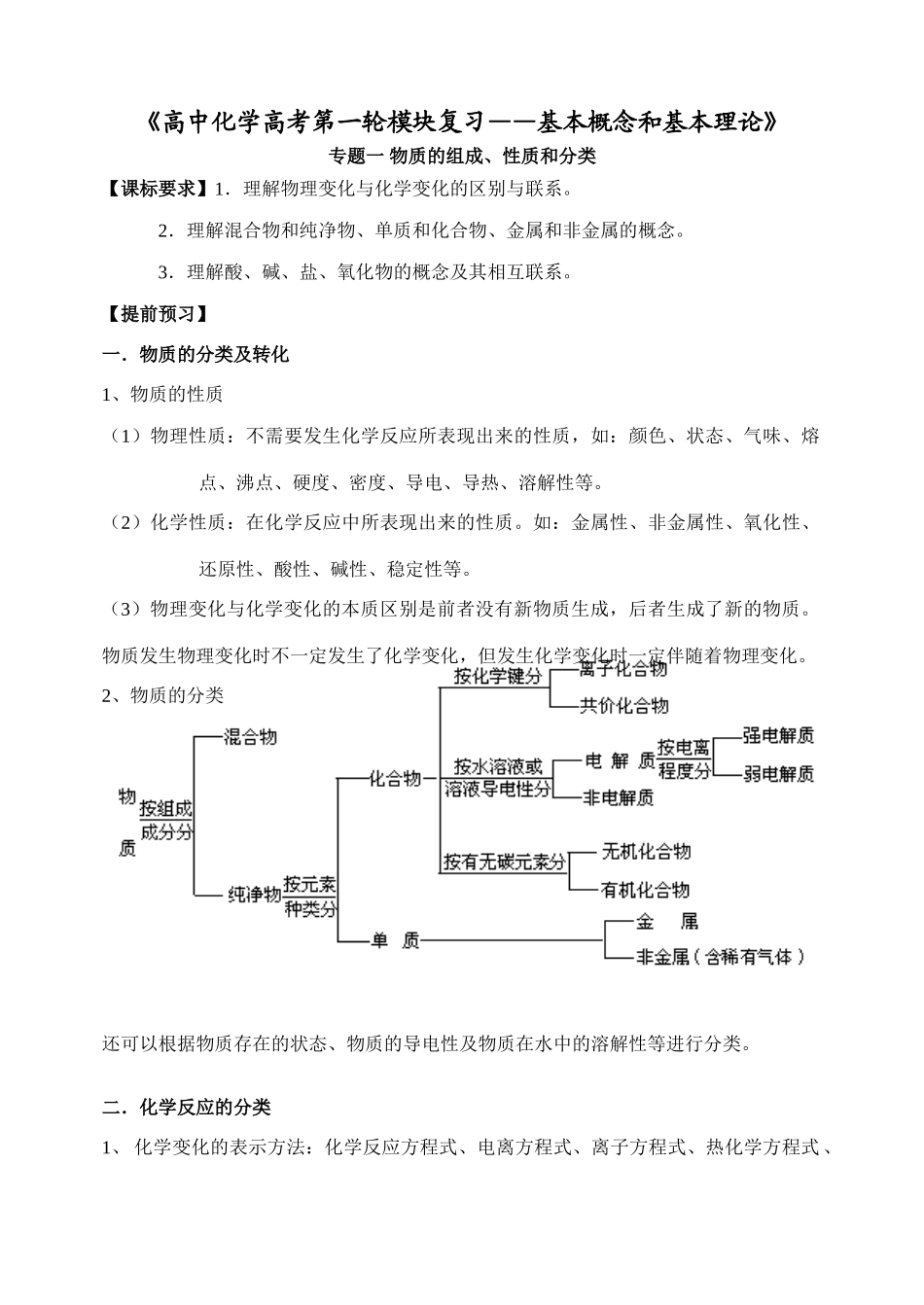
2、物质的分类还可以根据物质存在的状态、物质的导电性及物质在水中的溶解性等进行分类
二.化学反应的分类1、化学变化的表示方法:化学反应方程式、电离方程式、离子方程式、热化学方程式、电极方程式、电池反应、电解反应、水解反应等2、化学反应分类:按反应物、生成物组成形式变化可分为:化合、分解、置换、复分解,按电子转移可分为:氧化—还原反应、非氧化—还原反应,按是否有离子参加可分为:离子反应、非离子反应按反应的程度可分为:可逆反应、不可逆反应,按反应的热效应可分为:吸热反应、放热反应
有机化合物之间的反应还可以按反应机理分为取代反应、加成反应、氧化反应、聚合反应、酯化反应、消去反应等
【例题1】1.只含有一种元素的物质一定是纯净物吗
2.盐一定含有金属元素吗
3.金属氧化物一定是碱性氧化物吗
碱性氧化物一定是金属氧化物吗
4.非金属氧化物一定是酸性氧化物吗
酸性氧化物一定是非金属氧化物吗
5.Na2CO3·10H2O、盐酸是混合物还是纯净物
【例题2】下列物质:金属铁、金属锌、木炭、CuO、CaCO3、H2SO4、NaOH、Ba(OH