浙江省重点中学协作体2015届高考化学模拟试卷(二)一、选择题:本大题共7小题,每小题6分
在每小题给出的四个选项中,只有一项是符合题目要求的
1.(6分)对于工农业生产和日常生活中与化学有关的问题,下列认识不正确的是()A.含有氯化钠融雪剂的使用会加快桥梁的腐蚀B.铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获取铝C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅D.高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机2.(6分)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其电子层数的倍,Y是地壳中含量最高的金属元素,Z、W与Y同周期且互不相邻.下列叙述正确的是()A.X与氧气反应可生成不止一种氧化物B.原子半径:W>Z>Y>XC.气态氢化物稳定性:HmZ>HnWD.W位于第3周期第ⅦA族3.(6分)己烯雌酚是一种激素类药物,其结构简式如图所示.下列有关叙述中不正确的是()A.己烯雌酚的分子式为C18H20O2B.己烯雌酚分子中一定有16个碳原子共平面C.己烯雌酚为芳香族化合物D.己烯雌酚可发生加成、取代、氧化、加聚、酯化、硝化反应4.(6分)如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0
5mol/L,工作一段时间后,测得有0
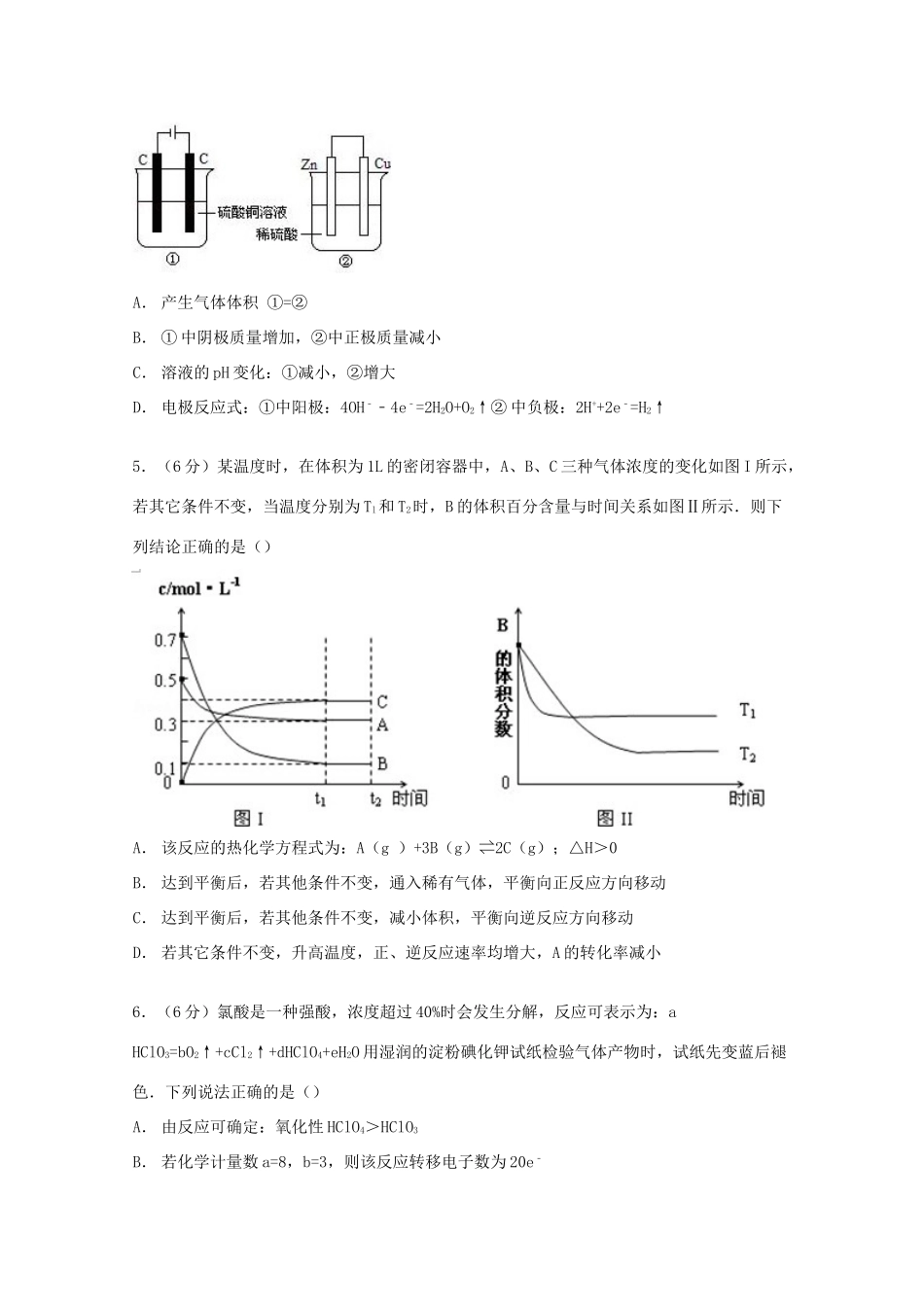
02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是()A.产生气体体积①=②B.①中阴极质量增加,②中正极质量减小C.溶液的pH变化:①减小,②增大D.电极反应式:①中阳极:4OH﹣﹣4e﹣=2H2O+O2↑②中负极:2H++2e﹣=H2↑5.(6分)某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是()A.该反应的热化学方