酸碱盐——计算1
(05云南)为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:第一次第二次第三次第四次第五次加入稀硫酸的质量/g1010101010剩余固体质量/g8
6请认真分析表中的数据,回答下列问题:(1)表示样品与稀硫酸恰好完全反应的是上表中第_________次操作;(2)计算样品中锌的质量分数;(3)计算实验中所用稀硫酸的溶质质量分数
(05北京)将15gCaCl2溶液逐滴加入到20gNa2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量,其关系如下图所示
请根据题意计算:(1)CaCl2溶液与Na2CO3溶液中溶质的质量分数之比
(2)将反应后的物质过滤,蒸干滤液后得到固体的质量
(05黑龙江)硫酸厂排放的污水中通常含有硫酸杂质
为测定污水中硫酸的溶质质量分数做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示
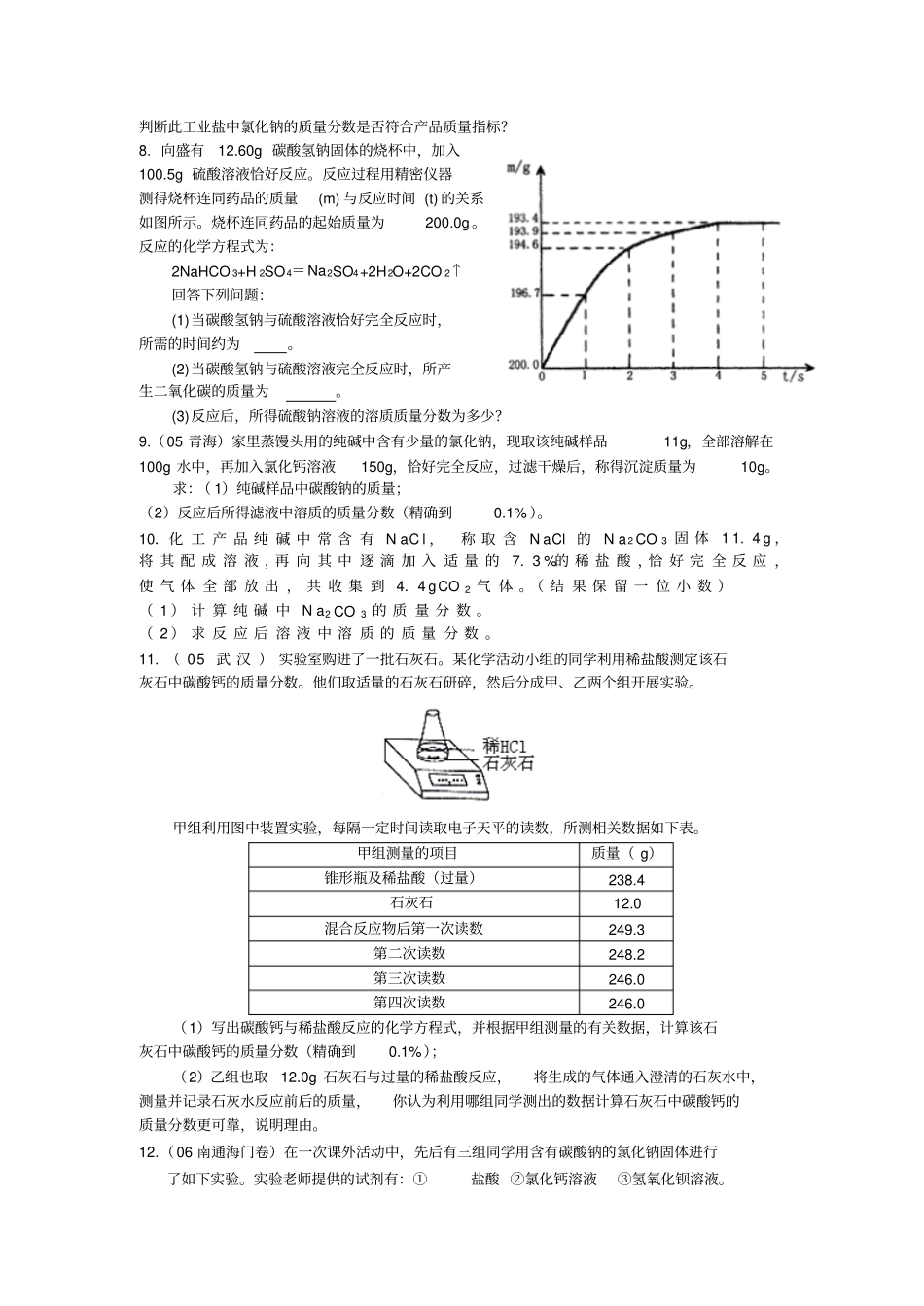
请根据实验计算,该污水中硫酸的溶质质量分数是多少
(05南通海门)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定
取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g
计算废水中盐酸的溶质质量分数
测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究
(1)配制100mL10%的盐酸(密度为1
05g/cm3)
他们应量取38%的盐酸(密度为1
19g/cm3)多少毫升
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸
有关实验中的数据记录如下:试在坐标系中绘出溶液温度变化与加入盐酸体积之间的变化关系图