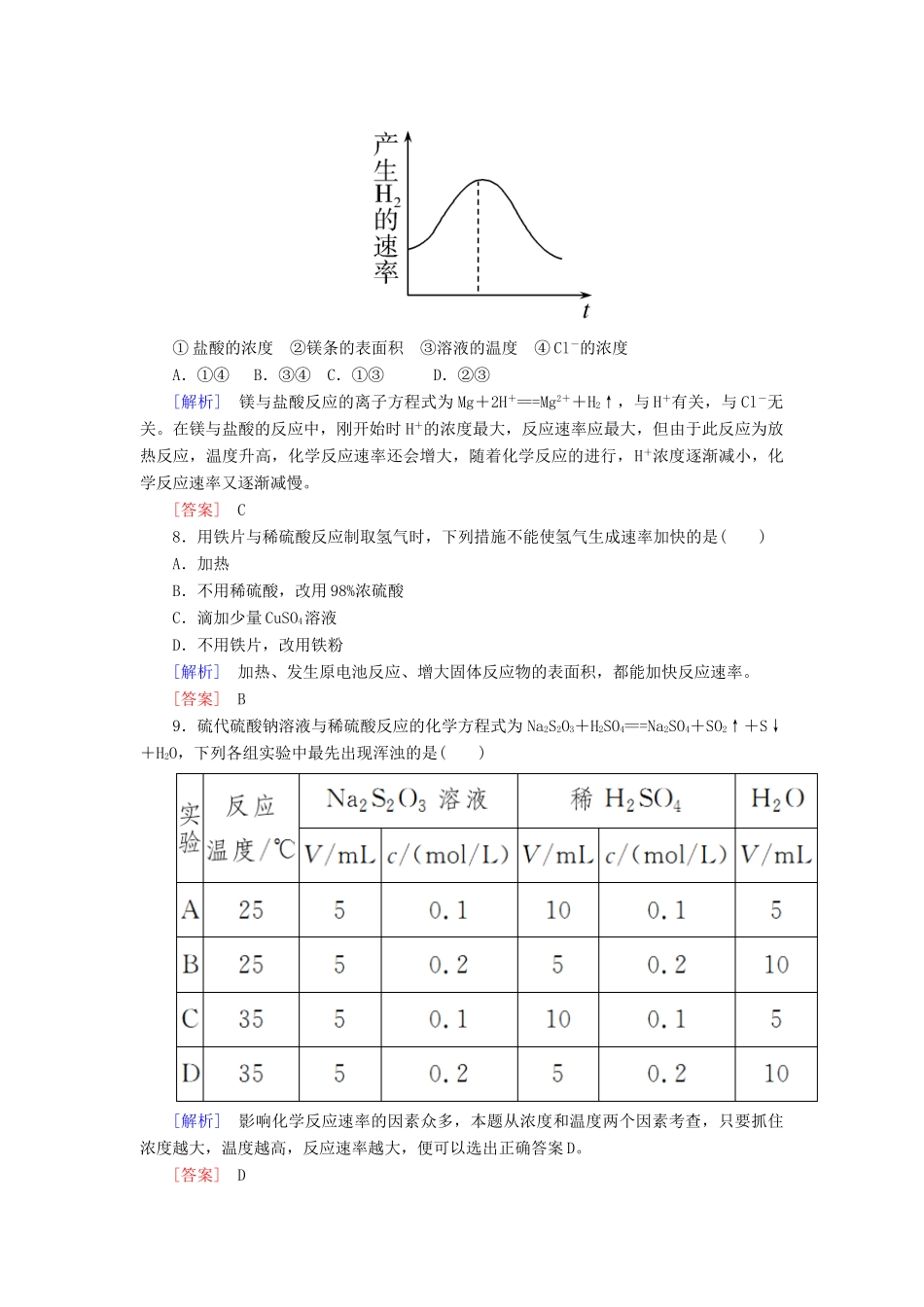
课后作业(十一)[基础巩固]一、化学反应速率1.下列关于化学反应速率的说法中,正确的是()A.化学反应速率是指一定时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加B.化学反应速率为“0.8mol·L-1·s-1”,所表示的意思是时间为1s时,某物质的浓度为0.8mol·L-1C.根据化学反应速率的大小可以知道化学反应进行的快慢D.对于任何化学反应来说,反应速率越大,反应现象越明显[解析]化学反应速率是指单位时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加,A错误;化学反应速率为“0.8mol·L-1·s-1”,所表示的意思是1s内,某物质的浓度改变量为0.8mol·L-1,B错误;有的化学反应发生时无现象,即使反应速率很快,反应现象也不明显,如NaOH溶液与盐酸的反应,D错误。[答案]C2.在反应C(s)+CO2(g)2CO(g)中,不可能使反应速率明显增大的措施是()A.增大压强B.升高温度C.增大CO2的浓度D.增加碳的量[解析]增大压强、升高温度、增大CO2的浓度均能增大反应速率;增加固体的用量,因其浓度是常数,故反应速率不会增加,选D。[答案]D3.反应4A(g)+5B(g)===4C(g)+6D(g)在5L的密闭容器中进行,半分钟后,C的物质的量增加了0.3mol。下列叙述正确的是()A.容器中D的物质的量至少为0.45molB.A的平均反应速率是0.01mol·L-1·s-1C.容器中A、B、C、D的物质的量之比一定是4∶5∶4∶6D.容器中A的物质的量一定增加了0.3mol[解析]半分钟后,C的物质的量增加了0.3mol,则根据方程式可知半分钟内一定同时生成0.45molD,由于不能确定反应前D的物质的量,因此容器中D的物质的量至少为0.45mol,A项正确;半分钟后,C的物质的量增加了0.3mol,则根据方程式可知一定同时消耗0.3molA,则A的平均反应速率是=0.002mol·L-1·s-1,B项错误;由于不能确定反应前各物质的物质的量,因此容器中A、B、C、D的物质的量之比不一定是4∶5∶4∶6,C项错误;容器中A的物质的量一定减少0.3mol,D项错误。[答案]A4.在2A(g)+B(g)3C(g)+4D(g)反应中,表示该反应速率最快的是()A.v(A)=0.5mol·L-1·s-1B.v(B)=0.3mol·L-1·s-1C.v(C)=0.8mol·L-1·s-1D.v(D)=6mol·L-1·min-1[解析]正确的思路应是根据反应速率与化学方程式中化学计量数之间的关系将各物质的反应速率转化为用同一种物质表示的速率。A项中据v(A)推知v(B)=0.25mol·L-1·s-1,C项中据v(C)推出v(B)≈0.27mol·L-1·s-1,D项中将时间单位换算为s,v(D)=0.1mol·L-1·s-1,据v(D)推出v(B)=0.025mol·L-1·s-1,故反应速率最快的是B选项。[答案]B二、影响化学反应速率的因素5.反应3Fe(s)+4H2O(g)=====Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是()A.增加铁的量B.将容器体积缩小一半C.升高温度D.压强不变,充入N2使容器体积增大[解析]A项,由于Fe是固体,其浓度不改变,增加铁的量,化学反应速率不变,正确;B项,将容器体积缩小一半,物质的浓度增大,体系的压强增大,反应速率加快,错误;C项,升高温度,化学反应速率加快,错误;D项,压强不变,充入N2使容器体积增大,反应物的浓度减小,化学反应速率减小,错误。[答案]A6.通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和生活质量的提高。下列各图所示的措施中,是为了增大化学反应速率的是()[解析]A项为防止铁门生锈,B项为防止橡胶老化,D项为防止木头腐烂,三者均为了减慢化学反应速率;C项是为了使炉火更旺,加快化学反应速率。[答案]C7.把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的是()①盐酸的浓度②镁条的表面积③溶液的温度④Cl-的浓度A.①④B.③④C.①③D.②③[解析]镁与盐酸反应的离子方程式为Mg+2H+===Mg2++H2↑,与H+有关,与Cl-无关。在镁与盐酸的反应中,刚开始时H+的浓度最大,反应速率应最大,但由于此反应为放热反应,温度升高,化学反应速率还会增大,随着化学反应的进行,H+浓度逐渐减小,化学反应速率又逐渐减慢。[答案]C8.用铁片与稀硫酸反应制取...