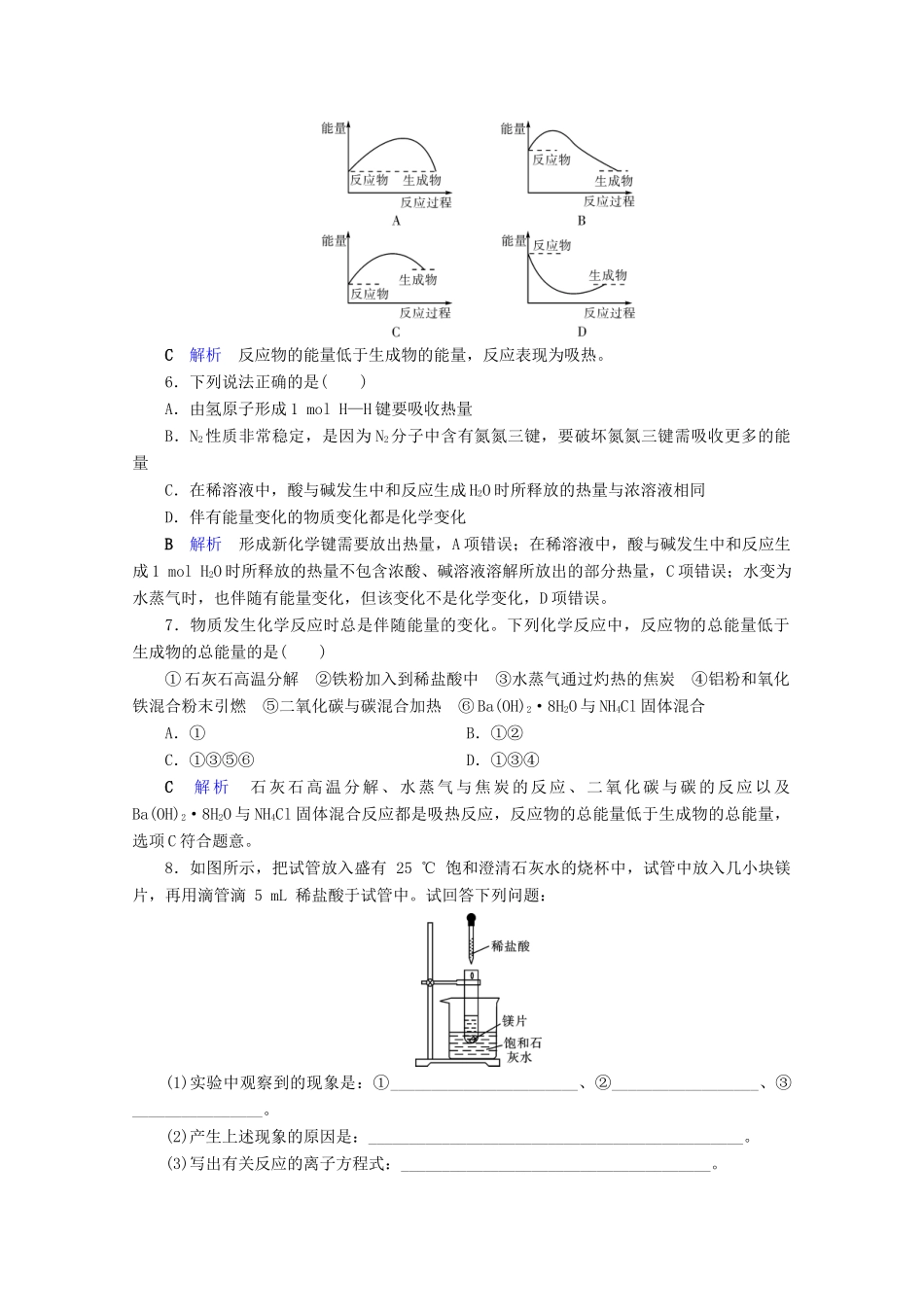
第1节化学能与热能考点对应题号基本目标发展目标1.反应热概念与能源1,2,32.放热反应和吸热反应判断4,5,711,133.反应热与物质能量、键能关系610,144.综合应用8,912,15[基本目标]1.我国科学家最近指出:2050年后全球将出现的四大能源是:①氢能②天然气水合物③空间太阳能发电④氚和氦-3的核聚变。这四大能源未来在提供能量过程中会产生新核素的是()A.①B.②C.③D.④D解析④发生的是原子核的变化,有新核素生成,其余都只发生了化学变化。2.下列有关能量转换的说法正确的是()A.煤燃烧生成CO2是热能转化为化学能的过程B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程B解析本题考查了自然界中能量的转化方式。煤燃烧是炭和氧气中的化学能转化为热能,同时生成新物质二氧化碳,A项错误;动物体内葡萄糖的氧化是化学能转化为其他形式的能量,C项错误;光合作用是太阳能转化为化学能的过程,D项错误。3.下列说法中,正确的是()A.干冰升华时要吸收热量,所以这是吸热反应B.加热后才能发生的反应一定是吸热反应C.1molBa(OH)2与1molH2SO4反应吸收的热量为QD.可燃物的燃烧都是放热反应D解析干冰升华吸收热量克服分子间作用力,是物理过程,A项错误;有些放热反应也要加热,B项错误;Ba(OH)2与H2SO4的反应为中和反应,应释放热量。4.下列反应中,既属于氧化还原反应,同时又是吸热反应的是()A.灼热的炭与CO2反应B.H2在O2中燃烧的反应C.铝与稀盐酸反应D.Ba(OH)2·8H2O与NH4Cl反应A解析A、B、C项是氧化还原反应,B、C项是放热反应,A项是吸热反应;D项是吸热反应,但不是氧化还原反应。5.如图表示吸收能量反应的图像是()C解析反应物的能量低于生成物的能量,反应表现为吸热。6.下列说法正确的是()A.由氢原子形成1molH—H键要吸收热量B.N2性质非常稳定,是因为N2分子中含有氮氮三键,要破坏氮氮三键需吸收更多的能量C.在稀溶液中,酸与碱发生中和反应生成H2O时所释放的热量与浓溶液相同D.伴有能量变化的物质变化都是化学变化B解析形成新化学键需要放出热量,A项错误;在稀溶液中,酸与碱发生中和反应生成1molH2O时所释放的热量不包含浓酸、碱溶液溶解所放出的部分热量,C项错误;水变为水蒸气时,也伴随有能量变化,但该变化不是化学变化,D项错误。7.物质发生化学反应时总是伴随能量的变化。下列化学反应中,反应物的总能量低于生成物的总能量的是()①石灰石高温分解②铁粉加入到稀盐酸中③水蒸气通过灼热的焦炭④铝粉和氧化铁混合粉末引燃⑤二氧化碳与碳混合加热⑥Ba(OH)2·8H2O与NH4Cl固体混合A.①B.①②C.①③⑤⑥D.①③④C解析石灰石高温分解、水蒸气与焦炭的反应、二氧化碳与碳的反应以及Ba(OH)2·8H2O与NH4Cl固体混合反应都是吸热反应,反应物的总能量低于生成物的总能量,选项C符合题意。8.如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中放入几小块镁片,再用滴管滴5mL稀盐酸于试管中。试回答下列问题:(1)实验中观察到的现象是:①_______________________、②__________________、③________________。(2)产生上述现象的原因是:______________________________________________。(3)写出有关反应的离子方程式:______________________________________。(4)由实验推知,生成的MgCl2和H2的总能量________(填“大于”“小于”或“等于”)参加反应的镁片和盐酸的总能量。解析镁片与盐酸的反应是放热反应,是由于反应物(Mg和盐酸)的总能量高于生成物(MgCl2和H2)的总能量。放出的热通过小试管传递给饱和石灰水溶液,使石灰的溶解度下降而析出Ca(OH)2晶体。答案(1)①镁片上有大量气泡产生;②参加反应的镁片逐渐溶解;③烧杯中溶液变浑浊(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体(3)Mg+2H+===Mg2++H2↑(4)小于9.为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液...