专题17化学平衡状态考点一化学平衡状态与化学反应进行的方向[考试标准]知识条目必考要求加试要求1
化学反应的限度ab2
化学平衡的概念ab3
化学平衡状态的特征ab4
自发反应的概念、熵变的概念a5
用熵变、焓变判断化学反应的方向c(一)化学平衡状态1.可逆反应在同一条件下既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应
2.化学平衡状态(1)概念一定条件下的可逆反应中,正反应速率与逆反应速率相等,反应体系中所有参加反应的物质的质量或浓度保持不变的状态
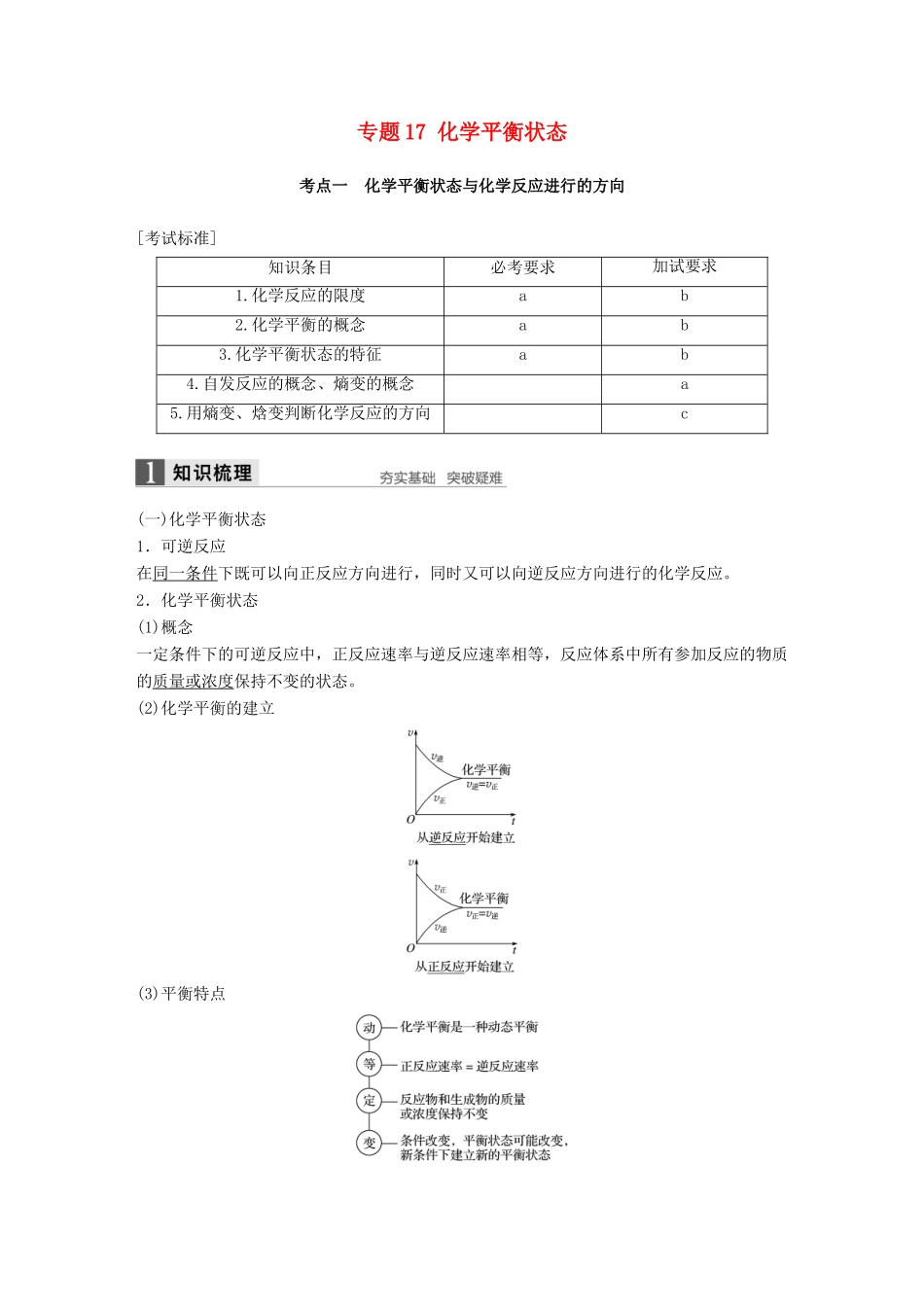
(2)化学平衡的建立(3)平衡特点(二)化学反应进行的方向(加试)1.自发过程(1)含义在一定温度和压强下,不需要借助外力作用就能自发进行的过程
(2)特点①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)
②在密闭条件下,体系有从有序转变为无序的倾向性(无序体系更加稳定)
2.自发反应在一定温度和压强下无需外界帮助就能自发进行的反应称为自发反应
3.判断化学反应方向的依据(1)焓变与反应方向研究表明,对于化学反应而言,绝大多数放热反应都能自发进行,且反应放出的热量越多,体系能量降低得也越多,反应越完全
可见,反应的焓变是制约化学反应能否自发进行的因素之一
(2)熵变与反应方向①研究表明,除了热效应外,决定化学反应能否自发进行的另一个因素是体系的混乱度
大多数自发反应有趋向于体系混乱度增大的倾向
②熵和熵变的含义a.熵的含义熵是衡量一个体系混乱度的物理量
用符号S表示
同一条件下,不同物质有不同的熵值,同一物质在不同状态下熵值也不同,一般规律是S(g)>S(l)>S(s)
b.熵变的含义熵变是反应前后体系熵的变化,用ΔS表示,化学反应的ΔS越大,越有利于反应自发进行
(3)综合判断反应方向的依据①ΔH-TΔS<0,反应能自发进行
②ΔH-TΔS=0,反应达到平衡状态
③ΔH-TΔS>0,反应不能自发