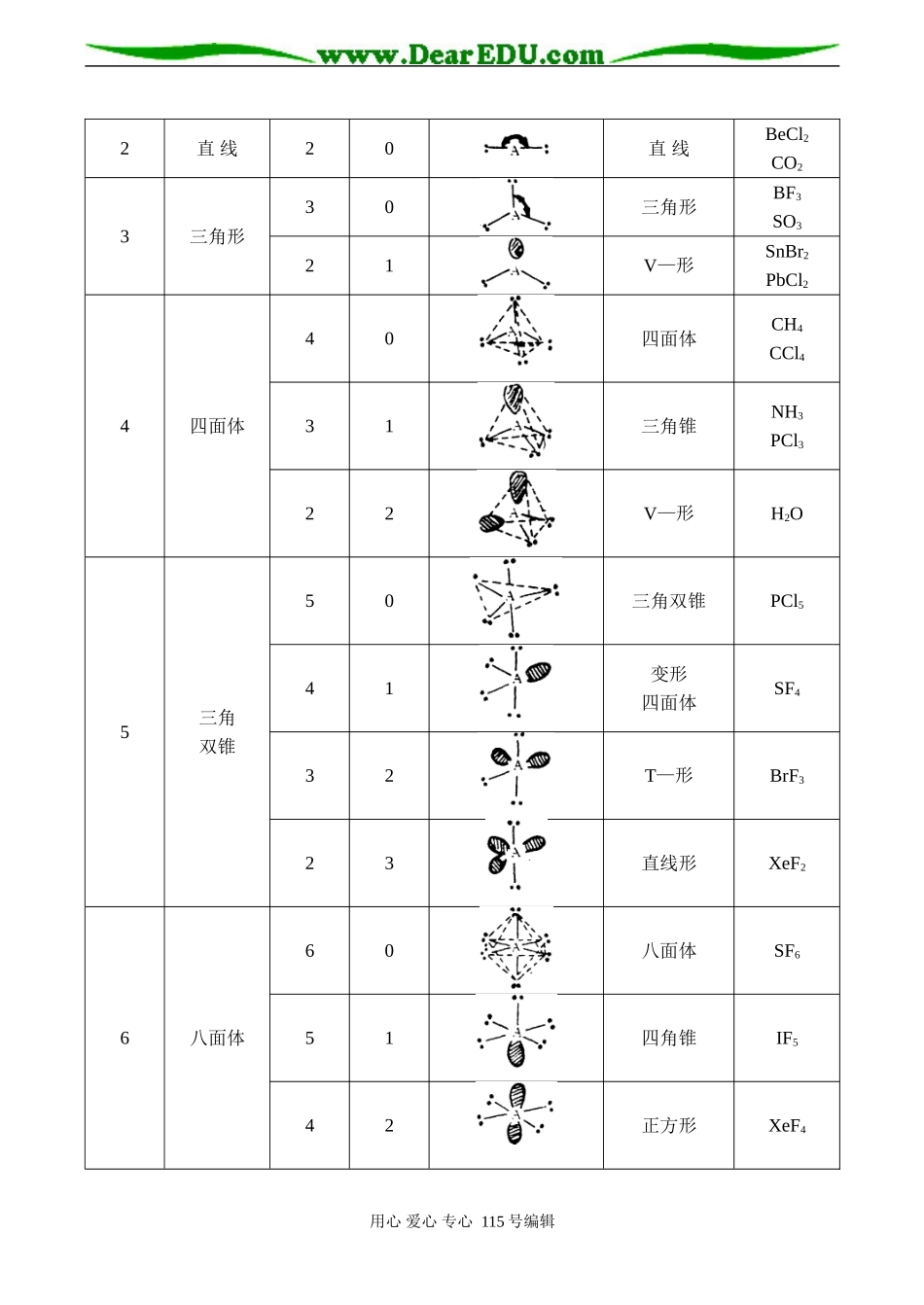
高一化学竞赛辅导价层电子对互斥理论(VSEPR)现代化学的重要基础之一是分子(包括带电荷的离子)的立体结构
实验测出,SO3分子是呈平面结构的,O—S—O的夹角等于120º,而SO32-离子却是呈三角锥体,硫是锥顶,三个氧原子是三个锥角,象一架撑开的照相用的三角架
又例如SO2的三个原子不在一条直线上,而CO2却是直线分子等等
价层电子对互斥理论用以预测简单分子或离子的立体结构,我们不难学会用这种理论来预测和理解分子或离子的立体结构,并用来进一步确定分子或离子的结构
价层电子对互斥理论认为,在一个共价分子中,中心原子周围电子对排布的几何构型主要决定于中心原子的价电子层中电子对的数目
所谓价层电子对包括成键的σ电子对和孤电子对
价层电子对各自占据的位置倾向于彼此分离得尽可能地远些,这样电子对彼此之间的排斥力最小,整个分子最为稳定
这样也就决定了分子的空间结构
也正因此,我们才可以用价层电子对很方便地判断分子的空间结构
例如:甲烷分子(CH4),中心原子为碳原子,碳有4个价电子,4个氢原子各有一个电子,这样在中心原子周围有8个电子,4个电子对,所以这4个电子对互相排斥,为了使排斥力最小,分子最稳定,它们只能按正四面体的方式排布
这样就决定了CH4的正四面体结构
利用VSEPR推断分子或离子的空间构型的具体步骤如下:①确定中心原子A价层电子对数目
中心原子A的价电子数与配位体X提供共用的电子数之和的一半,就是中心原子A价层电子对的数目
例如BF3分子,B原子有3个价电子,三个F原子各提供一个电子,共6个电子,所以B原子价层电子对数为3
计算时注意:(ⅰ)氧族元素(ⅥA族)原子作为配位原子时,可认为不提供电子(如氧原子有6个价电子,作为配位原子时,可认为它从中心原子接受一对电子达到8电子结构),但作为中心原子时,认为它提供所有的6个价电子
(ⅱ)如果讨论的是离子,则应加上或减去与离