专题6元素周期律元素周期表考点一元素周期律元素周期表[考试标准]知识条目必考要求加试要求1
元素周期表的结构,同主族、同周期元素原子核外电子排布、元素化学性质的递变规律bb2
元素周期律(核外电子排布、原子半径、元素主要化合价、元素的金属性和非金属性的周期性变化)bb3
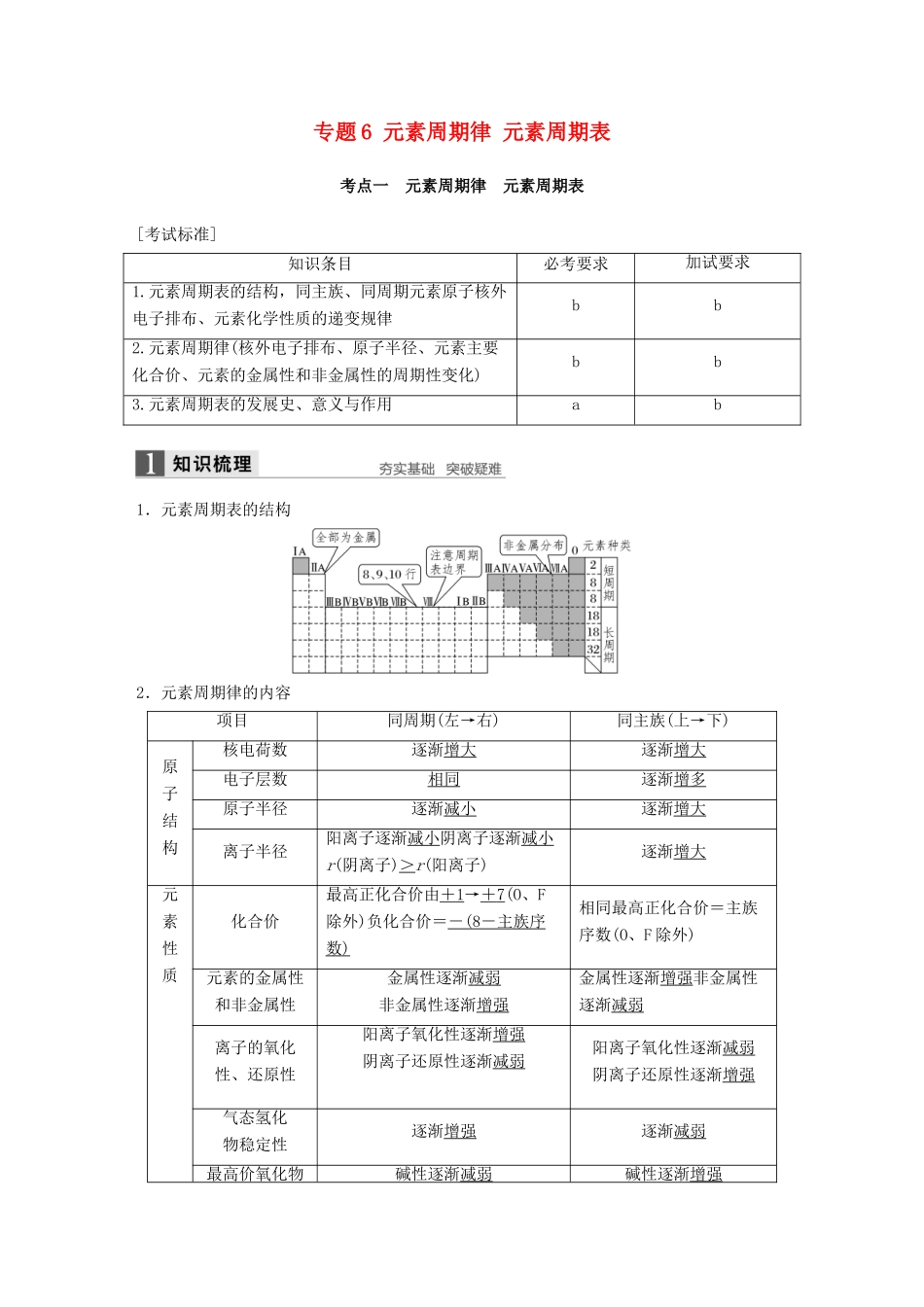
元素周期表的发展史、意义与作用ab1.元素周期表的结构2.元素周期律的内容项目同周期(左→右)同主族(上→下)原子结构核电荷数逐渐增大逐渐增大电子层数相同逐渐增多原子半径逐渐减小逐渐增大离子半径阳离子逐渐减小阴离子逐渐减小r(阴离子)>r(阳离子)逐渐增大元素性质化合价最高正化合价由+1→+7(O、F除外)负化合价=-(8-主族序数)相同最高正化合价=主族序数(O、F除外)元素的金属性和非金属性金属性逐渐减弱非金属性逐渐增强金属性逐渐增强非金属性逐渐减弱离子的氧化性、还原性阳离子氧化性逐渐增强阴离子还原性逐渐减弱阳离子氧化性逐渐减弱阴离子还原性逐渐增强气态氢化物稳定性逐渐增强逐渐减弱最高价氧化物碱性逐渐减弱碱性逐渐增强对应的水化物的酸碱性酸性逐渐增强酸性逐渐减弱3
元素周期表、元素周期律的应用(1)根据元素周期表中的位置寻找未知元素(2)预测元素的性质(由递变规律推测)①比较不同周期、不同主族元素的性质如:金属性Mg>Al、Ca>Mg,则碱性Mg(OH)2>Al(OH)3、Ca(OH)2>Mg(OH)2(填“>”、“<”或“=”)
②推测未知元素的某些性质如:已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2难溶;再如:已知卤族元素的性质递变规律,可推知元素砹(At)应为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt不溶于水等
(3)启发人们在一定区域内寻找新物质①半导体元素在金属与非金属分界线附近,如:Si、Ge、Ga等
②农药中常用元素在右上方,如:F、Cl、S、P、As等