考点12离子的检验与推断一、离子的检验1.检验离子的“三种方法”:①生成沉淀;②生成气体;③显现特殊颜色
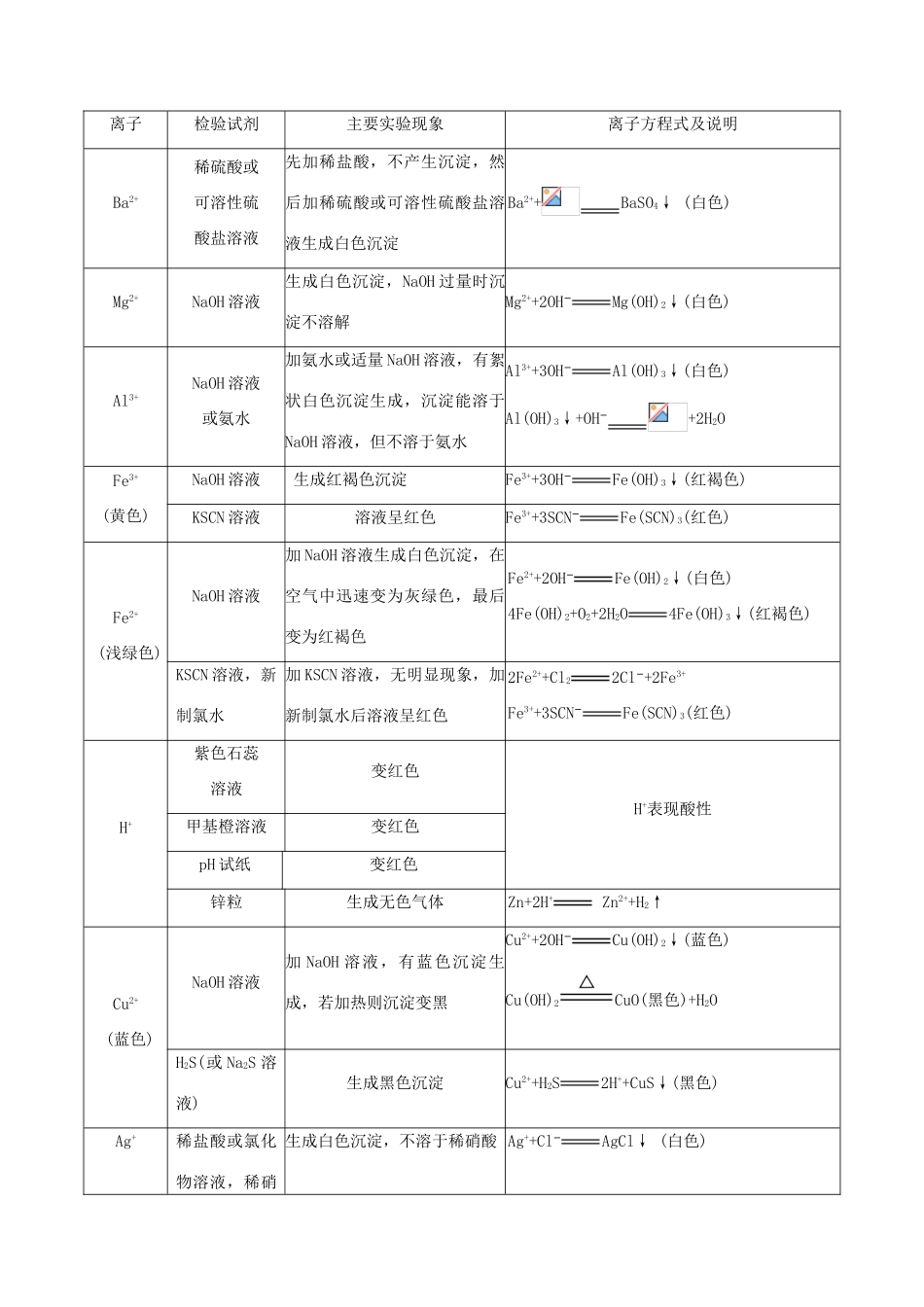
离子试剂现象注意沉淀法Cl-、Br-、I-稀HNO3和AgNO3溶液AgCl(白色)、AgBr(淡黄色)、AgI(黄色)—SO稀盐酸和BaCl2溶液白色沉淀先用稀盐酸酸化Fe2+NaOH溶液白色沉淀→灰绿色沉淀→红褐色沉淀—Fe3+NaOH溶液红褐色沉淀—Al3+NaOH溶液白色沉淀→溶解不一定是Al3+气体法NH浓NaOH溶液和湿润的红色石蕊试纸产生有刺激性气味且能使湿润的红色石蕊试纸变蓝的气体要加热CO稀盐酸和石灰水石灰水变浑浊SO、HSO、HCO有干扰SO稀H2SO4和品红溶液产生有刺激性气味且能使品红溶液褪色的气体—显色法I-氯水(少量),CCl4下层为紫色—Fe2+KSCN溶液和氯水先是无变化,滴加氯水后变血红色先加KSCN溶液,无变化,再加氯水Fe3+KSCN溶液血红色—Na+、K+Pt(Fe)丝和稀盐酸火焰分别呈黄色、紫色K+要透过蓝色钴玻璃观察焰色2.常见阳离子的检验离子检验试剂主要实验现象离子方程式及说明Ba2+稀硫酸或可溶性硫酸盐溶液先加稀盐酸,不产生沉淀,然后加稀硫酸或可溶性硫酸盐溶液生成白色沉淀Ba2++BaSO4↓(白色)Mg2+NaOH溶液生成白色沉淀,NaOH过量时沉淀不溶解Mg2++2OH−Mg(OH)2↓(白色)Al3+NaOH溶液或氨水加氨水或适量NaOH溶液,有絮状白色沉淀生成,沉淀能溶于NaOH溶液,但不溶于氨水Al3++3OH−Al(OH)3↓(白色)Al(OH)3↓+OH−+2H2OFe3+(黄色)NaOH溶液生成红褐色沉淀Fe3++3OH−Fe(OH)3↓(红褐色)KSCN溶液溶液呈红色Fe3++3SCN−Fe(SCN)3(红色)Fe2+(浅绿色)NaOH溶液加NaOH溶液生成白色沉淀,在空气中迅速变为灰绿色,最后变为红褐色